
19、质量分数为n的NaOH溶液,其物质的量浓度为a mol/L,加热蒸发水使其质量分数变为2n,此时,该溶液中的物质的量浓度为b mol/L,则a与b的关系正确的是( )
A、b=2a B、a=2b C、b﹥2a D、b﹤2a
18、下列实验或操作不合理的是 ( )
①钾的火焰颜色要透过蓝色钻玻璃观察
②用溴水检验汽油中是否含有不饱和脂肪烃
③将浓硫酸沿玻璃棒缓缓注入盛水的量筒中,边加边搅拌,以使产生的热量迅速散失
④用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
⑤仅用蒸馏水鉴别蔗糖、硫酸铜粉末、碳酸钙粉末
⑥配制一定物质的量浓度的氯化钠溶液,需要的玻璃仪器只有容量瓶、烧杯和玻璃棒
⑦用玻璃棒蘸取溶液滴在pH试纸中央,测定该溶液的pH
⑧向保温套中100mL小烧杯里,依次加入50mL0.5mol/L NaOH溶液和50mL0.55mol/L的盐酸溶液进行中和热测定。 ( )
A.③⑤⑥⑦ B.③④⑥ C.②④⑤⑧ D.①③④⑧
17、下列溶液中微粒的物质的量浓度关系正确的是
A.氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)]
B.Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+2 c(H2CO3)
C.等浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+ c(H2CO3)
D.室温下,向0.01 mol·L-1 NH4HSO4溶液中滴加NaOH溶液至中性:
c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
16、高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业上是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。
湿法制备的主要反应方程为:2Fe(OH)3+3ClO―+4OH―=2FeO42-+3Cl―+5H2O
干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4 +2Na2SO4
下列有关说法不正确的是
A.K2FeO4处理水时,不仅能消毒杀菌,还能吸附水中的悬浮杂质
B.湿法制备中每生成1 mol Na2FeO4转移3 mol电子
C.干法制备中每生成1 mol Na2FeO4转移4 mol电子
D.因为高铁酸钾氧化产物无污染,所以被称为绿色水处理剂
15、按下图所示装置进行实验(其中C1、C2均是石墨电极),下列说法中正确的是 ( )
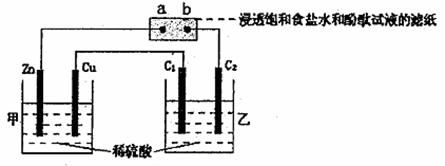
A.在通常状况下,Zn极减轻3.25g时,C2极上放出气体体积约为1.12L
B.发现b点附近显红色
C.在相同条件下,C1、C2电极所产生气体的体积比为2:1
D.乙池溶液的pH减小
14、短周期元素A、B、C、D、E的原子序数依次增大,A与D、C与E位于同一主族。D原子的内层电子总数是其最外层电子数的2.5倍,且D 的原子序数为A、C原子序数之和。下列叙述中正确的是( )
A. BC2、DC2、EC2的化学键类型和晶体类型都相同
B. AC2、AE2分子中所有原子最外层都满足8电子稳定结构
C.液态化合物AE2在足量氧气中燃烧,气体体积减少(相同状况)
D.EC2通入BaCl2溶液无任何现象,继续通入BC2也无沉淀生成
13、可逆反应aA(?)+2 B(g)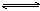 2C(g)+D(g),其中a为正整数。反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是( )
2C(g)+D(g),其中a为正整数。反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是( ) 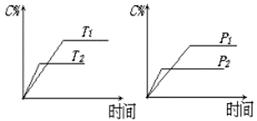
A.达到平衡后,加入催化剂则C%增大 B.达到平衡后,若升高温度,平衡向右移动
C.a可以为任意的正整数
D.达平衡后,增加A的量,有利于平衡向右移动
12、常温条件下,将SO2气体通入一定量NaOH溶液中,所得溶液呈中性,关于该溶液的判断错误的是( )
A.该溶液溶质一定为NaHSO3与Na2SO3 B.溶液中c(Na+)=c(SO32-)+c(HSO3-)
C.溶液中离子浓度最大的是Na+
D.向该溶液中加入氯化钾固体,溶液依然呈中性,且有c(K+)=c(Cl-)
11、下列各组物质的溶液,不用其他试剂,也不用焰色反应就能将它们区别开来的是
A.AgNO3、NaCl、BaCl2、NaOH B.K2CO3 、KHCO3 、HCl 、H2SO4
C.Na2CO3、NaHSO4、Ba(NO3)2、KCl D.KNO3 、 NaCl 、BaCl2、(NH4)2SO4
10、某溶液中存在XO3―,且X为短周期元素,则一定能在该溶液中大量共存的离子组是
A.Na+、H+、SO42―、I― B.Na+、Ca2+、CO32―、Al3+
C.Na+、K+、Fe2+、H+ D.K+、SO42―、Cl―、CO32―
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com