
14.在硫酸铝、硫酸钾和明矾的混合溶液中,如果c(SO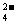 )=0.2 mol/L,当加入等体积、0.2 mol/L的KOH溶液时,恰好沉淀完全,则所得溶液中K
)=0.2 mol/L,当加入等体积、0.2 mol/L的KOH溶液时,恰好沉淀完全,则所得溶液中K 的物质的量浓度是(
)
的物质的量浓度是(
)
A.0.2 mol/L B.0.25 mol/L C.0.1 mol/L D.0.225 mol/L
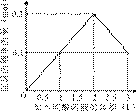
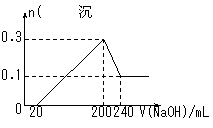 15将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入5mol/L NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如下图所示。则下列说法不正确的是
( )
15将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入5mol/L NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如下图所示。则下列说法不正确的是
( )
A.镁和铝的总质量为9 g
B.最初20 mLNaOH溶液用于中和过量的硫酸
C.硫酸的物质的量浓度为2.5 mol·L-1
D.生成的氢气在标准状况下的体积为11.2 L
13.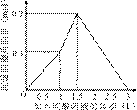
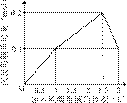
 在1 L含0.1 mol NaAlO2和0.1 mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.1
mol/L的H2SO4溶液,下列图象中能表示反应产生沉淀的物质的量与加入硫酸溶液体积之间关系的是
( )
在1 L含0.1 mol NaAlO2和0.1 mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.1
mol/L的H2SO4溶液,下列图象中能表示反应产生沉淀的物质的量与加入硫酸溶液体积之间关系的是
( )
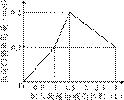
A B C D
12.下列表中对于相关物质的分类全部正确的一组是
|
编号 |
纯净物 |
混合物 |
弱电解质 |
非电解质 |
|
A |
明矾 |
蔗糖 |
NaHCO3 |
CO2 |
|
B |
天然橡胶 |
石膏 |
SO2 |
CH3CH2OH |
|
C |
冰 |
王水 |
H2SiO3 |
Cl2 |
|
D |
胆矾 |
玻璃 |
H2CO3 |
NH3 |
11.用48 mL 0.1 mol/L的FeSO4溶液,恰好还原2.4×10-3 mol[RO(OH)2]+离子,则R元素的最终价态为 ( )
A.+2 B.+3 C.+4 D.+5
10.对下列各种溶液中大量共存离子的判断合理的是
A.向无色溶液中加氯水,溶液变为橙色,溶液中一定有:SO42-、Br-、NO3-、Ag+
B.使酚酞试液变红的溶液中可能有:K+、Na+、NH4+、HCO3-
C.在水电离出的c(H+)=10-8 mol/L 的溶液中可能有:Na+、AlO2-、CO32-、SO32-
D.向溶液中加铝粉有氢气放出,则该溶液中一定有:K+、Na+、H+、NO3-
9.用等体积的0.1mol/L的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液的SO42-完全沉淀,则三种硫酸盐的物质的量浓度之比为
A.3∶2∶3 B.3∶1∶2 C.2∶6∶3 D.1∶1∶1
7.某电解质溶液中含 K+、H+、SO42-等离子,这三种离子的物质的量浓度相等,对于该电解质溶液,下列说法正确的是
A.该电解质溶液中有可能同时大量存在 Fe2+、NO3-
B.配制该电解质溶液一定要用硫酸氢钾作溶质
C.若该溶液还含 Fe2+、Cl-,则一定存在 2c(Fe2+)=c(Cl-)
D.向该溶液中加入漂白粉,可能有黄绿色气体产生
8?已知Fe3O4可表示成(FeO·Fe2O3),水热法制备Fe3O4纳米颗粒的总反应为:
3Fe2++2S2O32-+O2+4OH-=Fe3O4+S4O62-+2H2O,下列说法正确的是
A.O2和S2O32-是氧化剂,Fe2+是还原剂
B.每生成1molFe3O4,则转移电子数为 2mol
C.参加反应的氧化剂与还原剂的物质的量之比为 1∶1
D.若有 2molFe2+被氧化,则被 Fe2+还原的O2为 0.5mol
6.下列离子方程式正确的是
A.向NaHCO3溶液中加入足量的澄清石灰水:HCO3-+OH-+Ca2+=CaCO3↓+H2O
B.氨水吸收少量的二氧化硫:NH3·H2O+SO2=NH4++HSO3-
C.向AgCl悬浊液中加入饱和NaI溶液反应的离子方程式:Ag++I-=AgI↓
D.用稀硝酸溶解 FeS固体:FeS+2H+=Fe2++H2S↑
5.将铁、铝、硅的混合物分为等质量的两份,一份跟足量的NaOH溶液反应,另一份跟足量稀H2SO4反应,最终产生的H2一样多,则铁与硅物质的量之比为( )
A.2∶1 B.4∶1 C.1∶1 D.3∶1
4.下列物质反应后一定有+3价铁生成的是( )
①过量的Fe与Cl2反应;
②Fe与过量稀H2SO4反应后,再向其中加KNO3;
③Fe(NO3)2溶液中加少量盐酸;
④Fe和Fe2O3的混合物溶于盐酸中。
A.只有①② B.只有②③ C.只有①②③ D.全部
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com