
16.已知甲、乙、丙分别代表中学化学中的常见物质,请根据题目要求完成下列问题:
(1)甲的化学式为RCl3,其溶液在加热蒸干并灼烧时可发生反应:
a.甲+H2O 乙+丙 b.乙
乙+丙 b.乙 氧化物+H2O
氧化物+H2O
①若甲为某用途广泛的金属元素的氯化物,其溶液在上述变化中生成的氧化物为红棕色粉末,则该金属在周期表里的位置是:____________________。
②若甲为某短周期金属元素的氯化物,则甲发生a反应的化学方程式为:________________。
③将以上两种金属单质用导线连接,插入NaOH溶液构成原电池,则负极发生的电极反应为:_______________。
(2)若甲、乙、丙均是短周期中同一周期元素形成的单质或化合物,常温下乙为固体单质,甲和丙均为气态化合物,且可发生反应:甲+乙 丙。则:
丙。则:
①甲的结构式为______________________。
②写出上述反应的化学方程式:___________________。
③写出向200 mL 2 mol·L-1的NaOH溶液中通入6.72 L(标准状况)的气体甲发生完全反应的总离子方程式______________________。
15.有Ba(OH)2、NaHSO4、NaHCO3三种溶液,已知其中两种溶液的物质的量浓度相同,且分别为另一种溶液的物质的量浓度的2倍;若先将NaHSO4和NaHCO3溶液各 100 mL混合反应后,再加入Ba(OH)2溶液100mL,充分反应后,将生成的白色沉淀滤出,测得滤液中只含一种NaOH溶质,其物质的量的浓度为0.9mol/L(不考虑溶液混和时引起溶液体积的变化),试回答:
(1)通过分析,判断原Ba(OH)2、NaHSO4、NaHCO3三种溶液中哪两种溶液的物质的量的浓度不可能相同? ,原因是 。
(2)Ba(OH)2、NaHSO4、NaHCO3三种溶液可能的物质的量的浓度分别为__________、_________、_________。
14.将等质量混合的铜、锌、铁三种金属组成的混合物W g 加入到FeCl3和盐酸组成的混合液中,充分反应后:
(1)若无固体剩余,则溶液中一定有的金属离子是_____________________,可能有的金属离子是______。
(2)若剩余固体W/3g,则溶液中金属离子一定有_____________________,一定没有________________。
13.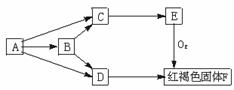 按下图要求写出下列两个反应的化学方程式,属于离子反应的写出离子方程式。
按下图要求写出下列两个反应的化学方程式,属于离子反应的写出离子方程式。
(1)B→C+D________________________________;
(2)E→F___________________________________。
12.把一支表面被氧化成10.2g氧化铝的铝条A,放入1L1.5mol/L热氢氧化钠溶液中,过一段时间后取出铝条,溶液质量增加了12.6g,此时的溶液称为甲溶液,体积仍为1L。再把另一支表面也被氧化的一定量的铝条B,放入1L0.9mol/L硫酸溶液中,过一会儿取出,其质量减小了25.8g,溶液的质量增加了25.2g,此时的溶液称为乙溶液,体积仍为1L。回答下列问题: (1)甲溶液的溶质是________________(写化学式),其物质的量_____________________。
(2)乙溶液的溶质是_______________________(写化学式),其物质的量是__________。
(3)将甲、乙两溶液反应,若使滴加的量最少,而产生的沉淀最多,应将________溶液______L滴加到_________溶液(用“甲”或“乙”填写),产生的沉淀最多是_______g。
11.将一定量的NaOH和NaHCO3的混合物A,放在密闭容器中加热,充分反应后生成气体V1L(V1≠0)。将反应后的固体残渣B与过量盐酸反应,又生成CO2V2L。(气体体积在标准状况下测定)
(1)B的成分是______________。
A.Na2CO3与NaOH B.Na2CO3与NaHCO3
C.Na2CO3 D.NaOH
(2)A中NaOH与NaHCO3共_____________mol;NaOH与NaHCO3物质的量之比为_____________。
10.将5.6 g Fe投入浓硝酸溶液,产生红棕色气体A,把所得溶液减压蒸干,得到20g Fe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红褐色的Fe2O3和气体B,A、B气体混合通入足量水中,在标准状况下剩余气体的物质的量为
A.2240mL B.4480mL C.3360mL D.1120mL
9.将含O2和CH4的混合气体充入装有23.4gNa2O2的密闭容器中点燃,反应结束后,容器温度为150℃,压强为0pa,将残留物溶于水无气体逸出。下列叙述正确的是
A.原混合气体中O2和CH4的体积比为2:1
B.原混合气体中O2和CH4的体积比为1:2
C.残留固体中有Na2CO3和NaOH
D.残留固体中只有Na2CO3
8.冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或氢气,或一氧化碳)法;③活泼金属置换法;④电解法。四种方法在工业上均有应用。古代有(Ⅰ)火烧孔雀石炼铜;(Ⅱ)湿法炼铜;现代有(Ⅲ)铝热法炼铬;(Ⅳ)从光卤石中炼镁,对它们的冶炼方法的分析不正确的是
A.(Ⅰ)用① B.(Ⅱ)用②
C.(Ⅲ)用③ D. (Ⅳ)用④
7.0.001mol金属放入10mL0.1mol/L某酸溶液中,产生22.4mL氢气(标准状况),下列情况中一定不可能的是
A.一价金属和一元酸 B.二价金属和二元酸
C.三价金属和二元酸 D.二价金属和一元酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com