
4.(8分)(08年山东理综·31)[化学--化学与技术]
钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在__________部分发生反应,在 __________部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为_________;加入硅、锰和铝的目的是_________。
(3)不锈钢含有的Cr元索是在炼钢过程的氧吹_________(填“前”或“后”)加入,原因是 _______________。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作_________。
答案:
(1)炉身 炉腰
(2)2P+5FeO+3CaO
 Ca3(PO4)2+5Fe 脱氧和调整钢的成分
Ca3(PO4)2+5Fe 脱氧和调整钢的成分
(3)后 避免Cr被氧化(或“氧吹前加入Cr会形成炉渣被除去”)
(4)CO 燃料(或还原剂)
3.(11分)(08年海南化学·29)如何防止铁的锈蚀是工业上研究的重点内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
|
序号 |
内容 |
实验现象 |
|
1 |
常温下将铁丝放在干燥空气中一个月 |
干燥的铁丝表面依然光亮 |
|
2 |
常温下将铁丝放在潮湿空气中一小时 |
铁丝表面依然光亮 |
|
3 |
常温下将铁丝放在潮湿的空气中一个月 |
铁丝表面已变得灰暗 |
|
4 |
将潮湿的铁丝放在常温的氧气流中一小时 |
铁丝表面略显灰暗 |
|
5 |
将潮湿的铁丝放在高于常温的氧气流中一小时 |
铁丝表面已变得灰暗 |
|
6 |
将浸过氯化钠溶液的铁丝放在高于常温的氧气流中一小时 |
铁丝表面灰暗程度比实验5严重 |
回答以下问题:
(1)上述实验中发生了电化学腐蚀的是(填实验序号) ;在电化学腐蚀中,负极反应是 ;正极反应是 。
(2)由该实验可知,可以影响铁锈蚀速率的因素是 。
(3)为防止铁的锈蚀,工业上普遍采用的方法是 (答两种方法)。
答案:(11分)(1)3、4、5、6 Fe-2e-=Fe2+(或2Fe-4e-=2Fe2+) O2+4e-+2H2O=4OH-
(2)湿度、温度、O2的浓度、电解质存在 (3)电镀、发蓝等表面覆盖层,牺牲阳极的阴极保护法等(其他合理答案也给分)
解析:工业上铁的锈蚀主要是电化学腐蚀,发生电化学腐蚀的条件是:活性不同的两极材料,电解质溶液,形成闭合回路。影响锈蚀速度的因素有:环境的温度、湿度、电解质存在、O2的浓度等。实验条件为有氧,为吸氧腐蚀:
负极:Fe-2e→Fe2+ 正极:O2+2H2O+4e→4OH-
保护钢铁不被腐蚀的措施
①外加保护层如:涂漆、搪瓷、电镀、表面钝化、油脂等。
②改变钢铁的内部结构,冶炼不锈钢。
③在钢铁的表面镶嵌比铁活泼的金属如锌,使活泼金属被氧化,而钢铁被保护。
34.[化学--选修化学与技术](15分)
(1)①造纸厂排放的碱性污水使X处河水pH升高,火力发电厂净化烟气的酸性废水治理未达标就排放,造成Y处等的河水,pH降低(或火力发电厂燃烧产生的SO2会导致酸雨,飘落后使Y处等的河水pH降低)
②化肥厂、农田及生活污水使Z处河水富营养化,水温较高,适于藻类等水生植物生长,河水中溶解氧被大量消耗,导致鱼类死亡
(2)①发电厂 焦化厂 炼铁厂 水泥厂
②Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
CaCO3+SiO2
 CaSiO3+CO2↑
CaSiO3+CO2↑
③
用炼铁厂的炉渣(或CaSiO3)作为水泥厂的原料
用发电厂的煤矸石和粉煤灰作为水泥厂的原料
将石灰石煅烧成生石灰,用于吸收发电厂和焦化厂烯煤时产生的SO2,减少对空气的污染建立污水处理系统
解析:A为发电厂,因为发电需要煤炭,且其为另外三厂提供电能,B为焦化厂,C的原料为赤铁矿和碳酸钙,碳酸钙可提供二氧化碳,制造水泥需要粘土。造纸厂排放的碱性污水使X处河水pH升高,火力发电厂净化烟气的酸性废水治理未达标就排放,造成Y处等的河水,pH降低(或火力发电厂燃烧产生的SO2会导致酸雨,飘落后使Y处等的河水pH降低),化肥厂、农田及生活污水使Z处河水富营养化,水温较高,适于藻类等水生植物生长,河水中溶解氧被大量消耗,导致鱼类死亡
2.[化学--选修化学与技术](15分)(08年宁夏理综·34)
分析下面两个案例并回答有关问题。
(1)某城镇生产、生活的分布情况如图所示,河流中W、X、Y、Z处某次水样抽测结果如表所示。

|
地点 项目 |
W |
X |
Y |
Z |
|
水温/℃ |
15 |
18 |
26 |
25 |
|
pH |
6 |
8 |
5 |
5 |
|
溶解氧量/(mg·L-1) |
11 |
9 |
7 |
3 |
①导致X、Y处水样pH变化的原因可能是 ;
②Z处鱼类大量减少,产生这种现象的原因可能是 。
(2)某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O3,还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。
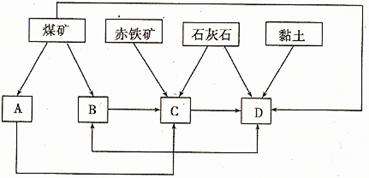
①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系。据此确定上图中相应工厂的名称A 、B 、C 、D ;
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式 ;
③从“三废”利用、环境保护等角度考虑,该地区和企业在生产中应采取的一些措施有(举出2种措施即可) 。
9.8×109g x y
则 ,解得x=8.0×103t y=9.83×109kJ。
,解得x=8.0×103t y=9.83×109kJ。
1.(07年宁夏理综·31A)化学选考题(15分)A.[化学-选修化学与技术]
工业上生产硫酸时,利用催化氧化反应将SO2 转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2 7% O2 11% N2 82%);
 |
0.1 |
0.5 |
1 |
10 |
|
400 |
99.2 |
99.6 |
99.7 |
99.9 |
|
500 |
93.5 |
96.9 |
97.8 |
99.3 |
|
600 |
73.7 |
85.8 |
89.5 |
96.4 |
(1) 已各SO2的氧化是放热反应,如何利用表中数据推断此结论?
;
(2)在大400~500℃时,SO2的催化氧化采用常压而不是高压,主要原因是:
;
(3)选择适宜的催化剂,是否可以提高SO2的转化率? (填“是”或“否”),是否可以增大该反应所放出的热量? (填“是”或“否”);
(4)为提高SO3吸收率,实际生产中用 吸收SO3;
(5)已知:2SO2(g)+O2(g)=2SO3(g);△H=-196.9kJ·mol-1,计算每生产1万吨98%硫酸所需要的SO3质量和由SO2生产这些SO3所放出的热量。
答案:(1)压强一定时,温度升高时,SO2转化率下降,说明升温有利逆反应的进行,所以正反应为放热反应。(2)增大压强对提高SO2转化率无显著影响,反而会增加成本。(3)否 否 (4)浓硫酸 (5)8.0×103t 9.83×109kJ
解析:(1)根据表格中的数据可以看出,在相同压强下(如在0.1MPa下)升高温度(如由400℃升高到500℃)时SO2的转化率降低(由99.2%降低为93.5%),即升高温度时此化学平衡向逆反应方向移动,而升高温度化学平衡应该向吸热反应方向移动,所以此反应的正反应为放热反应。
(2)根据表格中的数据可以得知:在0.1MPa(即常压1atm下)SO2的转化率已经很高,如在400℃时已达99.2%,若增大压强到10MPa(即100atm),压强增大了100倍但是SO2的转化率值增大为99.9%,只增大了0.7%变化不大。而压强增大100倍,需要对设备的材料、动力、能源等都作相应的提高,既要增大成本投入。
(3)使用催化剂只能改变化学反应的速率,改变反应到达平衡的时间,不能使化学平衡发生移动,即对SO2的转化率不产生影响;而在一定条件下,化学反应放出的热量与参加反应的反应物的量成正比,因SO2的转化率不变,所以反应放出的热量也不会增大。
(4)在生产实际中是采用98.3%的浓硫酸作吸收剂来吸收SO3的。因为若用水进行吸收会形成酸雾,将影响SO3的吸收速率和效率。
(5)1万吨98%的硫酸含H2SO4的质量:9.8×109g。 设需要SO3的质量为x,该反应产生的热量为y。
H2SO4 - SO3 - 放出的热量
98g 80g 196.9kJ
1.(07年山东理综·31)(8分)[化学-化学与技术]
 工业上对海水资源合开发利用的部分工艺流程如右图所示。
工业上对海水资源合开发利用的部分工艺流程如右图所示。
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽,离子膜和隔膜均允许通过的分子或离子是 。电解槽中的阳极材料为 。
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4顺序制备? 原因是 。
(3)溴单质在四氧化碳中的溶解度比在水中大得多,四氧化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氧化碳,原因是 。
答案:(1)阳离子(或Na+) 钛(或石墨)
(2)否。如果先沉淀Mg(OH)2,则沉淀中会夹杂有CaSO4沉淀,产品不纯。
(3)四氯化碳萃取法工艺复杂、设备投资大;经济效益低、环境污染严重。
解析:(1)工业上用离子交换膜法电解食盐水时采用的阳离子交换膜只允许Na+通过,隔膜电解槽中的隔膜只允许水和离子通过,则二者均允许通过的离子或分子共同的是阳离子(或Na+),电解槽中用来做阳极的是钛或石墨。
(2)硫酸钙是微溶性的物质,如果先反应生成氢氧化镁,加入石灰水生成氢氧化镁沉淀的同时,过量的Ca(OH)2会生成硫酸钙沉淀,造成产品中有杂质,使产品不纯。
(3)用四氯化碳萃取溴时需要的工艺复杂,设备投资大,并且四氯化碳会造成环境污染。
20.(2007海南·29)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。请按要求回答问题:
(1)“氨碱法”产生大量CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式: ;
(2)写出“联合制碱法”有关反应的化学方程式: ;
;
(3)CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同? ;
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列出计算原子利用率的表达式:
原子利用率(%)= 。
答案:(1)2NH4Cl +Ca(OH)2  CaCl2 +2NH3↑+2H2O
CaCl2 +2NH3↑+2H2O
(2)NH3 +H2O +CO2 +NaCl(饱和)=NaHCO3↓+ NH4Cl
2NaHCO3 Na2CO3 +CO2↑+H2O
Na2CO3 +CO2↑+H2O
(3)前者的CO2 来自合成氨厂,后者的CO2 来自煅烧石灰石。
(4)×100%=100%
考点:本题考查了氨碱法和联合制碱法的原理。
解析:明确氨碱法和联合制碱法的化学反应原理。“联合制碱法”原子利用率的表达式为:原子利用率(%)= 。
。
19. (09年海南化学·20.3)下列有关硬水及其软化的说法中错误的是:
(09年海南化学·20.3)下列有关硬水及其软化的说法中错误的是:
 A.离子交换法可以软化硬水
A.离子交换法可以软化硬水
 B.硬水中含有较多Ca2+、Mg2+
B.硬水中含有较多Ca2+、Mg2+
 C.生产、生活使用的天然水必须经软化
C.生产、生活使用的天然水必须经软化
 D.加热可使暂时硬水中的Ca2+生成CaCO3沉淀
D.加热可使暂时硬水中的Ca2+生成CaCO3沉淀
答案:C
解析:A、B、D是一些常识,C中生活使用的硬水不是“必须”经软化使用。
18. (09年海南化学·20.2)下列使用化肥、农药的描述中正确的是:
(09年海南化学·20.2)下列使用化肥、农药的描述中正确的是:
 A.高温多雨时比较适合施用钾肥
A.高温多雨时比较适合施用钾肥
 B.长期施用硫铵会造成土壤板结
B.长期施用硫铵会造成土壤板结
 C.石硫合剂必须与硫酸混合后才能施用
C.石硫合剂必须与硫酸混合后才能施用
 D.过磷酸钙必须经硫酸处理后才能施用
D.过磷酸钙必须经硫酸处理后才能施用
答案:B
解析:A中钾肥易溶于水,多雨时易造成化肥的流失;B中硫铵溶于水呈酸性,易破坏土壤的胶体结构使土壤板结;C中石硫合剂主要成分是多硫化钙,具有渗透和侵蚀病菌细胞及害虫体壁的能力,能在植物体表面形成一层药膜起保护作用,如果和硫酸混合后施用,会生成硫酸钙使石硫合剂失去作用。D中有效成份为Ca(H2PO4)2,属水溶性速效磷肥,应直接使用。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com