
1.怎样清除玻璃仪器上粘附的不易溶于水的下列物质?
(1)碳酸盐:(稀盐酸)(2)氢氧化物(氢氧化亚铁、氢氧化铜等):(稀盐酸)(3)二氧化锰:(浓盐酸、加热)(4)硫:(CS2或碱液煮沸)(5)银盐:(Na2S2O3)(6)油污:(NaOH或热纯碱液)(7)苯酚:(NaOH或酒精)(8)FeS:(稀H2SO4)(9)碘:(酒精)
下列各组物质均可以用一种试剂鉴别开来
|
被鉴别的物质组 |
所加的试剂 |
|
⑴NaCl NH4Cl Na2CO3
(NH4)2SO4
|
Ba(OH)2 |
|
⑵NaHCO3 Na2S2O3 Na2SiO3
K2SO3 KCl K2S |
盐酸或稀H2SO4 |
|
⑶AlCl3 FeCl2 KCl NH4NO3 Fe(NO3)3
MgSO4 |
NaOH或Ba(OH)2 |
|
⑷盐酸 AlCl3 BaCl2 Fe2(SO4)3 KOH |
Na2CO3 |
|
⑸Fe FeO CuO FeS CuS MnO2 |
浓盐酸(有的要加热) |
|
⑹NaNO3 NH3·H2O
BaCl2
Na2S KI |
Fe2(SO4)3或AgNO3 |
|
⑺氢硫酸 KI AgNO3 NaHCO3 NaCl |
氯水或FeCl3 |
|
⑻KNO3 Pb(NO3)2
NaHCO3
Ba(OH)2 |
(NH4)2SO4或Fe2(SO4)3 |
|
⑼KOH
HCl BaCl2 KCl AlCl3 FeCl3 |
(NH4)2CO3 |
|
⑽Pb(NO3)2 CH3COOH AlCl3 NaCl |
Na2S或Na2CO3 |
|
⑾NaBr NaI Na2CO3 NaCl Na2SO4 Na2S |
浓H2SO4 |
|
⑿苯酚 甲苯 己烯 己醇 四氯化碳 |
溴水 |
|
⒀KSCN KI Na2CO3 苯酚 |
FeCl3 |
|
⒁甲酸 乙酸 乙醛 乙醇 葡萄糖 |
新制Cu(OH)2悬浊液并加热 |
常见分子的类型与形状比较
|
分子类型 |
分子形状 |
键角 |
键的极性 |
分子极性 |
代表物 |
|
A |
球形 |
|
|
非极性 |
He Ne |
|
A2 |
直线形 |
|
非极性 |
非极性 |
H2 O2 |
|
AB |
直线形 |
|
极性 |
极性 |
HCl NO |
|
ABA |
直线形 |
180° |
极性 |
非极性 |
CO2 CS2 |
|
ABA |
角形 |
≠180° |
极性 |
极性 |
H2O SO2 |
|
A4 |
正四面体形 |
60° |
非极性 |
非极性 |
P4 |
|
AB3 |
平面三角形 |
120° |
极性 |
非极性 |
BF3 SO3 |
|
AB3 |
三角锥形 |
≠120° |
极性 |
极性 |
NH3 NCl3 |
|
AB4 |
正四面体形 |
109°28′ |
极性 |
非极性 |
CH4 CCl4 |
|
AB3C |
四面体形 |
≠109°28′ |
极性 |
极性 |
CH3Cl CHCl3 |
|
AB2C2 |
四面体形 |
≠109°28′ |
极性 |
极性 |
CH2Cl2 |
重要物质的俗称、用途小结一览表
|
化学式 |
俗称或主要成分 |
用途 |
|
PCl3 |
|
敌百虫的主要成分 |
|
CaCl2、Ca(ClO)2 |
漂白粉(混) |
|
|
CaF2 |
萤石 |
制HF |
|
NaF |
|
杀死地下害虫的农药 |
|
AgBr |
|
感光片 |
|
AgI |
|
人工降雨 |
|
FeS2 |
黄铁矿(硫铁矿)(混) |
制硫酸 |
|
CuFeS2 |
黄铜矿(混) |
|
|
CaSO4·2H2O |
石膏 |
调节水泥硬化速度、绷带 |
|
2CaSO4·H2O |
熟石膏 |
|
|
Na2SO4·10H2O |
芒硝 |
缓泻剂、玻璃、造纸、…… |
|
SO2 |
|
漂白、杀菌 |
|
ZnSO4·7H2O |
皓矾 |
收敛剂、防腐剂、媒染剂 |
|
BaSO4 |
重晶石 |
钡餐 |
|
Na2CO3 |
纯碱、苏打 |
玻璃、肥皂、造纸、纺织、洗涤剂 |
|
NaHCO3 |
小苏打 |
发酵粉、治疗胃酸过多 |
|
Na2S2O3 |
大苏打、海波 |
定影剂 |
|
K2CO3 |
草木灰(混) |
钾肥 |
|
HNO3(浓):3HCI(浓) |
王水 |
溶Au、Pt |
|
SiO2 |
水晶(纯净物)、硅藻土、石英 |
装饰玻璃、光导纤维、建筑等 |
|
Na2SiO3 |
水玻璃 |
粘合剂、耐水材料、防腐性能 |
|
Mg2SiO4 |
硅酸盐(混) |
砖瓦、陶瓷、水泥…… |
|
AI2(SiO5)(OH)4 |
||
|
KaISi3O8 |
||
|
Na2SiO3 CaSiO3、SiO2 |
普通玻璃(混) |
建材 |
|
2CaO·SiO2 2CaO·AI2O3 3CaO·AI2O3 |
水泥(混) |
建筑 |
|
AI+Fe2O3 |
铝热剂(混) |
焊接钢轨、冶炼 |
|
KCI·MgCI2·6H2O |
光卤石 |
制Mg |
|
AI2O3·H2O、AI2O3·3H2O +Fe2O3 |
铝土矿(矾土矿)(混) |
制AI |
|
AI2O3 |
刚玉、宝石 |
|
|
Fe2O3 |
铁红 |
油漆颜料 |
|
Fe2O3 |
赤铁矿(混) |
炼钢、炼铁 |
|
Fe3O4 |
磁性氧化铁、磁铁矿(混) |
|
|
2Fe2O3·3H2O |
褐铁矿(混) |
|
|
FeCO3 |
菱铁矿(混) |
|
|
MgCO3 |
菱镁矿(混) |
|
|
SiO2 |
脉石(混) |
|
|
CO、CO2、N2 |
高炉煤气(混) |
回收CO再利用 |
|
CO、Fe2O3 |
炼钢尾气(混) |
|
|
CH4 |
天然气、沼气(混) |
燃料 |
|
NaOH、CaO |
碱石灰(混) |
干燥剂 |
|
CHCI3 |
氯仿(三氯甲烷) |
溶剂 |
|
CaC2 |
电石 |
制乙炔 |
|
H2、CH4、C2H4、CO |
焦炉煤气(混) |
燃料、化工原料 |
|
CH3OH |
木精、木醇 |
|
|
HOCH2CHOHCH2OH |
甘油(丙三醇) |
硝化甘油 |
|
HCHO 35%~45%甲醛 |
蚁醛 福尔马林(混) |
杀菌、消毒 |
|
CH3COOH |
冰酯酸 |
|
|
C17H35COOH |
硬酯酸 |
|
|
C15H31COOH |
软酯酸 |
|
|
C17H33COOH |
油酸 |
|
|
高级脂肪酸、甘油酯 |
油脂、植物油、脂肪(混) |
|
|
(C6H3OHCH2)n |
酚醛树脂 |
电木 |
|
硬脂酸甘油酯 |
人造脂肪 |
肥皂、脂肪酸…… |
|
Ca(H2PO4)2+2CaSO4 |
普钙 |
磷肥 |
|
Ca(H2PO4)2 |
重钙 |
|
|
C6H12O6 |
葡萄糖 |
营养品 |
|
C6H12O6 |
果糖 |
食品工业 |
|
C12H22O11 |
蔗糖 |
|
|
C12H22O11 |
麦芽糖 |
|
|
(C6H10O5)n |
淀粉 |
食品 |
|
(C6H10O5)n |
纤维素 |
火棉、胶棉 |
|
CO+H2 |
水煤气 |
燃料 |
|
Na3AIF6 |
冰晶石 |
熔剂 |
|
NH4HCO3 |
气肥、碳铵 |
氮肥 |
|
N2O |
笑气 |
|
|
SiC |
金刚砂 |
|
|
(NH2)2CO |
尿素(碳酰二胺) |
氮肥 |
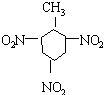 |
TNT (2,4、6一三硝基甲苯) |
烈性炸药 |
中学化学常见气体的实验室制法
⑴氧气
制取原理--含氧化合物自身分解
制取方程式--2KClO3=2KCl+3O2↑
装置--略微向下倾斜的大试管,加热
检验--带火星木条,复燃
收集--排水法或向上排气法
⑵氢气
制取原理--活泼金属与弱氧化性酸的置换
制取方程式--Zn+H2SO4 === Zn2SO4+H2↑
装置--启普发生器
检验--点燃,淡蓝色火焰,在容器壁上有水珠
收集--排水法或向下排气法
⑶氯气
制取原理--强氧化剂氧化含氧化合物
制取方程式--MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
装置--分液漏斗,圆底烧瓶,加热
检验--能使湿润的蓝色石蕊试纸先变红后褪色;
除杂质--先通入饱和食盐水(除HCl),再通入浓H2SO4(除水蒸气)
收集--排饱和食盐水法或向上排气法
尾气回收--Cl2+2NaOH=== NaCl+NaClO+H2O
⑷硫化氢
①制取原理--强酸与强碱的复分解反应
②制取方程式--FeS+2HCl=== FeCl2+H2S↑
③装置--启普发生器
④检验--能使湿润的醋酸铅试纸变黑
⑤除杂质--先通入饱和NaHS溶液(除HCl),再通入固体CaCl2(或P2O5)(除水蒸气)
⑥收集--向上排气法
⑦尾气回收--H2S+2NaOH=== Na2S+H2O或H2S+NaOH=== NaHS+H2O
⑸二氧化硫
①制取原理--稳定性强酸与不稳定性弱酸盐的复分解
②制取方程式--Na2SO3+H2SO4=== Na2SO4+SO2↑+H2O
③装置--分液漏斗,圆底烧瓶
④检验--先通入品红试液,褪色,后加热又恢复原红色;
⑤除杂质--通入浓H2SO4(除水蒸气)
⑥收集--向上排气法
⑦尾气回收--SO2+2NaOH=== Na2SO3+H2O
⑹二氧化碳
①制取原理--稳定性强酸与不稳定性弱酸盐的复分解
②制取方程式--CaCO3+2HClCaCl2+CO2↑+H2O
③装置--启普发生器
④检验--通入澄清石灰水,变浑浊
⑤除杂质--通入饱和NaHCO3溶液(除HCl),再通入浓H2SO4(除水蒸气)
⑥收集--排水法或向上排气法
⑺氨气
①制取原理--固体铵盐与固体强碱的复分解
②制取方程式--Ca(OH)2+2NH4ClCaCl2+NH3↑+2H2O
③装置--略微向下倾斜的大试管,加热
④检验--湿润的红色石蕊试纸,变蓝
⑤除杂质--通入碱石灰(除水蒸气)
收集--向下排气法
⑻氯化氢
①制取原理--高沸点酸与金属氯化物的复分解
②制取方程式--NaCl+H2SO4Na2SO4+2HCl↑
③装置--分液漏斗,圆底烧瓶,加热
④检验--通入AgNO3溶液,产生白色沉淀,再加稀HNO3沉淀不溶
⑤除杂质--通入浓硫酸(除水蒸气)
⑥收集--向上排气法
⑼二氧化氮
①制取原理--不活泼金属与浓硝酸的氧化-还原;
②制取方程式--Cu+4HNO3===Cu(NO3)2+2NO2↑+2H2O
③装置--分液漏斗,圆底烧瓶(或用大试管,锥形瓶)
④检验--红棕色气体,通入AgNO3溶液颜色变浅,但无沉淀生成
⑤收集--向上排气法
⑥尾气处理--3NO2+H2O===2HNO3+NO
NO+NO2+2NaOH===2NaNO2+H2O
⑩一氧化氮
①制取原理--不活泼金属与稀硝酸的氧化-还原;
②制取方程式--Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
③装置--分液漏斗,圆底烧瓶(或用大试管,锥形瓶)
④检验--无色气体,暴露于空气中立即变红棕色
⑤收集--排水法
⑾一氧化碳
①制取原理--浓硫酸对有机物的脱水作用
②制取方程式--HCOOHCO↑+H2O
③装置--分液漏斗,圆底烧瓶
④检验--燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊
⑤除杂质--通入浓硫酸(除水蒸气)
⑥收集--排水法
⑿甲烷
①制取方程式--CH3COONa+NaOH CH4↑+Na2CO3
②装置--略微向下倾斜的大试管,加热
③收集--排水法或向下排空气法
⒀乙烯
①制取原理--浓硫酸对有机物的脱水作用
②制取方程式--CH3CH2OH CH2=CH2↑+H2O
③装置--分液漏斗,圆底烧瓶,加热
④除杂质--通入NaOH溶液(除SO2,CO2),通入浓硫酸(除水蒸气)
收集--排水法
⒁乙炔
①制取原理--电石强烈吸水作用
②制取方程式--CaC2+2H2OCa(OH)2+CH CH↑
③装置--分液漏斗,圆底烧瓶(或用大试管,锥形瓶)
④检验--无色气体,能燃烧,产生明亮的火焰,并冒出浓的黑烟
⑤除杂质--通入硫酸铜溶液(除H2S,PH3),通入浓硫酸(除水蒸气)
收集--排水法或向下排气法
一些快速制法(即无需加热)
20. HI
(1)将等检气体通入AgNO3溶液中,如果出现黄色的沉淀,则证明待检气体是HI。
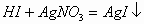 (黄色)
(黄色)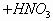
(2)另两种方法同HCl的(1)、(3)。
实验专题
洗涤仪器
19. HBr
(1)将待检气体通入AgNO3溶液中,如果出现浅黄色的沉淀,则证明待检气体是HBr。
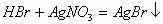 (浅黄色)
(浅黄色)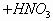
(2)另两种方法同HCl的(1)、(3)。
18. HCl
(1)打开待检气体瓶盖,有白雾产生,则待检气体为HCl。(注:当其他几种HX同时存在时,此法则不适用。)
(2)将待检气体通入AgNO3溶液中,如果出现白色的沉淀,则证明待检气体是HCl。
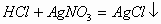 (白色)
(白色)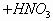
(3)用润湿的蓝色石蕊试纸靠近待检气体,如果蓝色石蕊试纸变红,则证明待检气体是HCl。(注:当有其他几种酸性气体同时存在时,此法则不适用。)
17.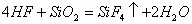 HF
HF
将待检气体通入水中,配成溶液,用配制的溶液在玻璃上刻字,如果能刻上字,则证明待检气体为H。
16. I2(蒸气)
(1)观察待检气体的颜色,如果呈紫色,则待检气体是I2(蒸气)。
(2)将待检气体冷却,有紫黑色固体产生,则待检气体是I2(蒸气)。
(3)将待检气体通入淀粉溶液,溶液呈蓝色,则待检气体是I2(蒸气)。
15. Br2(蒸气)
(1)观察待检气体的颜色,如果呈红棕色,并将此气体通入水中,如果此气体水溶液的颜色呈黄色,则证明待检气体是Br2(蒸气)。
(2)将待检气体用冰水冷却,如果转化为红棕色的液体,则待检气体为Br2(蒸气)。
(3)将待检的红棕色气体通入AgNO3溶液中,如果出现浅黄色的沉淀,则证明待检气体是Br2(蒸气)。
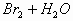
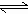
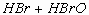
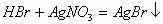 (浅黄色)
(浅黄色)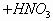
14. Cl2
(1)观察待检气体的颜色,如果呈黄绿色,则证明待检气体是Cl2。
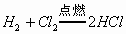 (2)将H2点燃并伸入待检气体中,如果氢气继续燃烧,并产生苍白色火焰,同时,在瓶口附近有白雾产生,则证明待检气体为Cl2。
(2)将H2点燃并伸入待检气体中,如果氢气继续燃烧,并产生苍白色火焰,同时,在瓶口附近有白雾产生,则证明待检气体为Cl2。
 (3)将润湿的KI淀粉试纸靠近盛待检气体的瓶口,如果KI淀粉试纸变蓝,则证明待检气体为Cl2。(注:当有几种氧化性气体同时存在时,此法则不适用。)
(3)将润湿的KI淀粉试纸靠近盛待检气体的瓶口,如果KI淀粉试纸变蓝,则证明待检气体为Cl2。(注:当有几种氧化性气体同时存在时,此法则不适用。)
13. SO2
将待检气体通入品红溶液中,如果品红溶液褪色,且受热后又恢复原色,则证明待检气体是SO2。
12. H2S
(1)闻待检气体的气味,如果有臭鸡蛋气味,则证明待检气体为H2S。
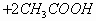
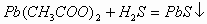 (2)用润湿的
(2)用润湿的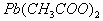 试纸靠近盛待检气体的瓶口,如果
试纸靠近盛待检气体的瓶口,如果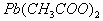 试纸变成黑色,则证明待检气体是H2S。
(黑色)
试纸变成黑色,则证明待检气体是H2S。
(黑色)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com