
3.地域文化对人口的影响是通过影响人们的生育意愿而表现出来的。下列叙述正确的是 ( )
A.“男孩偏好”的传统与“稻米文化”密切相关
B.中国的儒家文化有“男性偏好”的传统思想,但重视子女的质量和注重自我发展
C.发达国家受基督教的影响,没有性别偏好
D.“重男轻女指数”反映发展中国家普遍渴望生育男孩
2.人口生育意愿与中国文化传统相似的国家是 ( )
A.韩国、泰国、菲律宾 B.菲律宾、泰国、尼泊尔
C.巴基斯坦、尼泊尔、韩国 D.哥伦比亚、肯尼亚、委内瑞拉
1.从图中可以看出,这个地区人口变化趋势的特征有( )
A.青壮年劳动力充足
B.人口老龄化显著
C.自然增长率上升
D.人口出生率较高
重男轻女指数是指希望生育男孩的母亲人数与希望生育女孩的母亲人数的比例,下表是联合国人口机构2006年公布的部分国家“重男轻女指数”。分析回答完成2-3题。
|
国家 |
巴基 斯坦 |
尼泊 尔 |
韩国 |
泰国 |
肯尼 亚 |
哥伦 比亚 |
菲律 宾 |
委内 瑞拉 |
|
指数 |
4.9 |
4.0 |
3.3 |
1.4 |
1.1 |
1.0 |
0.9 |
0.9 |
29.(16分)硝酸是一种重要的化工原料,工业上生产硝酸的主要过程如下:
(1)以N2和H2为原料合成氨气。反应N2(g)+3H2(g)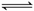 2NH3(g);△H<0
2NH3(g);△H<0
①下列措施可以提高H2的转化率是(填选项序号) 。
a.选择适当的催化剂 b.增大压强 c.及时分离生成的NH3 d.升高温度
②一定温度下,在密闭容器中充入1 mol N2和3 mol H2发生反应。若容器容积恒定,达到平衡状态时,气体的总物质的量是原来的,则N2的转化率a1= ;
若容器压强恒定,达到平衡状态时,N2的转化率为a2,则a2____a1(填“>”、“<”或“=”)。
(2)以氨气、空气为主要原料制硝酸。
①NH3被氧气催化氧化生成NO的反应的化学方程式是 。
②在容积恒定的密闭容器中进行反应2NO(g)+O2(g)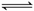 2NO2(g);△H>0
2NO2(g);△H>0
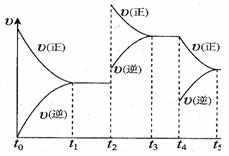
该反应的反应速率(v)随时间(t)变化的关系如右图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号) 。
a.在t1~t2时,可依据容器内气体的压强保持不变判断反应
已达到平衡状态
 b.在t2时,采取的措施可以是升高温度
b.在t2时,采取的措施可以是升高温度
c.在t3-t4时,可依据容器内气体的密度保持不变判 断反应已达到平衡状态
d.在t5时,容器内NO2的体积分数是整个过程中的最大值
(3)硝酸厂常用如下两种方法处理尾气。
①催化还原法:催化剂存在时用H2将NO2还原为N2。
已知:2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ/mol
N2(g)+2O2(g)=2NO2(g);△H =+67.7 kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是 。
②碱液吸收法:用Na2CO3溶液吸收NO2生成CO2。
若每9.2 g NO2和Na2CO3溶液反应时转移电子数为0.1 mol,则反应的离子方程是 。
28.(16分)A、B、C、D、E 5种短周期主族元素分占三个周期,A、B、C为同一周期依次相邻的3种元素,A和C的原子序数之比为3:4,E原子的电子层数等于最外层电子数,D的原子序数小于E。用化学用语回答相关问题:
(1)A元素在周期表中的位置 。
(2)比较C和E简单离子半径大小: 。
(3)元素E的一种常见的可溶性盐溶液呈碱性,其原因是(用离子方程式表示):
;
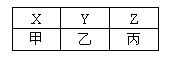 (4)X、Y、Z、甲、乙、丙是由A、B、C分别与D形成
(4)X、Y、Z、甲、乙、丙是由A、B、C分别与D形成
的化合物,六种化合物可以排成下表,其中同一横行的分
子中电子数相同,同一纵行的物质所含元素种类相同,其
中X、Y、甲常温常压下为气体, Z、乙、丙常温常压下为液体。
①甲的分子式为 ,丙的电子式为 。
②乙和丙常作火箭推进器的燃料,反应后的产物无污染。已知8g液态乙与足量液态丙完全反应,产物均为气体时放出热量为160.35 kJ,试写出 该反应的热化学方程式: 。
(5)2007年7月2日,美、德两国科学家成功合成了具有独特化学特性的E2D6化合物,写出它在C2中完全燃烧的化学方程式: 。
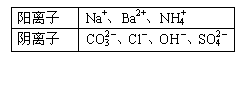
27.(14分)有A、B、C、D四种强电解质,它们
在水中电离可产生表中离子(每种物质只含一种
阴离子且互不重复)。已知:①A、C液体的pH
均大于7, A、B的溶液中水的电离程度比纯水大;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象。
填写下列空白:
(1)A是 ,B是 ,C是 ,D是 。
(2)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为 。
(3)常温下,0.15 mol•L-1 C溶液与0.20 mol•L-1 盐酸混合,所得混合液的pH=13,则C溶液与盐酸的体积比是 。
26.(14分)H2O2是在医疗、化工方面应用广泛的化学试剂。
(1)Na2O2、CaO2以及BaO2都可与酸作用生成过氧化氢,实验室通过上述某种过氧化物与适量稀硫酸作用,过滤后即可制得较纯净的H2O2溶液,则应选择的过氧化物是_______________;
(2)实验室可用H2O2与次氯酸钠反应制氧气, 其中还原剂是__________,生成0.5 mol氧气,转移电子____________mol,其反应的化学方程式为____________________________________;
(3)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量,有两位同学分别用以下化学方程式表示其中的反应原理:
①5H2O2+2KMnO4+3H2SO4→2MnSO4+K2SO4+5O2↑+8H2O
②3H2O2+2KMnO4+3H2SO4→2MnSO4+K2SO4+4O2↑+6H2O
 你认为其中错误的是_______(认为没有可以不填),简述理由________________________。
你认为其中错误的是_______(认为没有可以不填),简述理由________________________。
13.有关①100 mL 0.1 mol/L NaHCO3 ②100 mL 0.1 mol/L Na2CO3两种溶液的叙述不正确的是( )
A.溶液中水电离出的H+个数:②>① B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中: c(CO2-3 )>c(H2CO3) D.②溶液中: c(HCO-3)>c(H2CO3)
第Ⅱ卷(非选择题)
12.已知,Fe2+结合S2-的能力大于结合OH-的能力,而Al3+则正好相反。在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是( )
A.Al2S3、FeS和S B.Fe(OH)3和Al(OH)3
C.Fe2S3和 Al(OH)3 D. FeS、Al(OH)3和S
11.比较氯元素和硫元素的非金属性的相对强弱,下列方案中不能达到目的的是( )
A.加热条件下,氯气和硫分别与铜反应,比较生成物中铜的化合价
B.比较氯化氢和硫化氢的热稳定性
C.往H2S溶液中通入氯气
D.分别测定0.1 mol/L氯化钠溶液和0.1 mol/L硫化钠溶液的pH
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com