
15.Д№АИЃКD
НтЮіЃКAЁЂBбЁЯювђЪЧИЩдяЕФЙЪHClЁЂCl2ЖМВЛзїгУЃЛCЯюСНепЖМЩњГЩАзЩЋГСЕэЁЃЖјDЯюHClЮоБфЛЏЃЌCl2ПЩЪЙЦфБфРЖЁЃ
14.Д№АИЃКA
НтЮіЃКШєНЋKOHШмвКЕЮМгЕНAl2(SO4)3ШмвКжаЃЌБпЕЮБпеёЕДЃЌЫљЗЂЩњЕФЯжЯѓЪЧГСЕэЃЌШЛКѓШмНтЃЌзюКѓГСЕэЯћЪЇЁЃШєНЋAl2(SO4)3ШмвКЕЮМгЕНKOHШмвКжаЃЌБпЕЮБпеёЕДЃЌЫљЗЂЩњЕФЯжЯѓЪЧЃЌЦ№ЪМЮоГСЕэВњЩњЃЌШЛКѓГСЕэСПж№НЅдіЖрЃЌМЬајЕЮМгГСЕэВЛдйдіЖрЃЌвВВЛЛсЯћЪЇЁЃгаЙиРызгЗНГЬЪНЮЊЃКAl3++4OHЃ===AlO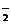 +2H2O,Al3++3AlO
+2H2O,Al3++3AlO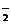 +6H2O===4Al(OH)3Ё§ЁЃ
+6H2O===4Al(OH)3Ё§ЁЃ
13.Д№АИЃКCD
НтЮіЃКЖдИїзщШмвКЃЌЗжБ№ВЩгУСНСНЛьКЯЗЈНјааЧјЗжЁЃбЁЯюCжаKHCO3МгШыNaAlO2ВњЩњАзЩЋГСЕэЃЌHCO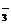 +AlO+H2O===CO
+AlO+H2O===CO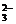 +Al(OH)3Ё§ЃЌМгШыNaHSO4ШмвКжаВњЩњЮоЩЋЦјЬхЃЌДгЖјМгвдЧјЗжЃЛбЁЯюDжаЪзЯШЙлВьГіFeCl3ШмвКЃЌШЛКѓРћгУFeCl3ШмвКМјБ№ГіNaOHШмвКЃЌдйгУNaOHШмвКМјБ№ГіMgCl2ШмвКЁЃ
+Al(OH)3Ё§ЃЌМгШыNaHSO4ШмвКжаВњЩњЮоЩЋЦјЬхЃЌДгЖјМгвдЧјЗжЃЛбЁЯюDжаЪзЯШЙлВьГіFeCl3ШмвКЃЌШЛКѓРћгУFeCl3ШмвКМјБ№ГіNaOHШмвКЃЌдйгУNaOHШмвКМјБ№ГіMgCl2ШмвКЁЃ
12.Д№АИЃКA
НтЮіЃКбЁЯюAЪЧРћгУШ§жжгаЛњЮяЕФШмНтадКЭУмЖШДѓаЁМгвдЧјЗжЃЌБНФбШмгкЫЎБШЫЎЧсЃЌввЫсФмШмгкЫЎЃЌЫФТШЛЏЬМФбШмгкЫЎЕЋБШЫЎжиЁЃбЁЯюBжаввДМЁЂввШЉЁЂввЫсОљФмШмгкЫЎЃЌФбвдЧјЗжЃЛбЁЯюCжаввШЉЁЂввЖўДМКЭбЁЯюDжаввДМЁЂИЪгЭНдФмШмгкЫЎЃЌЮоЗЈЧјЗжЁЃ
11.Д№АИЃКB
НтЮіЃКвЛжжбЮШмвКОЋжЦЕФЙ§ГЬЃЌВЛПЩФмгУН№ЪєФЦЃЛУЂЯѕЕФЛЏбЇЪНЪЧNa2SO4ЁЄ10H2OЃЌВЛФмМгШШЭбШЅНсОЇЫЎЁЃгЩДЫПЩМћЃЌЗВЪЧЩцМАЕНЂкЁЂЂнСНИіВйзїВНжшЕФбЁЯюЖМЪЧВЛе§ШЗЕФбЁЯюЁЃ
10.Д№АИЃКB
НтЮіЃКгЩЬтИјЗДгІЃЌвЊжЄУїгаIO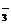 ЃЌгІгУЕНIЃЁЂЕэЗлКЭЫсЁЃЯжИјГіСЫKIЕэЗлЪджНЃЌАќРЈЧАСНжжЪдМСЃЌЫљвддйбЁгУЪГДз(МДЫс)БуПЩЭъГЩЩЯЪіМьбщЁЃЯђД§ВтвКжаМгШыДзЫсЃЌШЛКѓНЋШмвКЕЮдкKIЕэЗлЪджНЩЯЃЌШєЪджНБфРЖЃЌМДжЄУїгаIO
ЃЌгІгУЕНIЃЁЂЕэЗлКЭЫсЁЃЯжИјГіСЫKIЕэЗлЪджНЃЌАќРЈЧАСНжжЪдМСЃЌЫљвддйбЁгУЪГДз(МДЫс)БуПЩЭъГЩЩЯЪіМьбщЁЃЯђД§ВтвКжаМгШыДзЫсЃЌШЛКѓНЋШмвКЕЮдкKIЕэЗлЪджНЩЯЃЌШєЪджНБфРЖЃЌМДжЄУїгаIO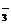 ЁЃ
ЁЃ
9.Д№АИЃКBD
НтЮіЃКИљОнЕЮМгЕФЫГађВЛЭЌЃЌВњЩњЕФЯжЯѓВЛЭЌМгвдЧјБ№ЁЃBжаШєНЋЯЁH2SO4ЕЮШыNa2CO3ШмвКжаЃЌВњЩњHCO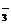 ,ЮоУїЯдЯжЯѓЃЛШєНЋNa2CO3ШмвКЕЮШыЯЁH2SO4жаЃЌдђгаCO2ВњЩњЁЃDжаNaAlO2ШмвКЕЮШыбЮЫсжаЃЌЮоГСЕэВњЩњЃЛЖјНЋбЮЫсЕЮШыNaAlO2ШмвКжаЃЌдђгаAl(OH)3ГСЕэВњЩњЁЃ
,ЮоУїЯдЯжЯѓЃЛШєНЋNa2CO3ШмвКЕЮШыЯЁH2SO4жаЃЌдђгаCO2ВњЩњЁЃDжаNaAlO2ШмвКЕЮШыбЮЫсжаЃЌЮоГСЕэВњЩњЃЛЖјНЋбЮЫсЕЮШыNaAlO2ШмвКжаЃЌдђгаAl(OH)3ГСЕэВњЩњЁЃ
8.Д№АИЃКC
НтЮіЃКбЁЯюAПЩРћгУЦфдкЫЎжаШмНтадКЭУмЖШЕФДѓаЁРДЧјЗжЃЛбЁЯюBКЭбЁЯюDПЩРћгУЦфдкЫЎжаЕФШмНтадМгвдЧјЗжЁЃ
7.Д№АИЃКBD
НтЮіЃКбЁЯюBжаЕФСђЫсТСКЭЧтбѕЛЏФЦСНжжШмвКЗДгІПЩЩњГЩАзЩЋГСЕэЃЌДЫГСЕэЗжБ№гыСђЫсЁЂЙ§СПЧтбѕЛЏФЦШмвКЗДгІЛсЯћЪЇЃЌЖјЧвЃЌНЋСђЫсТСгыЧтбѕЛЏФЦЛьКЯЪБЃЌШчЙћНЋЧАепЕЮШыКѓепЃЌгЩгкЧтбѕЛЏФЦЙ§СПЃЌдђЩњГЩЕФГСЕэЛсКмПьШмНтЃЌЫцзХЕЮШыЕФСђЫсТСж№НЅдіМгЃЌГСЕэШмНтЕФЫйТЪж№НЅБфТ§жБЕНВЛШмЁЃЗДжЎЃЌШєНЋЧтбѕЛЏФЦЕЮШыСђЫсТСжа,дђЩњГЩЕФГСЕэж№НЅдіЖрЃЌжБжСзюИпЯоСПГСЕэгжж№НЅШмНтЁЃетбљЃЌНЋВЛФбЧјБ№ЧтбѕЛЏФЦКЭСђЫсТССНжжШмвКЁЃНЋСђЫсКЭТШЛЏФЦСНжжШмвКЗжБ№ЕЮШыЧтбѕЛЏТСжаЃЌДгЖјПЩЪЙЧтбѕЛЏТСШмНтМДФмДгжаЧјБ№ГіСђЫсЃЌПЩМћЃЌбЁЯюBDЮЊБОЬтД№АИЁЃ
6.Д№АИЃКB
НтЮіЃКНтДЫЬтЕФЙиМќЪЧХЊЧхОЋжЦфхБНЕФзюКѓСНВНЃЌгУЫЎЯДЃЌдђашИЩдяМСИЩдяЃЌЗжРыГіИЩдяМСдђжЛФмгУеєСѓЕФЗНЗЈЃЌЫљвдзюКѓСНВНгІЮЊЂлЂйЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com