
2、由于固体浓度为一常数,所以在平衡常数表达式中不再写出。
1、化学平衡常数K表示可逆反应进行的程度。
(1)化学平衡常数K只针对达到平衡状态的可逆反应适用,非平衡状态不适用。
(2)化学平衡常数K的表达式与可逆反应的方程式书写形式有关。对于同一可逆反应,正反应的平衡常数等于逆反应的平衡常数的倒数,即:K正=1/K逆。
(3)K值越大,表示反应进行的程度越大,反应物转化率或产率也越大。
(4)K值不随浓度或压强的改变而改变,但随着温度的改变而改变。
(5)一般情况下, 对于正反应是吸热反应的可逆反应,升高温度,K值增大;而对于正反应为放热反应的可逆反应,升高温度,K值减少。
对于正反应是吸热反应的可逆反应,升高温度,K值增大;而对于正反应为放热反应的可逆反应,升高温度,K值减少。
在一定温度下,可逆反应无论从正反应开始还是从逆反应开始,无论反应混合物的起始浓度是多少,当反应达到平衡状态时,正反应速率等于逆反应速率,反应混合物中各组成成分的含量保持不变,即各物质的浓度保持不变。生成物浓度的幂次方乘积与反应物浓度的幂次方乘积之比是常数,这个常数叫化学平衡常数,用K表示。
化学平衡常数的计算公式为:
对于可逆反应:mA(g) + nB(g) pC(g) + qD(g)
pC(g) + qD(g)
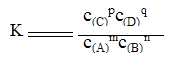
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com