
11.可逆反应:2NO2(g) 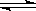 2NO(g) + O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是
2NO(g) + O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是
① 单位时间内生成n mol O2的同时生成2 n mol NO2
② 单位时间内生成n mol O2的同时生成2 n mol NO
③ 用NO2、NO、O2表示的反应速率数值之比为2∶2∶1的状态
④ 混合气体的颜色不再改变的状态
⑤ 混合气体的密度不再改变的状态
A.①④ B.②③⑤ C.①③④ D.①②③④⑤
10.根据下表中的数据,结合学过的化学知识,判断下列说法正确的是
|
物质 |
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
|
沸点/℃ |
1465 |
1412 |
181(升华) |
57.6 |
A.以上四种物质中,只有SiCl4是共价化合物
B.若上述数据变化规律具有普遍性,则可预测:LiCl 的沸点大于BCl3的沸点
C.因为AlCl3的沸点低,所以工业上可用电解熔融AlCl3制备Al
D.据上述数据,可判断NaCl、MgCl2为分子晶体
9.下列说法中不正确的是
A.共价化合物中一定不含有离子键,离子化合物中可能含有共价键
B.一定条件下1 mol N2与3 mol H2在密闭容器中充分反应可生成2 mol NH3
C.铁质器件附有铜质配件,在接触处易生铁锈
D.HClO4、H2SO4、H3PO4的酸性依次增强
8.同周期的X、Y、Z三种元素,已知其最高价氧化物对应水合物的酸性强弱顺序是:HXO4>H2YO4>H3ZO4,则下列各判断中正确的是
A.原子半径:X>Y>Z B.非金属性:X>Y>Z
C.气态氢化物稳定性:X<Y<Z D.原子序数:X<Y<Z
7.已知在550℃时,一定容积的容器中发生反应:2SO2+O2
 2SO3(正反应放热),判断该反应达到平衡状态的标志是
2SO3(正反应放热),判断该反应达到平衡状态的标志是
A.SO2和SO3浓度相等 B.SO3的生成速率与SO2的消耗速率相等
C.容器中气体的压强不变 D.容器中混合气体的密度保持不变
6.下列各图中,表示正反应是吸热反应过程的能量变化图是
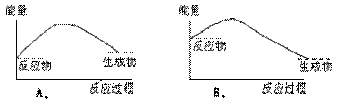
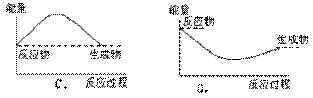
5.已知4NH3+5O2===4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是
A.4v(NH3)=5v(O2) B.5v(O2)=6v(H2O)
C.2v(NH3)=3v(H2O) D.4v(O2)=5v(NO)
4.下列几种元素中,非金属性最强的是
A.原子结构示意图: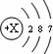 B.原子的电子式:
B.原子的电子式: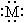
C.第二周期ⅦA族的元素 D.第三周期ⅠA族的元素
3.从化学学科的角度分析,下列叙述不正确的是
A.绿色植物光合作用过程中是由太阳能转变成化学能
B.研制乙醇汽油技术,可降低机动车辆尾气中有害气体的排放
C.煤、石油、天然气属于可再生能源
D.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
2.决定化学反应速率的主要因素是
A.参加反应的物质本身的性质 B.催化剂
C.温度、压强以及反应物的接触面 D.反应物的浓度
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com