
3.知道功是能量转化的量度。
2.知道做功的过程就是物体能量的转化过程。
1.知道在能量相互转化过程中,转化了的能量的多少,可以由做功的多少来确定。
4.25 =3/1
C4H10 6.5 0.75 ,所以乙烷的百分含量为3/4×100%=75%。
答案:75%
总之,烃燃烧规律的灵活应用还有很多地方,需要在学习中逐渐体会与感悟。
3、推断混合物的成分或含量
例4.丙稀和某气态烃组成的混合气体,完全燃烧时所需O2的体积是混合气体的5倍(同温同压下),则另一种气体是 ( )
A.C4H8 B. C3H4 C. C2H6 D. C2H4
解析:根据烃燃烧规律可知1mol烃的耗氧量等于(n+m/4)mol,故丙稀为4.5mol、C4H8为6mol,C3H4 为4mol,C2H6为3.5mol,C2H4为3mol。由题意得1mol混合气体完全燃烧所需的氧气平均为5mol,所以根据平均值原理知另一种组分的耗氧量应大于5mol。
答案:A
例5.相同状况下,1.12升乙烷和丁烷的混合物完全燃烧需氧气4.76升,求混合气体中乙烷的百分含量。
解析:由题意知1L混合物完全燃烧耗氧量为4.76L/1.12=4.25L,而1L乙烷、丁烷的耗氧量分别为3.5L和6.5L,则:
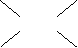 C2H6 3.5
2.25
C2H6 3.5
2.25
2、推断烃的分子式
例2.充分燃烧某液态芳香烃X,并收集产生的全部水,恢复到室温时得到水的质量跟原芳香烃X的质量相等。则X的分子式是( )
A.C10H14 B.C11H16 C.C12H18 D. C13H20
解析:由燃烧通式CnHm + (n + m/4)O2 → nCO2 + m/2 H2O 及“得到水的质量跟原芳香烃X的质量相等”可知芳香烃中碳的质量与水中氧的质量与相等,故芳香烃中碳与氢的质量比恰好是水中氧与氢的质量比。
答案:C。
例3.常温下,10mL某种气态烃在50mL氧气里充分燃烧,得到液态水和体积为35mL的混合气体(所有气体体积都是在同温同压下测定的),则该气态烃可能是( )
A.甲烷 B.乙烷 C.丁炔 D.丙烯
解析:本题在考查烃燃烧规律的同时,还涉及过量判断的问题。根据“液态水和体积为35mL的混合气体”可知O2有剩余。故
CnHm + (n + m/4)O2 → nCO2 + m/2 H2O △V
1 n + m/4 n (1+ m/4)
10mL (60-35)mL=25mL
解得:m=6;而n是任意实数,即分子中有6个H原子的气态烃就满足条件。C2H6、C3H6和C4H6分子中均含有6个H原子,又因10mLC4H6完全燃烧时至少需要55mL氧气,故C4H6不符题意。
答案:B、D。
1、判断耗氧量及水或二氧化碳的生成多少问题
例1、下列各组物质中各有两组份,两组份各取1摩尔,在足量氧气中燃烧,两者耗氧量不相同的是( )
A .乙烯和乙醇 B .乙炔和乙醛 C .乙烷和乙酸甲酯 D .乙醇和乙酸
解析:本题是烃燃烧规律的灵活运用问题。CH3CH2OH(乙醇)可改写成C2H4·H2O,故它和C2H4的耗氧量相等;CH3CHO(乙醛)可改写成C2H2·H2O,故它和C2H2的耗氧量相等;CH3COOCH3(乙酸甲酯)可改写成C2H6·CO2,故它和C2H6的耗氧量相等。CH3COOH(乙酸)可改写成CH4·CO2或C2·2H2O。
答案:D。
根据烃燃烧的化学方程式CnHm + (n + m/4)O2 → nCO2 + m/2 H2O可知有如下规律:①等物质的量的烃完全燃烧时,耗氧量的多少决定于n的值,n的值越大,耗氧量越多。
②等质量的烃完全燃烧时,耗氧量的多少决定于氢的质量分数,即m/n 的值,m/n越大,耗氧量越多。
③最简式相同的烃无论以何种比例混合,都有混合物中碳氢元素的质量比和质量分数都不变;一定质量的混合烃完全燃烧时消耗O2的质量不变,生成的CO2和H2O的质量不变。
④对气态烃完全燃烧时,若温度低于100℃则反应后的气体体积一定减少为(1+m/4),若温度高于100℃时,则存在:m=4时,完全燃烧前后气体的体积不变;m<4时,完全燃烧后气体的体积减少;m>4时,完全燃烧后气体的体积增大。
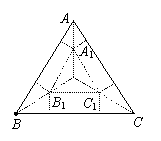
2.解:设O为△ABC的中心,连结OA、OB、OC,并设OA、OB、OC的中点分别为A1、B1、C1,过A1、B1、C1分别向三边作垂线,则所得三个矩形即为三个侧面,三个角上的小四边形拼在一起即为上底面
[变式] △ABC若为一般三角形,又如何拼接?(取O为三角形的内心,其余同)
2. 边长为a的正三角形,要拼接成一个正三棱柱且不剩料,应如何设计?(在图中用虚线画出)

解:1.C.提示:设内切球半径为r,截面AEF的面积为S,由VA-BEFD=VA-CEF得
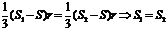
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com