
31.(14分,每空2分)
OH- Cl- K+ 铁粉 Ag(或银) Ag+、Fe3+、Cl-、OH- KNO3
30.(16分)(1)Ar、K、F、Br、M(每空1分)
(2)H2O HCl PH3 (3分)、PH3(2分)
(3)Al(OH)3+OH-=AlO2-+2H2O(3分) Al(OH)3+3H+=Al3++3H2O(3分)
29.(16分,除注明外,每空2分)
(1)A和C C 淀粉酶在40℃时活性相对较高,淀粉酶
催化淀粉水解产生的还原糖多 E 酶失活
(2)剩余的淀粉遇碘变蓝
(3)在20℃和100℃之间(1分)每隔一定温度设置一个实验组(1分),其他实验条件保持一致(1分)。以反应液和上述试剂(或答碘液或答班氏试剂或答斐林试剂)发生颜色反应的程度为指标确定最适温度(1分)。
化学题部分
28. (18分)
实验一:光照强度(2分) CO2浓度(2分) 激素调节(1分) 生长素(1分) 减慢(1分)
实验二:由叶绿体基质向类囊体片层(2分) 减少 (2分) B、D (2分)
|
叶片编号 |
MB |
MA |
|
1 |
|
|
|
2 |
|
|
|
3 |
|
|
|
平均值 |
|
|
实验三:(1)(3分)
(2)B叶片被截取部分在6小时内光合作用
合成的有机物总量(2分)
27.(16分,除注明外,每空1分)
(1)蛋白质 [⑥]线粒体(2分) 主动运输
(2)[⑦]高尔基体(2分) 水解酶 ②④⑤⑥⑦⑨(共2分,漏答1个扣1分;错答1个即得0分) 酶 (3)B 2 [③]中心体(2分) (4)抑癌基因 糖蛋白
26.(14分)(1)[14]液泡 [13]核糖体 (2)[4]叶绿体 [11]线粒体
(3)①③④ 太阳能 (4)③
36.(18分)如图,某货场需将质量为m1=100 kg的货物(可视为质点)从高处运送至地面,
为避免货物与地面发生撞击,现利用固定于地面的光滑四分之一圆轨道,使货物由轨道顶
端无初速滑下,轨道半径R=1.8 m。地面上紧靠轨道依次排放两个完全相同的木板A、B,
长度均为l=2.0m,质量均为m2=100 kg,木板上表面与轨道末端相切。货物与木板间的动
 摩擦因数为
摩擦因数为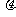 1,木板与地面间的动摩擦因数
1,木板与地面间的动摩擦因数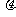 =0.20。
=0.20。
(最大静摩擦力与滑动摩擦力大小相等,取g=10 m/s2)
求:(1)求货物到达圆轨道末端时受轨道的支持的大小。
(2)若货物滑上木板A时,木板不动;而滑上木板B时,木板B开始滑动,求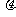 1应满足的条件。
1应满足的条件。
(3)若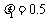 ,求货物滑到木板A末端时的速度和在木板B上运动的时间。
,求货物滑到木板A末端时的速度和在木板B上运动的时间。
2010-2011学年第一学期高三期中考试
理综答案
选择题部分
生物题部分
35.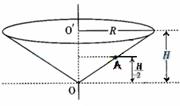 (18分)如图,竖直放置的圆锥筒可绕其中心OO′转动,筒内壁粗糙,筒口半径和筒高分
(18分)如图,竖直放置的圆锥筒可绕其中心OO′转动,筒内壁粗糙,筒口半径和筒高分
别为R和H,A点的高度为筒高的一半。内壁上有一质量为m的小物块。求:(1)当筒不
转动时,物块静止在筒壁A点受到的摩擦力和支持力的
大小;(2)当物块在A点随筒做匀速转动,且其受到的摩
擦力为零时,筒转动的角速度。
34.(1)①在验证力的平行四边形定则的实验中,橡皮绳的一端固定在木板上,用两个测力计把橡皮绳另一端拉到一个确定的点O。下面步骤中错误的是( )
A.实验中测力计必须与木板平行并紧贴木板 B.读数时视线要正对测力计的刻度
C.实验中用两弹簧秤同时拉橡皮条时,两弹簧秤之间的夹角不得大于90°
D.实验时先用一把弹簧秤拉橡皮绳并使读数达到最大,再用另一把弹簧秤拉橡皮绳使它的另一端与O点重合。
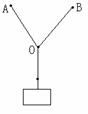 ② 某同学尝试验证平行四边形定则,他找到三条相同的橡皮筋(遵循胡克定律)和若干小重物,及刻度尺、三角板、铅笔、细绳、白纸、钉子,设计了如下实验:将两条橡皮筋的一端分别挂在墙上的两个钉子A、B上,另一端与第三条橡皮筋连接,结点为O,将第三条橡皮筋的另一端通过细绳挂一重物。
② 某同学尝试验证平行四边形定则,他找到三条相同的橡皮筋(遵循胡克定律)和若干小重物,及刻度尺、三角板、铅笔、细绳、白纸、钉子,设计了如下实验:将两条橡皮筋的一端分别挂在墙上的两个钉子A、B上,另一端与第三条橡皮筋连接,结点为O,将第三条橡皮筋的另一端通过细绳挂一重物。
Ⅰ.为完成实验,下述操作中必需的是 ( )
A. 测量橡皮筋的原长
B. 测量细绳的长度
C. 测量悬挂重物后橡皮筋的长度
D. 记录悬挂重物后结点O的位置
Ⅱ.本实验中所采用的科学研究方法是( )
A.等效替代法 B.极值法 C.控制变量法 D.放大法
 (2) 如图,小车拖着纸带从斜面上滑下,重力加速度为g。下图是打出的纸带的一段。
(2) 如图,小车拖着纸带从斜面上滑下,重力加速度为g。下图是打出的纸带的一段。
①已知交流电频率为50Hz,由纸带的数据求出小车的加速度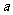 =_____ 。
=_____ 。
②为了求出小车在下滑过程中所受的阻力,还需测量的物理量有_____ ______
。用测得的量及加速度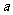 表示阻力大小的计算式为f =_________。
表示阻力大小的计算式为f =_________。
33. (13分)(1)合成氨工业对化学工业和国防工业具有重要意义。工业
(13分)(1)合成氨工业对化学工业和国防工业具有重要意义。工业
合成氨生产示意图如图。 ①X的化学式为 ;
②图中条件选定的主要原因是(选填字母序号) ;
A.温度、压强对化学平衡影响
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
(2)合成氨工厂常通过测定反应前后混合气体的密度来确定氮的转化率。某
工厂测得合成塔中N2、H2的投料比(体积比)为2:3,从合成塔中出来的混合气体在相同条件下密度为0.693g/L(标准状况)。求该合成氨厂N2的转化率并写出解题过程。
(3)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成A和B两种物质。A为铵盐,
B在标准状况下为气态。在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;
若每反应8.96L氨气(标准状况),同时生成0.3molA。
①写出氨气和氟气反应的化学方程式 ;
②在标准状况下,每生成1 mol B,转移电子的物质的量为 mol。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com