
某CaCO3样品含一种杂质,与足量稀盐酸反应,如生成的CO2的质量与所用样品质量之间关系如下图,则该样品中可能含有的杂质是
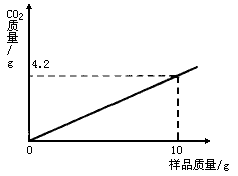
[ ]
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
| 猜 想 | 实验设计 | 现 象 | 判 断 | |
| 猜想a | 样品含碳酸盐 | 取少量样品,滴加盐酸 | 无气泡放出 | |
| 猜想b | 样品中含有Na2CO3,且还含有CaO、Ca(OH)2、CaCO3中的一种 | (1) (2) |
(1); (2)有气泡放出 |
猜想b成立 |

查看答案和解析>>
科目:初中化学 来源: 题型:
| 100 |
| x |
| 73 |
| 100g×10.95% |
| 100 |
| x |
| 73 |
| 100g×10.95% |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 相关的质量 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 所加入稀盐酸的质量(g) | 50 | 50 | 50 | 50 | 50 |
| 烧杯中剩余的质量(g) | 72.8 | 120.6 | 168.4 | 216.2 | 266.2 |
| 100 |
| x |
| 44 |
| 8.8g |
| 100 |
| x |
| 44 |
| 8.8g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com