
| ||
| △ |
| 245 |
| x |
| 96 |
| 9.57g |
| 0.5g |
| 15.32g |


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

| 实验现象 | 结论 |
| (1) (2) |
| 实验步骤 | 实验现象 | 结论 |
| 待实验一完成后,将试管中的残余物小心过滤,并将全部滤渣洗涤、干燥、称量,观察是否仍为a g. | 称重氧化铁的质量为ag |
| 实 验 步 骤 | 实 验 现 象 | 结 论 |
| 将实验二的滤渣重新放入试管中,再加入少量过氧化氢溶液,并插入带火星木条,如此反复多次实验,观察现象. | 带火星木条复燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量的熟石灰样品于烧杯中,加适量的水充分溶解后过滤. 向滤液中加入适量的 向滤出固体中加入适量 |
猜想正确 |
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| ①用试管取少量蒸馏水,滴入1-2滴无色酚酞试液,振荡 | 试管内溶液仍为无色 | 水分子不能使无色酚酞试液变红色 |
| ②用试管取少量氯化钠溶液,滴入1-2滴无色酚酞试液,振荡 | ||
| ③用试管取少量氢氧化钠溶液,滴入1-2滴无色酚酞试液,振荡 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
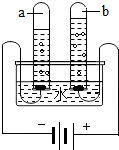 (1)①从微观角度看,水分子由
(1)①从微观角度看,水分子由查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com