
科目: 来源: 题型:
【题目】A、B、C是初中化学中涉及到的不同单质,它们的相对分子A质量依次增大且不超过65,A 与B,B与C均能发生化学反应,B是水电解的生成物之一。请写出:
(1)A与B反应的现象及化学方程式:__________________,__________________。
(2)B与C反应的现象及化学方程式:_______________,___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】右图是康康同学用蒸馏水、10%氢氧化钠溶液、二氧化碳以及软塑料瓶设计的对比实验,用于证明二氧化碳和氢氧化钠发生反应,实验现象是乙瓶变得更瘪。请回答:
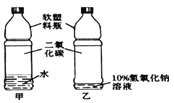
(1)该实验设计不符合对比实验的基本原则,为什么?
(2)设计实验探究反应后乙瓶溶液中溶质的成分。
查看答案和解析>>
科目: 来源: 题型:
【题目】“绿水青山就是金山银山”,生活实际中经常要处理工厂排放的废水,中和反应应用广泛。
(1)某同学将氢氧化钠固体放入盛有稀硫酸的试管中并振荡,试管壁发烫,得出中和反应放热。但该结论不合理,理由是___________ 。
(2)改进实验:将稀硫酸慢慢滴入装有氢氧化钠溶液的烧杯中,烧杯内溶液温度变化如图1:
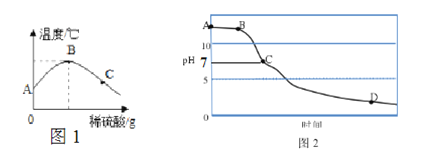
①由图1可知,中和反应是 ______(填“放热”或“吸热”)反应,图1中B点表示的含义是_________。
②用pH传感器测得烧杯中溶液的pH随滴加液体与时间的变化曲线如图2,图中B、C、D所对应溶液中所含溶质硫酸钠的质量大小关系有 ______________。
(3)若一定体积的废水中含有0.01mol氢氧化钠,中和这些碱,需要________mol的硫酸?(例式计算)
(4)而将稀硫酸滴入氢氧化钠溶液中,有气泡产生,可能是氢氧化钠溶液已变质。分析变质的原因_______________________________(用化学方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸是一种常见的化学试剂,工业和农业中使用广泛。
(1)硫酸是由________种元素组成,0.1mol硫酸的质量为_____g,约含_________个硫原子。
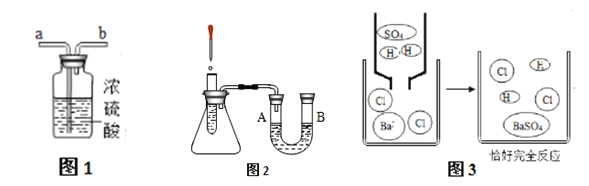
(2)浓硫酸可作干燥剂,若干燥排水法收集的氧气,气体从图1_______端(选“a”或“b”)通入。
(3)图2所示,U型管中是红墨水,向试管中加入浓硫酸,U型管中红墨水液面变化情况是_______。
(4)将氧化铜粉末放入足量稀硫酸中至反应结束,写出发生的化学方程式____________。
(5)将硫酸溶液加入盛有BaCl2溶液的烧杯中,物质变化的微观示意图如图3, 观察到明显的实验现象是 _________。
查看答案和解析>>
科目: 来源: 题型:
【题目】明明同学采用如下图所示装置进行趣味实验(装置气密性良好)。
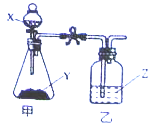
﹙1)若X、Y对应的分别是稀盐酸和碳酸氢钠,Z是紫色石蕊溶液,请简述乙中观察到的实验现象及原因?
(2)若换一组药品,用所得干燥气体填充气球,气球在空气中上升.则X、Y、Z对应的药品是什么?(写出一组即可).
查看答案和解析>>
科目: 来源: 题型:
【题目】在点燃条件下,4.4gC3H8与12.8g氧气恰好完全反应,生成7.2g水、4.4g二氧化碳和a g X。则X的化学式为 ;该反应的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)化学与人类生活、生产息息相关,请回答下列问题:
①家用净水器是利用活性炭的___________性,除去有色有味的杂质;
②炒菜时油锅中的油不慎着火,可以采取的灭火方法是___________________________;
③2017年5月,我国在南海进行了天然气水合物(可燃冰)的试开采,天然气的主要成分是_________
④胃液里含有适量盐酸,服用含氢氧化铝[Al(OH)3]药物可治疗胃酸过多症,反应的化学方程式为______________
(2)根据图文回答下列问题。

① 金刚石的________(填“硬度”或“密度”)大;
② 钠元素是人体必需的________(填“常量”或“微量”)元素;
③ 面包中淀粉属于________(填字母序号);
A. 糖类 B. 蛋白质 C. 油脂
④ 100 g该硫酸溶液中溶质的质量为________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水。某化学课外兴趣小组对生成物中碳的氧化物种类进行了如下实验探究:
【提出问题】 生成物中有哪几种碳的氧化物?
【猜想】
猜想1 | 猜想2 | 猜想3 |
只有CO | 只有________ | 含有CO和CO2 |
【设计实验】 基于猜想3,依据CO和CO2的性质,兴趣小组同学设计了如下实验:
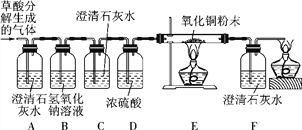
【实验探究】
(1) 观察到________(填序号)装置中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成。
(2) 有两种实验现象都能分别证明草酸分解的气体中含有CO:
① C装置中澄清石灰水不变浑浊,F装置中___________________________;
② E装置中出现_____________________________________的现象。
【实验结论】 通过实验探究证明:猜想3成立。
草酸分解的化学方程式是____________________________________________。
【问题讨论】
(1) B装置的作用是________________________;D装置的作用是__________________。
(2) 装置末端酒精灯的作用是________________________________。
(3)对装置E中玻璃管内的产物成分探究
【查阅资料】
Ⅰ. 一氧化碳还原氧化铜。除生成铜外还可能生成氧化亚铜(Cu2O);
Ⅱ. Cu2O为不溶于水的红色固体;
Ⅲ. Cu2O+H2SO4===CuSO4+Cu+H2O。
【提出问题】 红色固体含有什么物质?
【猜想假设】
假设一:红色固体只含Cu。
假设二:红色固体只含Cu2O。
假设三:________________________。
【实验验证】 该小组为验证上述假设,取少量红色固体,加到足量稀硫酸中,观察到溶液变为蓝色,红色固体部分溶解。
【实验结论】 根据上述实验结果,可知红色固体中一定含有________。
【数据处理】 为进一步确定红色固体的成分,甲、乙两同学分别称取各自实验后的一定质量的红色固体,加到足量稀硫酸中使其充分反应,经过滤、洗涤、干燥后,称量剩余红色固体质量如表,请完善表中内容。
实验 人员 | 红色 固体/g | 剩余红色 固体/g | 实验结论 |
甲 | 7.2 | 3.2 | ① __________________ |
乙 | 4.08 | 2.48 | ② __________________ |
查看答案和解析>>
科目: 来源: 题型:
【题目】某科研小组设计利用稀硫酸浸取某废弃的氧化铜锌矿(主要成分为CuO和ZnO,其余成分既不与酸反应,也不溶解于水)的方案,实现废物综合利用。部分实验流程如图:
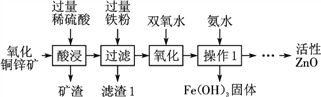
请根据上述实验流程回答下列问题:
(1) 操作1的名称是________。
(2) 在氧化铜锌矿中加入过量稀硫酸,主要成分发生反应的化学方程式为__________________________(任写一个)
(3) 加过量铁粉后,发生反应的基本反应类型是______,得到滤渣1的成分为_______(填化学式)。
(4) 在实验过程中,双氧水会与Fe2+反应生成Fe3+和水,以便在后续的操作中将溶液中铁元素除去。高锰酸钾溶液也能将Fe2+氧化成Fe3+,选用双氧水的优点是____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列装置,结合所学化学知识回答下列问题:
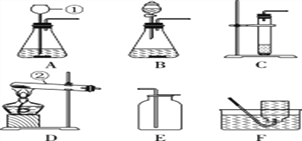
(1) 写出图中标号仪器的名称:① _______。
(2) 实验室用高锰酸钾制取氧气时,发生装置应选用________(填字母);其反应的化学方程式为__________________________。如果改用氯酸钾和二氧化锰制取氧气,反应前后二氧化锰的质量分数________(填“增大”、“减小”或“不变”)。
(3) 实验室制取少量二氧化碳时,发生装置最好选用________(填字母,下同),收集装置选用________,常用此收集方法的原因是____________________,某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊,可能的原因______________________________________________
(4) 化学反应可控制才能更好地为人类造福,我们可以通过改变反应的条件、药品用量、改进装置等途径来达到控制反应的目的。常温下块状电石(CaC2)与水反应生成乙炔(C2H2)气体和氢氧化钙,该反应的化学方程式是______________________________,实验室制取乙炔时,须严格控制加水速度,以免剧烈反应放热引起装置炸裂。图中适合制取乙炔气体的发生装置有________(填装置序号)。
(5)下图是干燥、收集某气体的装置。由实验装置可以推测该气体的有关性质,请你在表中找出相对应的选项(____)
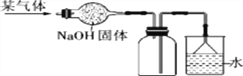
序号 气体性质 | A | B | C | D |
溶于水中所得溶液的pH | >7 | <7 | >7 | <7 |
其密度(ρ1)与空气密度(ρ2)的比较 | ρ1>ρ2 | ρ1>ρ2 | ρ1<ρ2 | ρ1<ρ2 |
在水中的溶解性 | 极易溶 | 难 溶 | 极易溶 | 难 溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com