
【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物进行系列实验。
(査阅资料)碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应:![]() 。
。
(进行实验)实验1:取质量比1:11的木炭粉和氧化铜混合物![]() ,进行实验。
,进行实验。
序号 | | |
装置 |
|
|
反应后物质的 颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量黑色物质 |
实验2:取一定量的混合物,用1-2装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
| 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
| 1:10 | 混有很少量黑色物质 | |
| 1:11 | 混有极少量黑色物质 | |
| 1:12 | 无黑色物质 | |
| 1:13 | 混有较多黑色物质 | |
(1)实验![]() 中,证明产生了
中,证明产生了![]() 的现象是______。
的现象是______。
(2)实验![]() 比
比![]() 更好的原因是______。
更好的原因是______。
(3)实验2的结论是______。
(反思与评价)
(4)实验2没有进行质量比为1:14的实验,理由是______。
(5)为检验![]() 的红色固体中是否
的红色固体中是否![]() 请你设计实验方案三
请你设计实验方案三![]() 方法、现象及结论
方法、现象及结论![]()
方法:______。可能的现象及结论______。
【答案】澄清石灰水变浑浊 使热量聚集,更好的加热氧化铜 木炭与氧化铜质量比为1:12时恰好完全反应,因此木炭与氧化铜反应的最佳质量比为1:12 木炭与氧化铜的质量比为1:13时,氧化铜已过量 取样品,加入稀硫酸 溶液由无色变成蓝色,且有红色固体剩余,样品中含有氧化亚铜
【解析】
(1)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以实验![]() 中,证明产生了
中,证明产生了![]() 的现象是:澄清石灰水变浑浊;
的现象是:澄清石灰水变浑浊;
(2)通过分析反应装置可知,实验![]() 比
比![]() 更好的原因是:使热量聚集,更好的加热氧化铜;
更好的原因是:使热量聚集,更好的加热氧化铜;
(3)实验2提供的数据以及实验现象可以看出,木炭与氧化铜质量比为1:12时恰好完全反应,因此木炭与氧化铜反应的最佳质量比为1:12;
(4)实验2没有进行质量比为1:14的实验,是因为当木炭与氧化铜的质量比为1:13时,氧化铜已过量;
(5)检验④的红色固体中含有![]() 的方法是:向红色固体中加入足量的稀硫酸,可以观察到溶液由无色变成蓝色,且有红色固体剩余。
的方法是:向红色固体中加入足量的稀硫酸,可以观察到溶液由无色变成蓝色,且有红色固体剩余。


科目:初中化学 来源: 题型:
【题目】科技推动着奥林匹克运动的发展,在奥运会中化学的表现十分突出。

(1)建造“鸟巢”时使用了大量的钢铁。其中炼铁的原理是在高温下用CO还原![]() ,其反应的化学方程式为______。
,其反应的化学方程式为______。
(2)“水立方”的膜结构是由化学合成材料ETFT制成的,化学式是![]() ,该物质中碳、氢、氟三种元素的原子个数比是______。
,该物质中碳、氢、氟三种元素的原子个数比是______。
(3)撑杆跳高使用的玻璃纤维杆,其主要成分是![]() 等,在物质分类中它们属于______(填序号)。
等,在物质分类中它们属于______(填序号)。
A.单质 B.化合物 C.氧化物
(4)采集奥林匹克圣火的唯一方式是:在奥林匹克的赫拉神庙前用凹面镜聚集太阳光,引燃圣火。此过程中最关键的燃烧条件是______。
(5)奥运会需要大量的能量。物质发生化学反应的同时,伴随着能量的变化,通常表现为______的变化。太阳能、______(任填一种新能源)、潮汐能等新能源的广泛开发利用还有待于研究。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】做完“铁丝在氧气中燃烧”实验后,小冬同学有两个疑惑不解的问题,于是他进行了以下探究活动,请你一同参与。
(问题1)铁丝燃烧时溅落下来的黑色高温熔化物中还有没有铁呢?
(查阅资料1)(1)自然界中铁的氧化物主要是![]() 和
和![]() 两种(
两种(![]() 极易被氧化为
极易被氧化为![]() );
);
(2)铁的氧化物均能溶于酸的溶液。
(实验探究)将冷却后的黑色物质碾碎,装入试管,加入______溶液,观察到的现象是______,说明铁燃烧时溅落下来的黑色物质中还有含有铁。
(问题2)铁燃烧的产物为什么不是![]() 呢?
呢?
(查阅资料2)
(1)![]() 和
和![]() 的分解温度、铁的熔点见右表:
的分解温度、铁的熔点见右表:
|
|
| |
分解温度 | 1538℃ | 1400℃ | — |
熔点 | — | — | 1535℃ |
(2)![]() 高温时分解成
高温时分解成![]()
(理论探讨)
根据实验现象,并结合表中数据,可推知铁丝在氧气中燃烧时所产生的高温应该在______之间,在此温度范围内![]() 已分解,所以铁在氧气中燃烧产生的是
已分解,所以铁在氧气中燃烧产生的是![]() 。
。
A.1400℃~1535℃ B.1400℃~1538℃ C.1535℃~1538℃
(拓展延伸)
(1)请写出铁丝在氧气中燃烧的化学方程式:______。
(2)实验中为了防止集气瓶炸裂,必须______。
(3)有些超市的食品密封包装盒的透明盖内放有黑色的![]() 粉末,若粉末的颜色______
粉末,若粉末的颜色______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
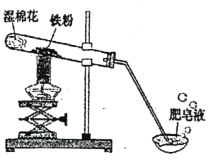
(1)试管尾部放一团湿棉花的作用是____________。
(2)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是_________________。
(3)探究试管中剩余固体成分是什么?
(查阅资料)
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
金属氧化物可以与酸反应,生成水和另一种金属化合物(如:CuO+2HCl=CuCl2+H20)。
(初步验证)试管中剩余固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是Fe与Fe3O4;
猜想二:剩余固体是__________。
(实验探究)
实验操作 | 实验现象 | 结论 |
取少量黑色固体于试管中,加入足量的稀盐酸。 | ________________ | 猜想一正确 |
________________ | 猜想二正确 |
(实验结论)铁和水蒸气反应的化学方程式为_____________。
(反思与交流)该黑色固体不可能是Fe2O3,理由是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E都是初中化学常见的物质。B、D、E均为氧化物,常温下B为固态,D为液态,E为气态;A、B、C中均含有同一种金属元素。它们之间的转化关系如图所示(部分生成物略去)。
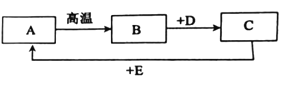
写出下列物质的名称:
A_______
E________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室中同学们进行了如下图所示实验,用正确的试剂成功探究出了在空气中久置的氢氧化钠固体的变质情况。下列说法正确的是

A. 甲溶液可以选择Ca(OH)2溶液或CaC12溶液(查阅资料得知:CaC12溶液显中性)
B. 若Ⅱ、Ⅲ均有明显现象,则说明样品部分变质
C. D物质可能是气体,也可能是沉淀
D. 溶液B中的溶质至少有两种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】家用纯碱常含有少量的氯化钠杂质。为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品1.1g,充分溶解于13g水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示。求:(友情提示:该反应的化学方程式为CaC12+Na2C03=CaC03↓+2NaC1)

(1)该纯碱样品中碳酸钠的质量______。
(2)恰好完全反应时所得溶液的溶质质量分数______。
(3)通过交流反思,同学们认为下列做法会影响样品中碳酸钠的质量分数测定结果的是______
A.加入氯化钙溶液质量太少(少于11.1g)
B.称量完纯碱样品质量后,在放入烧杯的过程部分样品洒出
C.量取溶解纯碱样品的水时仰视读数
D.使用足量稀盐酸代替氯化钙溶液进行实验,测定反应后生成CO2的质量并计算
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图X表示M、N两种不含结晶水的固体物质的溶解度曲线。根据图示判断,下列说法中正确的是( )
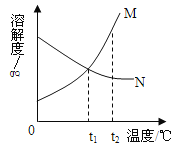
A. 物质M、N的溶解度都随温度的升高而增大
B. 将t1℃时M的饱和溶液升温至t2℃,溶液的质量分数增大
C. 在t1℃时,M、N的饱和溶液的溶质的质量分数相等
D. 将M、N t2℃时的饱和溶液分别降温至t1℃,两溶液中均析出晶体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是实验室中常见的气体制备和收集装置,请回答下列问题:
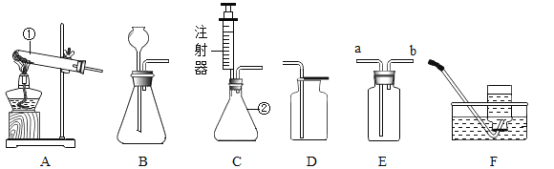
(1)写出图中标有序号的仪器名称:①______________。
(2)实验室用高锰酸钾制取氧气,选用发生装置________(填字母序号),O2的检验方法是__________。但是该装置要改进的一点是_________,目的是_______反应的化学方程式_________。
(3)欲使用装置E用排空气法收集CO2,则气体应从_____(填a或b)端通人;欲使用装置E用排水法收集O2,先将瓶中装满水,再将气体从_____(填a或b)端通人。
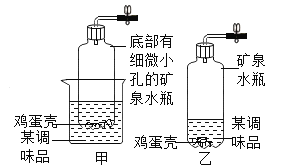
(4)小明同学选用片状的鸡蛋壳和________(填一种厨房调味品)反应来制取二氧化碳,并利用矿泉水瓶、玻璃杯、橡皮塞、导管、止水夹等组装了如图所示甲、乙气体发生装置。比较甲、乙装置甲装置的优点是____________________(写一点即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com