
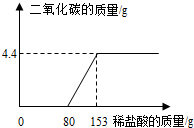
 某工厂排放的废水中含有NaOH和Na2CO3,为了测定废水中NaOH的质量分数,取废水100g逐滴加入稀盐酸至过量,测得生成气体的质量与所加稀盐酸的质量关系如图所示.试计算:
某工厂排放的废水中含有NaOH和Na2CO3,为了测定废水中NaOH的质量分数,取废水100g逐滴加入稀盐酸至过量,测得生成气体的质量与所加稀盐酸的质量关系如图所示.试计算:分析 氢氧化钠和稀盐酸反应生成氯化钠和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,反应产生了4.4g二氧化碳,根据二氧化碳质量可以计算碳酸钠的质量和反应的氯化氢质量,根据氯化氢质量可以计算稀盐酸的质量分数,进一步可以计算恰好完全反应时所得溶液的溶质质量分数.
解答 解:(1)当所取样品完全反应时,生成气体的质量为4.4g.
故填:4.4.
(2)设和碳酸钠反应的氯化氢质量为x,生成氯化钠质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
73 117 44
x y 4.4g
$\frac{106}{x}$=$\frac{73}{y}$=$\frac{117}{z}$=$\frac{44}{4.4g}$,
x=10.6g,y=7.3g,z=11.7g,
稀盐酸质量分数为:$\frac{7.3g}{153g-80g}$×100%=10%,
设和氢氧化钠反应生成氯化钠质量为z,
NaOH+HCl═NaCl+H2O,
36.5 117
80g×7.3% z
$\frac{36.5}{80g×7.3%}$=$\frac{117}{z}$,
z=18.72g,
恰好完全反应时所得氯化钠溶液溶质质量分数为:$\frac{11.7g+18.72g}{100g+153g-4.4g}$×100%=12.2%,
答:恰好完全反应时所得氯化钠溶液溶质质量分数为12.2%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 倒入废液缸 | B. | 交回实验室集中处理 | ||
| C. | 放回原试剂瓶 | D. | 投入通向下水道的水槽内 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
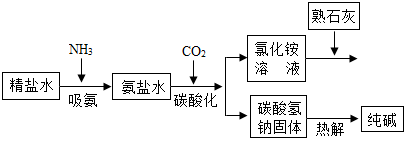 利用井盐和合成氨生产的氨气及二氧化碳生产纯碱的“联合制碱法”是由我国著名化学家侯德榜先生发明的,其氯化钠的利用率高达96%.其原理流程如图所示:
利用井盐和合成氨生产的氨气及二氧化碳生产纯碱的“联合制碱法”是由我国著名化学家侯德榜先生发明的,其氯化钠的利用率高达96%.其原理流程如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 |
| 取少量上层料液,滴加稀盐酸 | 无明显现象 |
| 另取少量上层料液,滴加碳酸钠溶液 | 产生白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
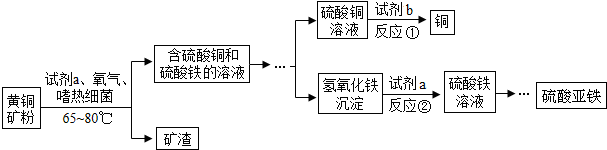
| A. | (1)(2) | B. | (2)(3) | C. | (4)(5) | D. | (2)(5) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
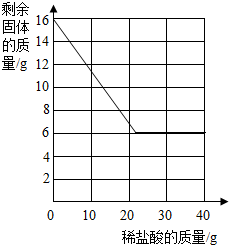 某研究性学习小组的同学前往当地的大理石进行调査,他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测.采用了以下的办法:取16g这种大理石,逐滴滴加稀盐酸,剩余固体的质量与所加盐酸的质量关系如图示(杂质不溶于水,不与盐酸反应).
某研究性学习小组的同学前往当地的大理石进行调査,他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测.采用了以下的办法:取16g这种大理石,逐滴滴加稀盐酸,剩余固体的质量与所加盐酸的质量关系如图示(杂质不溶于水,不与盐酸反应).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
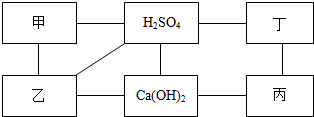 如图中每条直线两端的物质在一定条件下都可以发生化学反应,其中甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、盐酸四种物质中的一种.
如图中每条直线两端的物质在一定条件下都可以发生化学反应,其中甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、盐酸四种物质中的一种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com