
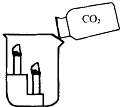
 点燃两支蜡烛,分别放在白铁皮架的两个阶梯上,把白铁皮架放在烧杯里(如图所示).沿烧杯内壁缓缓倾倒二氧化碳.
点燃两支蜡烛,分别放在白铁皮架的两个阶梯上,把白铁皮架放在烧杯里(如图所示).沿烧杯内壁缓缓倾倒二氧化碳.分析 因为二氧化碳的密度比空气的大,所以可以像倾倒液体一样倒入烧杯中,二氧化碳不燃烧,也不支持燃烧;因此下层蜡烛先被熄灭,上层后被熄灭.
解答 解:(1)因沿烧杯内壁缓缓倾倒二氧化碳时,可观察到下面的蜡烛先熄灭,过一会上面的蜡烛再熄灭,故答案为:烧杯中的蜡烛下面的先熄灭,上面的后熄灭;
(2)由蜡烛熄灭可知二氧化碳不燃烧也不支持燃烧,由蜡烛熄灭的顺序可知下面的先熄灭,即二氧化碳由下到上充满烧杯中,则密度比空气的大,故答案为:一般情况下,二氧化碳既不能燃烧,也不能支持燃烧;二氧化碳的密度大于空气的密度;
(3)因二氧化碳不燃烧也不支持燃烧,且密度比空气的大,可使可燃物与空气隔绝而起到灭火的作用,即可利用二氧化碳来灭火,故答案为:灭火.
点评 本题考查学生根据实验中观察到的现象来分析其性质和用途,现象的观察是解答本题的关键,学生应注意观察的全面性及细致性,并明确观察的重点及观察方法.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:实验探究题

| 物质 | K2CO3 | K2SO | KMnO4 |
| 溶解度/g | 111 | 11.1 | 6.34 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源:2017届湖北省老河口市九年级中考适应性考试化学试卷(解析版) 题型:选择题
栀子花开,香气四溢,此现象说明( )
A.分子在不断运动 B.分子间有间隔
C.分子的体积很小 D.分子的质量很小
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
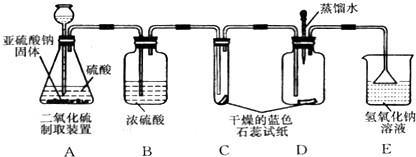
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
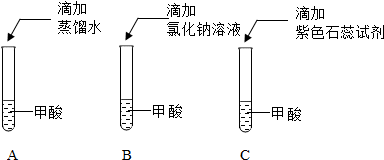
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com