
【题目】海水素有“液体工业原料”之美誉。工业“从海水中提取镁”的主要流程如下:
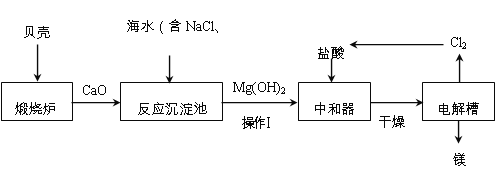
(1)煅烧炉中,发生反应的化学方程式为:CaCO3![]() CaO+CO2↑,此反应属于基本类型中的______反应。
CaO+CO2↑,此反应属于基本类型中的______反应。
(2)反应沉淀池中发生如下反应:
①CaO+H2O=Ca(OH)2;
②Ca(OH)2+ MgSO4= CaSO4 + Mg(OH)2↓,
操作Ⅰ为_________。
(3)电解槽中,能生成镁的反应物为____________。
(4)从海水中提取镁的过程中,镁元素的化合价变化为__________。
科目:初中化学 来源: 题型:
【题目】乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体。
(提出问题)白色固体是什么物质?
(做出猜想)小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二:__________________;猜想三:Ca(OH)2。
他的依据是____________________。
(交流反思)经过同学们交流讨论,认为猜想一不成立。否定猜想一的理由是:_______________。
(进行实验)
(1)取少量白色固体放入试管中,滴加稀盐酸,没有观察到____________,证明猜想二不成立。
(2)取少量白色固体加入到水中,静置后取上层清液,___________,有白色沉淀出现,证明猜想三成立。该反应的化学方程式为:_____________。
结论:白色固体是Ca(OH)2。由碳化钙与水反应制取乙炔的化学方程式为___________
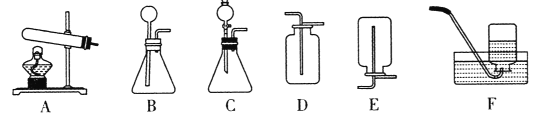
(拓展应用)已知碳化钙与水反应非常剧烈,乙炔的密度比空气略小。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的发生装置是_____,收集装置是_________(选填图中装置序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
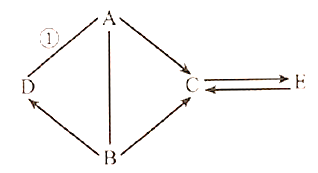
【题目】A、B、C、D、E是初中化学常见的物质。A、C是氧化物,B是胃液中含有的酸,D是通常状况下密度最小的气体,E可用作补钙剂,反应①中有红色物质生成。物质间相互关系如图所示(“一”表示两端物质能发生化学反应,“→”表示物质间的转化关系;部分反应物、生成物和反应条件已略去),请回答。
(1)A的化学式_____
(2)写出C→E的化学方程式_____。
(3)反应①的基本反应类型是_____。
(4)写出B的一种用途_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是一种常用的化肥,工业上生产尿素的反应的微观示意图如图所示:
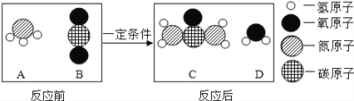
则下列说法正确的是( )
A. 图中A、B、D三种物质都是氧化物
B. 参加反应的A、B两物质的粒子数之比为1 : 1
C. 该反应前后分子种类、原子种类均没有发生改变
D. 参加反应的A、B两物质的质量之比为17∶22
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
A 木炭燃烧 | B铁丝燃烧 |
(1)木炭在氧气中燃烧时,可观察到的实验现象为______________________。 (2)若验证生成物,需向集气瓶中加入的药品为_________________。 |
(1)铁丝在氧气中燃烧的化学方程式为_______。 (2)实验时,预先在集气瓶里装少量水的作用是_________________________。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验能达到目的的是
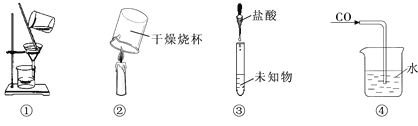
A. ①分离溶液中的FeCl2和CuCl2 B. ②检验蜡烛燃烧生成的水
C. ③检验CO32- 的存在 D. ④用水吸收CO
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)用化学方程式表示:
(1)用稀盐酸除去小刀上的铁锈:_____ 。
(2)有非金属单质参加的置换反应: 。
(3)有非金属单质生成的反应: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是我国最新研制的大型水面救援飞机,飞机的外壳主要是镁铝合金,飞机中有些零件是由钢铁制成的。
(1)镁铝合金属于_____(填“金属”或“合成”)材料。
(2)生活中常在钢铁制品表面喷漆,不仅美观,而且可有效防止铁与_____接触而生锈。
(3)向一支试管中加入一根生锈的铁钉,然后加入一定量的稀硫酸,写出稀硫酸除铁锈的化学方程式_____。铁锈消失后,将铁钉取出,若要检验试管中的液体是否含有稀硫酸,可选择的试剂是_____(填字母)
A.酚酞溶液 B.Cu
C.CuO D.BaCl2溶液
(4)金属矿物储量有限,而且不能再生。保护金属资源的有效途径,除防止金属腐蚀外,还有_____(写出一条即可)

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上炼铁炼钢和轧制钢材的主要流程如图.

已知生铁的含碳量为 2%--4.3%,钢的含碳量为 0.03%--2%。
(1)反应:①Fe2O3+3CO ![]() 2Fe+3CO2 ,②3C + 2Fe2O3
2Fe+3CO2 ,②3C + 2Fe2O3 ![]() 4Fe + 3CO2↑。属于置换反应的是_________ ,用于高炉炼铁的原理是 _________(填序号)
4Fe + 3CO2↑。属于置换反应的是_________ ,用于高炉炼铁的原理是 _________(填序号)
(2)生铁属于 _________ (填“纯净物”或“混合物”),其熔点比纯铁 _________(填“高”或“低”),铁是由 _________ 构成的物质(填“分子”、“原子”或“离子”)。
(3)炉渣中含有硅酸钙(CaSiO3),其中硅元素的化合价是 _________ 。
(4)将钢锭轧成钢板,属于_________(填“物理变化”或“化学变化”) 。
(5)钢铁制品可能会生锈,写出用稀硫酸除锈反应的化学方程式 _____________________ 。
(6)请用一个化学方程式证明铁的活泼性大于铜 __________________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com