
【题目】A、B、C、D、E是初中化学常见的物质。A、C是氧化物,B是胃液中含有的酸,D是通常状况下密度最小的气体,E可用作补钙剂,反应①中有红色物质生成。物质间相互关系如图所示(“一”表示两端物质能发生化学反应,“→”表示物质间的转化关系;部分反应物、生成物和反应条件已略去),请回答。
(1)A的化学式_____
(2)写出C→E的化学方程式_____。
(3)反应①的基本反应类型是_____。
(4)写出B的一种用途_____。

【答案】 CuO Ca(OH)2+CO2=CaCO3↓+H2O 置换反应 金属除锈
【解析】
根据A、B、C、D、E是初中化学常见的物质,A、C是氧化物,B是胃液中含有的酸,所以B是盐酸,D是通常状况下密度最小的气体,所以D是氢气,E可用作补钙剂,反应①中有红色物质生成,所以A是氧化铜,C是二氧化碳,E是碳酸钙,碳酸钙和二氧化碳可以相互转化,然后将推出的物质进行验证即可。
(1)A的化学式是CuO;
(2)C→E的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(3)反应①是氢气和氧化铜在加热的条件下生成铜和水,基本反应类型是置换反应;
(4)B的一种用途是:金属除锈。


科目:初中化学 来源: 题型:
【题目】如图所示是甲物质的溶解度曲线。把甲物质的不饱和溶液变为饱和溶液,下列有关说法正确的是
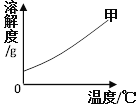
A. 溶剂的质量一定变小
B. 溶液的质量可能不变
C. 溶质的质量分数一定变大
D. 溶质的质量一定不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在化学反应前后有元素的化合价发生变化的反应称为氧化还原反应。据此可判断下列化学反应属于氧化还原反应的是( )
A. CaO+H2O ![]() Ca(OH)2 B. 2H2O2
Ca(OH)2 B. 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
C. Cu(OH)2![]() CuO+H2O D. HCl+AgNO3
CuO+H2O D. HCl+AgNO3![]() AgCl↓+HNO3
AgCl↓+HNO3
查看答案和解析>>
科目:初中化学 来源: 题型:
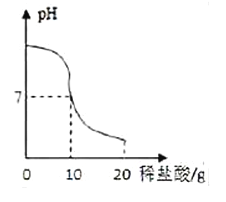
【题目】将20.0g稀盐酸逐滴加入到10.0g溶质质量分数为40%的氢氧化钠溶液中,边滴加边搅拌,随着稀盐酸的滴加,溶液的pH变化情况如图所示,溶液的温度变化如表所示(不考虑反应过程中热量散失)
反应时间(s) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶液温度(℃) | 20.5 | 20.6 | 20.7 | 20.8 | 20.9 | 20.8 | 20.7 |
(1)当稀盐酸与氢氧化钠溶液恰好完全反应时,溶液的温度是_____℃
(2)计算稀盐酸中溶质的质量分数_________(精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氟元素、钙元素对人体的主要作用是帮助构造骨骼和牙齿。右图是氟元素和钙元素的原子结构示意图,以及这两种元素摘自元素周期表的图示。
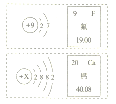
其中x=_______,钙的离子符号为____,氟元素与钙元素形成化合物的化学式为______。葡萄糖酸钙(化学式Ca(C6H11O7)2)是一种促进骨骼生长的营养物质,葡萄糖酸钙由_________种元素组成。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国高铁制造已处于世界先进水平。请回答下列问题。
(1)田老师乘高铁外出学习,在列车上购买了一盒快餐,其中有米饭、酱牛肉、炒白菜,牛肉中富含的营养素是_____。快餐盒使用的是可降解塑料,这样可以减轻的环境问题是“_____”。
(2)高铁水箱中装有生活用水,在净水过程中利用了活性炭的_____性。请写出节约用水的一种做法_____
(3)越来越多的新型材料应用于高铁建设,其中合金属于_____(填“金属”或“合成”)材料。
(4)合金较其组分金属具有一定的优良性能。用钒钢合金制造高铁的钢轨,主要利用其_____的性能。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为实验室制取气体的常见装置。请回答:

(1)写出用A装置制取氧气的化学方程式_____。
(2)若收集﹣瓶氧气用于完成铁丝在氧气中燃烧的实验最好用_____(填序号)装置收集氧气。
(3)实验室制取二氧化碳发生装置选择B的依据是_____,写出该反应的化学方程式_____。
(4)若用F装置干燥二氧化碳,瓶中应盛装_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海水素有“液体工业原料”之美誉。工业“从海水中提取镁”的主要流程如下:
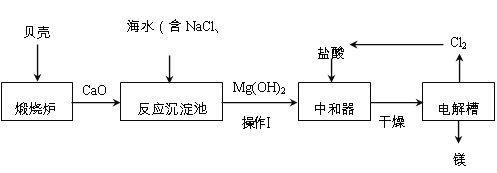
(1)煅烧炉中,发生反应的化学方程式为:CaCO3![]() CaO+CO2↑,此反应属于基本类型中的______反应。
CaO+CO2↑,此反应属于基本类型中的______反应。
(2)反应沉淀池中发生如下反应:
①CaO+H2O=Ca(OH)2;
②Ca(OH)2+ MgSO4= CaSO4 + Mg(OH)2↓,
操作Ⅰ为_________。
(3)电解槽中,能生成镁的反应物为____________。
(4)从海水中提取镁的过程中,镁元素的化合价变化为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁的冶炼与利用是学习和研究化学的重要课题。
Ⅰ.铁的冶炼,竖炉炼铁的工艺流程如图1所示。
(1)“燃烧室”中CH4燃烧的作用是__
(2)写出“还原反应室”中炼铁的一个反应的化学方程式__。
(3)CH4与高温尾气中的CO2或H2O都能反应生成CO和H2,则16g CH4在催化反应室中完全反应后,理论上得到H2的质量(m)范围是__。
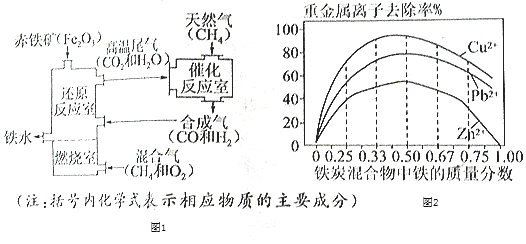
Ⅱ.铁的利用,利用铁炭混合物(铁屑和活性炭的混合物)处理含有Cu(NO3)2,Pb(NO3)2和Zn(NO3)2的铜冶炼废水。在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中重金属离子的去除率,实验结果如图2所示。
(1)铁炭混合物中铁的质量分数为100%时,水中的Cu2+、Pb2+能被除去、而Zn2+不能被除去,其原因是__。
(2)铁炭混合物中铁的质量分数为0时,也能除去水中少量的重金属离子,其原因是__。
(3)处理效果最好时,铁炭混合物中的铁的质量分数为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com