
【题目】为探究分子的运动及影响分子运动速率的因素,某同学设计了以下三种实验方案,请回答有关问题
(实验方案一)如图1。
①观察到的实验现象是_____;
②该方案的不足之处是_____。(说出一点即可)
(实验方案二)如图2、图3。
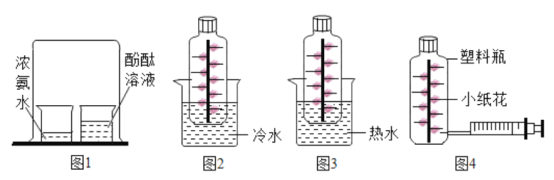
图中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图4的操作方式分别用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40℃的热水中。
①观察到的现象是_____;
②图2、图3采用对照实验的方法,变量只有一个,被控制的量有多个,请说出4个被控制的量_____。
③若图4中的小纸花上喷有_____,而注射器向瓶中注入的是浓盐酸,可以观察到小纸花的颜色从下至上变为红色。
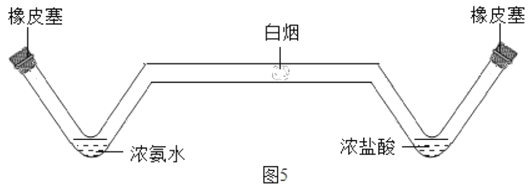
(实验方案三)如图5
用长柄V形玻璃管进行实验,向左、右两端的V形玻璃管口分别同时滴入等量的浓氨水和浓盐酸,塞紧橡皮塞。
①过一会儿后,从图5中观察到有白烟产生且位置偏右,说明_____。
②图5中生成白烟的反应为化合反应,其化学方程式为_____。
(实验结论)上述实验证明:分子是不断运动的,且分子的运动速率与_____有关。(说出一点即可)
【答案】酚酞溶液变红色 ;没有设计对比实验 。小纸花由下而上依次变红色,并且图3比图2变色快 ;塑料瓶的材质、大小、形状完全相同;小纸花大小和形状相同;小纸花上都均匀喷有酚酞溶液;用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水 。石蕊溶液 ,氯化氢和氨气发生了化学反应,氨分子运动的比氯化氢分子运动的快 。NH3+HCl=NH4Cl 。相对分子质量
【解析】
微观粒子是不断运动的,温度越高运动的越快;显碱性溶液能使酚酞试液变红色,显酸性溶液能使石蕊试液变红色;氨气和氯化氢反应生成氯化铵。
【实验方案一】
①观察到的实验现象是酚酞试液变红色;②该方案的不足之处是没有设计对比实验,不能排除空气中的物质使酚酞溶液变色。
【实验方案二】
①观察到的现象是小纸花由下而上依次变红色,并且图3比图2变色快;②4个被控制的量是塑料瓶的材质、大小、形状完全相同;小纸花大小和形状相同;小纸花上都均匀喷有酚酞溶液;用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水;③若图4中的小纸花上喷有石蕊溶液,而注射器向瓶中注入的是浓盐酸,可以观察到小纸花的颜色从下至上变为红色。
【实验方案三】
①过一会儿后,从图5中观察到有白烟产生且位置偏右,说明氯化氢和氨气发生了化学反应,氨分子运动的比氯化氢分子运动的快;②图5中生成白烟,是因为氨气和氯化氢反应生成了氯化铵,反应的化学方程式为:NH3+HCl=NH4Cl。
上述实验证明:分子是不断运动的,且分子的运动速率与相对分子质量有关,即相对分子质量越小,运动的速率越快。


科目:初中化学 来源: 题型:
【题目】请用化学知识回答下列问题:
(1)吸烟对人体有害。燃着的香烟产生的烟气中含有一 种能与血液中血红蛋白结合的有毒气体,这种气体能使氧化铜还原成铜,请写出还原氧化铜的化学方程式____________,
(2)金属铝的化学性质非常活泼,但金属Al具有很好的抗腐蚀性能的原因是_______;
(3)物质在溶解时,常常会使溶液的温度发生改变。现有下列三种物质; NaCl、NH4NO3、NaOH,其中溶解时会放热的是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过下列图示实验得出的结论中正确的是
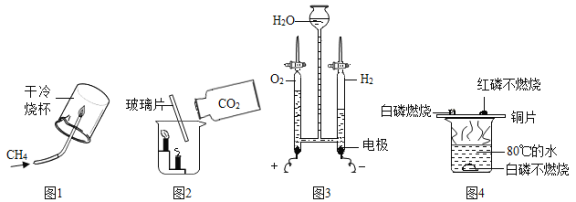
A.图1所示实验既说明甲烷具有可燃性,又说明甲烷中含有碳、氢两种元素
B.图2所示实验既说明二氧化碳密度比空气大,又说明二氧化碳不能燃烧也不支持燃烧
C.图3所示实验既说明电解水生成氢气和氧气,又说明水是由氢气和氧气组成的
D.图4所示实验既可探究可燃物的燃烧条件,又说明红磷不是可燃物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁及其化合物在生产生活中有广泛的应用。
(一)铁的应用和防护
(1)某麦片中含微量铁粉,食用后铁粉与胃酸反应转化为人体可吸收的铁元素,反应的化学方程式为______。
(2)铁锈主要成分是Fe2O3nH2O ,铁生锈主要与空气中的______有关。
(3)如图实验说明NaCl在铁生锈中的作用是______。
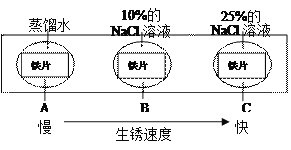
(4)铁生锈的次要过程:
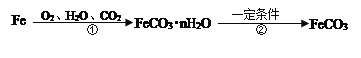
写出Fe转化为FeCO3总反应的化学方程式______。
(5)为防止铁生锈,可对铁制品进行“发蓝”处理,使其表面生成致密氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为______。
(二)废铁的再利用
黄钠铁矾[NaFex(SO4)y(OH)z]是一种高效净水剂。用废铁屑(主要成分为Fe,含少量Fe2O3和FeCO3)制备黄钠铁矾的主要流程如下:

(1)将废铁屑研磨成粉末的目的是______。
(2)“酸溶”时H2SO4与Fe、FeCO3反应,还发生的化学方程式有______和Fe+Fe2(SO4)3=3FeSO4。
(3)“转化1”发生反应的化学方程式为______。反应时温度不宜过高的原因是______。
(三)黄钠铁矾组成确定
称取9.70g黄钠铁矾,用下图装置进行热分解实验。
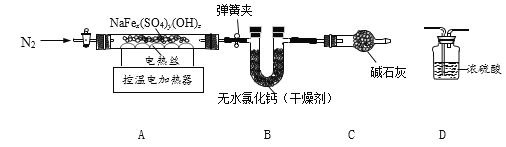
(资料)①NaFex(SO4)y(OH)z在T1℃分解会生成H2O(气态),提高温度至T2℃继续分解产生SO3气体,并得到Fe203和Na2SO4。
②浓硫酸可用于吸收SO3。
(1)装配好实验装置后,先要______。
(2)分别控制温度在T1℃、T2℃对A中固体加热。
①控制温度在T1℃加热,实验后测得B装置质量增加1.08g。
②用D装置替换B装置,控制温度在T2℃,加热至反应完全。
③T1℃、T2℃时,加热后均通入一段时间N2,目的是______。
(3)完全反应后,将A装置中固体溶于足量水,过滤、洗涤、烘干得4.80g固体,将滤液蒸干得1.42g固体(不含结晶水)。
结论:NaFex(SO4)y(OH)z中,x:y:z=_______。
反思:若该实验过程中缺少C装置,则x:z的值____(选填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】充分燃烧1kg天然气和煤所产生CO2和SO2的质量如图所示,下列说法不正确的是( )
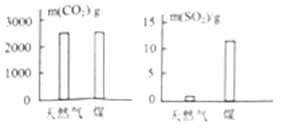
A. 等质量的煤和天然气充分燃烧,产生CO2的量接近,但产生SO2的量却相差较大
B. 煤、天然气充分燃烧产生的CO2和SO2是导致酸雨的主要气体
C. 煤、天然气及石油等是重要的化石燃料,属于不可再生能源
D. 由图示可知,提倡将煤改为天然气作燃料,有利于改善空气质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】进行如下微型实验,研究物质的性质。
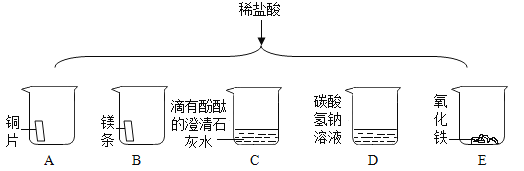
(1)能产生气泡的是_____________(填序号)。
(2)能证明C中发生反应的现象是______________。
(3)有一只烧杯中的物质不与稀盐酸反应,原因是__________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表是NaCl和Na2CO3在不同温度下的溶解度,下列说法中不正确的是( )
温度/℃ | 0 | 10 | 20 | 30 | 40 | |
溶解度/g | NaCl | 35.0 | 35.5 | 36.0 | 36.5 | 37.0 |
Na2CO3 | 6.0 | 10.0 | 18.0 | 36.5 | 50.0 | |
A. 两种物质溶解度相等的温度在30℃
B. 生活在盐碱湖附近的人们习惯“夏天晒盐、冬天捞碱”
C. 40℃时,5gNaCl中加10g水可得溶质质量分数为26.3%的溶液
D. 40℃时,9g Na2CO3中加20g水,充分溶解后再降温到10℃,析出固体的质量为7g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过化学变化可以制备物质。
(1)某兴趣小组欲用200 g 4%的氢氧化钠溶液吸收二氧化碳制备碳酸钠,反应的化学方程式是___;若要将提供的氢氧化钠全部转化为碳酸钠,请列出计算需二氧化碳质量(x)的比例式_____;
(2)在实验中,该小组同学发现,要定量控制通入氢氧化钠溶液中二氧化碳气体的质量,难以操作。请分析若通入二氧化碳气体的量不足时会导致产物中混有的杂质是_____;
(3)查阅资料:
Na2CO3+CO2+H2O===2NaHCO3;NaHCO3+NaOH===Na2CO3+H2O;
该小组同学将制备方案改进如下:
步骤 | 实验操作 | 实验目的 |
一 | 将200g 4%的NaOH溶液分为两等份 | / |
二 | ①_____ | 将其中一份溶液中的NaOH全部转化为NaHCO3 |
三 | 将步骤二所得溶液小心煮沸1~2分钟 | ②___ |
四 | ③___ | 将NaHCO3全部转化为Na2CO3 |
(4)假设每步转化都完全,该小组同学利用改进后的方案制取的碳酸钠质量m1=___g;经老师指导,该小组同学将步骤四反应后的溶液蒸干并充分灼烧得到碳酸钠粉末的质量为m2g,发现m1=m2,由此证明他们的方案改进成功。
查看答案和解析>>
科目:初中化学 来源: 题型:
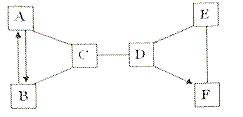
【题目】A~F是初中化学常见的物质,已知A、B、C、D、E是五种不同类别的物质,A是空气中含有的一种气体,E是地壳中含量最多的金属元素组成的单质,F中各元素质量比为2:1:2,六种物质之间的反应与转化关系均为初中化学常见的化学反应,图中“﹣”表示相连的物质能相互反应,“→”表示一种物质转化成另一种物质(部分反应物、生成物及反应条件已略去)请回答下列问题:
(1)E物质的化学式_____。
(2)A和C反应的化学方程式_____。
(3)E和F反应的化学方程式_____。
(4)如图所有的化学反应中涉及到的基本反应类型有_____种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com