
【题目】汽车尾气是造成城市空气污染的重要原因,为减少有害气体的排放,人们在汽车排气管上安装“催化转化器”,使尾气中的CO和NOx转化为N2和CO2。
(1)写出CO和NOx在“催化转化器”中反应的化学方程式__________________;
(2)若x=1,CO和N2在化学方程式中的化学计量数之比为________________;
(3)若x=2.5时,则NOx的化学式为_________________。
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:初中化学 来源: 题型:
【题目】水和溶液在生活、生产和化学实验中起着重要的作用
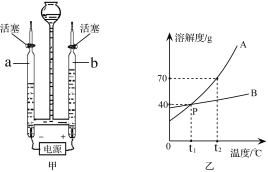
(1)上图甲是电解水的实验装置,切断装置中的电源,用_____分别检验a、b两个玻璃管中产生的气体。
(2)上图乙为A、B两种固体物质的溶解度曲线。据图回答:
①A、B两种物质的溶解度曲线交于P点,则P点表示的意义是_____。
②若A中含有少量B,提纯A应采取的方法是_____。
③有同学说:“t2℃时A物质饱和溶液中溶质的质量分数为70% 。”这种说法对吗?_____(填“对”或“不对”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为某同学所做的实验及现象。
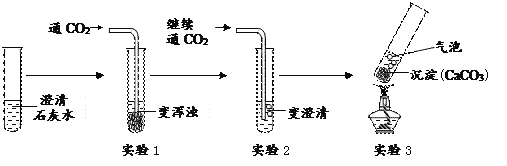
(1)实验1发生反应的化学方程式为________。
(2)实验2生成Ca(HCO3)2。实验3发生反应的化学方程式为________,该实验说明CaCO3比Ca(HCO3)2热稳定性________(选填“强”或“弱”)。
(3)某地区硬水中溶有较多的可溶性Ca(HCO3)2 、Mg(HCO3)2 。
①生活中常用________来区分硬水和软水。
②煮沸硬水可降低水的硬度,同时生成难溶性混合物固体A。
[猜想]固体A中除CaCO3外,还含有:
猜想1:只含MgCO3 猜想2:只含Mg(OH)2 猜想3:MgCO3和Mg(OH)2
[实验]取10.0g干燥的固体A,加入足量的稀盐酸充分反应,产生4.4gCO2气体。
[结论]①猜想1、2错误。其中判断猜想1错误的理由是________。
②猜想3正确。固体A中MgCO3和Mg(OH)2的质量比是________。
[拓展]在100℃时加热溶有较多Ca(HCO3)2 、Mg(HCO3)2的硬水,1小时后得到CaCO3和Mg(OH)2MgCO33H2O的固体混合物。写出Mg(OH)2MgCO33H2O与稀盐酸反应的化学方程式________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小强称取一定量NaOH固体于烧杯中,观察其在空气中的潮解与变质情况,一段时间后,称得固体质量为15.0g然后向该烧杯中逐滴加入一定溶质质量分数的稀盐酸,过一会后观察到烧杯中有气泡冒出,当烧杯中不再冒出气泡时,所滴加稀盐酸的质量是200.0g此时称得烧杯中溶液的质量为213.9g。请回答
(1)烧杯中冒出的气体的质量是_____g
(2)小强根据NaOH固体表面潮湿及加入稀盐酸有气泡冒出的现象,判断NaOH固体潮解并已变质,NaOH变质的化学方程式为_____。求变质后的固体中含碳酸钠的质量_________。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g进行系列实验。
(查阅资料)①氧化铜(CuO)为黑色固体。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应:Cu2O + H2SO4 = CuSO4 + H2O + Cu
(进行实验)
实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。

实验2:取一定量的混合物,用1—2装置进行实验。
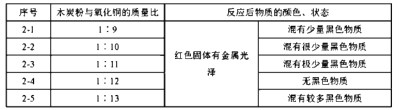
(解释与结论)
(1)配平化学方程式:___C+___CuO高温 ___Cu+ ___CO2↑。
(2)实验1—2中,证明产生CO2的现象是_______________________。
(3)实验1的目的是__________。
(4)实验2的结论是_____________。
(反思与评价)
(5)实验2没有进行质量比为1:14的实验,理由是________________。
(6)为检验2—4的红色固体中是否含Cu2O,所需试剂是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究金属活动性,将锌和铜分别放入稀硫酸中,铜不反应而锌的表面有气泡产生,写出锌和稀硫酸反应的化学方程式:___。老师告诉学生,铜和浓硫酸在加热的条件下也能反应且产生气体。
(提出问题)铜与浓硫酸反应的生成物是什么?其中气体是什么?
(猜想假设)同学们对产生的气体作出了猜想。
猜想一:氢气;
猜想二:二氧化硫;
猜想三:氢气和二氧化硫的混合物。
(查阅资料)
(1)二氧化硫可以使品红溶液褪色,也能和碱性溶液反应
(2)H2+CuO![]() Cu+H2O
Cu+H2O
(实验探究)师生设计了如下装置进行实验(部分仪器省略),请完成下列表格。
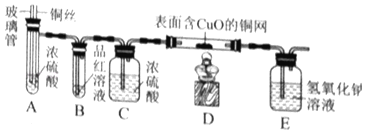
主要实验步骤 | 主要现象 | 解释或结论 |
①加热装置A一段时间 | 装置B中的现象是_____ | 有二氧化硫生成 |
②点燃装置D处酒精灯 | 装置D玻璃管中无明显现象 | 猜想_____正确 |
③停止加热,将铜丝上提,向装置A中玻璃管鼓入空气 | / | / |
④冷却,将A中液体用水稀释 | A中液体变为_____色 | 有硫酸铜生成 |
(表达交流)
(1)在步骤③中,鼓入空气的目的是_____。
(2)请完成铜与浓硫酸反应的化学方程式:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+_____
CuSO4+SO2↑+_____
(反思拓展)
(1)若将装置A中铜丝换成锌片,随着反应的进行,硫酸的浓度逐渐变小,装置D玻璃管中看到的现象是_____。
(2)下列各组药品能够证明锌的活动性比铜强的是_____(填序号)。
①锌、铜、稀盐酸②锌、硫酸铜溶液③锌、铜、氯化镁溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧气是人类无法离开的物质,在不同的生活、生产环境中对氧气浓度的要求不同,人类常采用不同的方法制取氧气。
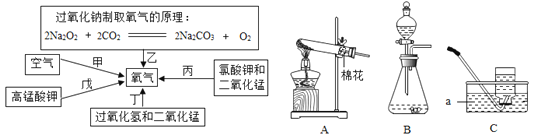
(1)工业上一般采用甲路径分离净化后的液态空气制取氧气。在生产中应控制温度的范围是___;(已知在1.0l×105Pa时,O2的沸点为-183℃,N2的沸点为-196℃)
(2)实验室常通过丙、丁、戊三种路径来制取氧气;
①写出装置C中a仪器的名称___;
②若用路径戊,应选择的发生装置是____;
③若用路径丁,发生反应的化学方程式是___;
④在这三种路径中消耗能源最少的是___(填序号);
(3)在上述五个路径中最适合潜水艇中获得氧气的是___(填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】结合右图中KNO3和NaCl的溶解度曲线,回答下列问题。
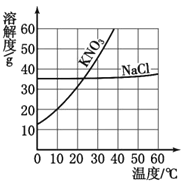
(1)10℃时,溶解度较大的物质是__________;
(2)20℃时,将20gNaCl加入到100g水中,充分溶解后,得到__________(填“饱和”或“不饱和”)溶液;
(3)将50℃的KNO3饱和溶液降温至10℃,下列分析正确的是__________。
A.溶液中溶质质量不变B.降温后的溶液仍是饱和溶液C.溶液中溶质的质量分数变大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中的①、②分别是氟元素、钙元素在元素周期表中的信息,A、B、C、D分别是四种粒子的结构示意图。根据题中信息回答:
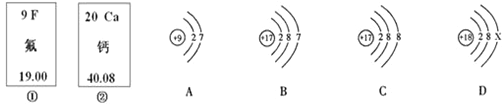
(1) 氟原子的核电荷数为____________,
(2) 钙元素的相对原子质量为________;
(3) A、B、C、D中属于同种元素的粒子是_____________(填序号);
(4) A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似_______(填序号);
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com