
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:(1)氧化铁能与足量的一氧化碳反应生成铁和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(合理即可).
(2)根据金属活动性顺序,铁能和酸反应,铜和酸不反应,故可用盐酸(或稀硫酸)除去铁,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+2HCl=FeCl2+H2↑(合理即可).
(3)要除去FeSO4溶液中的CuSO4,实质就是除去铜离子,可利用CuSO4溶液与足量的铁粉反应生成硫酸亚铁溶液和铜,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
故答案为:(1)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(合理即可);(2)Fe+2HCl=FeCl2+H2↑(合理即可);(3)Fe+CuSO4═FeSO4+Cu.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


科目:初中化学 来源: 题型:推断题
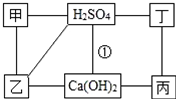 如图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.
如图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 碳元素是组成许多物质的基本元素.
碳元素是组成许多物质的基本元素.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 下列这幅卡通画形象地展现了钠与氯气反应形成氯化钠的微观过程,在此过程中,钠原子变成了钠离子.
下列这幅卡通画形象地展现了钠与氯气反应形成氯化钠的微观过程,在此过程中,钠原子变成了钠离子.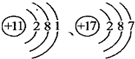
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该原子核带2个单位的正电荷 | B. | 该元素是金属元素 | ||
| C. | 该原子核外有3个电子 | D. | 该原子是一种氢原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
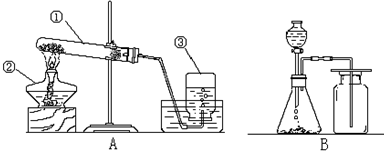
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学实验 | 取中和反应后溶液少许于试管中,向试管中滴加几滴无色酚酞溶液 | 溶液变红色 | 猜想(3)成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com