
【题目】开发利用氢能源是实现可持续发展的需要。
(1)根据图示分析,回答问题:
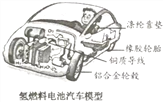

①氢燃料电池汽车模型标示的各部件中,用金属材料制成的是_________(填序号)。
A.涤纶靠垫 B.橡胶轮胎 C.铜质导线 D.铝合金轮毂
②氢燃料电池的工作原理是:将氢气送到燃料电池中,经过催化剂的作用,通过质子交换膜,再与氧气反应,同时产生电流。请写出氢燃料电池工作原理示意图中反应的化学方程式___________。
③氢气作燃料的优点是___________。
(2)工业上可通过下列工艺流程处理工厂排放的含二氧化硫的尾气并获得氢气。
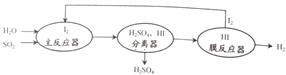
主反应器中反应的化学方程式是___________。膜反应器中反应的类型是________。该工艺流程中,能被循环利用的物质是___________。
【答案】 CD 2H2+O2 ![]() 2H2O 无污染 SO2+2H2O+I2=2HI+H2SO4 分解反应 I2
2H2O 无污染 SO2+2H2O+I2=2HI+H2SO4 分解反应 I2
【解析】根据所学知识和题中信息知,①氢燃料电池汽车模型标示的各部件中,用金属材料制成的是铜质导线和铝合金轮毂,金属材料包括金属和合金。故选CD。②氢燃料电池工作原理示意图中反应的化学方程式是2H2+O2 ![]() 2H2O。③氢气作燃料的优点是产物是水,无污染。(2) 主反应器中反应的化学方程式是SO2+2H2O+I2=2HI+H2SO4。膜反应器中反应的类型是分解反应,一种物质反应分解生成了两种物质。该工艺流程中,能被循环利用的物质是I2。
2H2O。③氢气作燃料的优点是产物是水,无污染。(2) 主反应器中反应的化学方程式是SO2+2H2O+I2=2HI+H2SO4。膜反应器中反应的类型是分解反应,一种物质反应分解生成了两种物质。该工艺流程中,能被循环利用的物质是I2。
点睛∶开发利用氢能源是实现可持续发展的需要。氢能源热值高,产物是水,对环境没有污染。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】镁在国产大飞机C-919”的制造中大显身手,小亮在实验室模拟“海水制镁”的原理来富集镁,他将25g氯化钠和氯化镁的固体混合物全部溶解于盛有70g水的烧杯中,然后向其中加入63.6g氢氧化钠溶液至恰好完全反应(图像如下),过滤,称量滤液质量为147g,求:
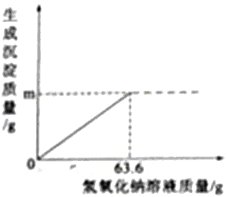
(1)图像中m=_____g。
(2)滤液中溶质的质量分数是____________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中兴缺“芯”事件震惊国人。芯片是电脑、智能家庭等的核心部件,芯片的主要成分是纯度极高的硅,其运算速率与硅的纯度有关。
(1)硅与金刚石结构相似,则构成硅的粒子是__________(填粒子名称)。
已知硅原子结构示意图为![]() 下面是四种粒子的结构示意图,其中与硅的化学性质相似的是_______(填序号)。
下面是四种粒子的结构示意图,其中与硅的化学性质相似的是_______(填序号)。
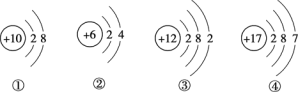
(2)光伏发电的太阳能电池板也需用高纯硅。在日光下高纯硅的作用主要是将光能转化为________能。
(3)自然界中的硅元素主要以二氧化硅的形式存在,请写出二氧化硅的化学式___。硅胶是常用的干燥剂,其主要成分可视作二氧化硅(如图),你认为硅胶可作干燥剂的原因可能是__________(一条即可)。

(4)高纯硅的制备以石英砂(主要成分是二氧化硅)为原料,生产过程示意图如下:

①上述四个步骤中属于物理变化的是_____________。
②物质M是该生产过程中可循环使用的物质,写出步骤4反应的化学方程式_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有一份氧元素质量分数为 89.5%的过氧化氢溶液,加入 MnO2 充分反应后,得到液体的 质量为 90g(不考虑操作过程中液体的损失),则生成氧气的质量为________________g(精确到小 数点后 1 位)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(一)请结合下列实验装置,回答问题:
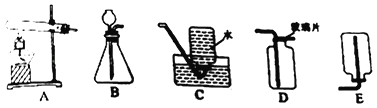
(1)以高锰酸钾为原料、利用A装置制取氧气的化学方程式为_____。
(2)用石灰石和稀盐酸制取并收集二氧化碳,选用的装置为_____(填字母)。
(3)与集气瓶配套使用的玻璃片一般一面为光滑面,另一面为磨砂面,收集气体时用玻璃片的_____盖好集气瓶(填“光滑面”或“磨砂面”)。
(二)题中制取CO2后残留的废液收集在学校实验室的废液缸中。某化学课外小组的同学想探究废液中溶质的成分,请我们共同参与探究并回答下列问题:
(1)[查阅资料]CaCl2溶液呈中性。
(2)[提出问题]废液中的溶质是什么物质?
(3)[作出猜想]猜想一:废液中的溶质只有CaCl2。
猜想二:废液中的溶质有CaCl2和_____(填化学式)。
(4)(实验与结论)①甲同学取少量CaCl2溶液和废液分别加入到2支试管中,并向其中分别滴加无色酚酞溶液做对比实验,结果两试管中溶液均无色,于是甲同学认为猜想一是正的。
②你认为甲同学的实验_____ (填“能”或“不能”)证明猜想是正确的,理由是_____。
③如果要证明猜想一是正确的,你做对比实验时选择加入的试制是_____,实验时装有废液的试管中可能观察到的现象是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铜锌合金又称假黄金。向盛有30g铜锌合金粉末样品的烧杯中逐渐加入稀硫酸,生成氢的质量与加入稀硫酸的质量关系如右图所示,计算:
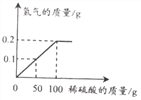
(1)充分反应后生成氢气的质量为___________g。
(2)合金样品中锌的质量为_________。
(3)恰好完全反应时,所得溶液溶质的质量分数为_________。(结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小金为探究铁制品锈蚀的条件,进行如下实验:
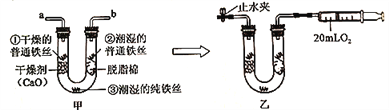
步骤1:利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好.药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器,收集20mLO2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形普内的铁丝其现象如表所示。
观察对象 | 现象 |
①干燥的普通铁丝 | 没有明显变化 |
②潮湿的普通铁丝 | 较多红褐色锈斑 |
③潮湿的纯铁丝 | 没有明显变化 |
(1)步骤1中,检查U形管内是否已充满O2的方法是_______。
(2)铁制品锈蚀的条件之一是需要 O2,在此实验中能支持此条件的证据是_____。
(3)通过对比实险现象,此实验还可得出铁制品锈蚀的条件是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某课外活动小组同学用图中装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体)。实验过程如下:
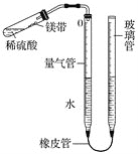
①取一段镁带样品,准确称得其质量为0.030 g;
②往量气管内装水至低于刻度“0”的位置,如图所示,(未装药品)装配好仪器;
③_________________________;
④在试管中加入足量的稀硫酸,稍倾斜试管,将用水湿润的镁带小心贴在试管壁上,塞紧橡皮塞;
⑤调整量气管液面,使两边的液面保持同一水平,记录量气管中液面位置;
⑥把试管底部略为抬高,使镁带与稀硫酸接触完全反应;
⑦待冷却至室温后,再次记录量气管中液面位置;
⑧算出量气管中增加的气体体积为23.96 mL;
已知:同温同压下,不同气体混合后体积等于混合前各气体体积之和。
请回答下列问题:
(1)写出镁与稀硫酸反应的化学方程式:____________________。
(2)能否用托盘天平称量0.030 g镁带样品________(填“能”或“不能”)。
(3)操作③是_________________________。
(4)实验过程⑦中再次记录量气管的液面位置时,试管中留有氢气,是否会影响实验最终结果________(填“是”或“否”),理由是_______________________。
(5)若实际测得氢气的体积与理论值相比偏大,则可能的原因是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com