
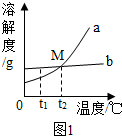
 如图1是氯化钠和硝酸钾两种固体物质的溶解度曲线
如图1是氯化钠和硝酸钾两种固体物质的溶解度曲线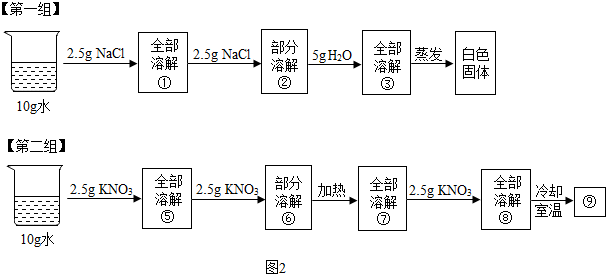
分析 根据题目信息和溶解度曲线可知:硝酸钾、氯化钠两种固体物质的溶解度,都是随温度升高而增大,而硝酸钾的溶解度随温度的升高变化比氯化钠大;图1中b表示氯化钠的溶解度曲线,因为氯化钠的溶解度受温度的影响变化不大;曲线上N点的含义是:t2℃时,NaCl和KNO3的溶解度相同;由如图2信息可知:②⑥所得溶液一定达到饱和;溶质质量分数一定相等的是①⑤.
解答 解:(1)图1中b表示氯化钠的溶解度曲线,因为氯化钠的溶解度受温度的影响变化不大;故答案为:NaCl
(2)曲线上N点的含义是:t2℃时,NaCl和KNO3的溶解度相同,②故答案为:t2℃时,NaCl和KNO3的溶解度相同
(3)由如图2信息可知:②⑥所得溶液一定达到饱和;溶质质量分数一定相等的是①⑤,故答案为:②⑥;①⑤
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.


科目:初中化学 来源: 题型:解答题
 请完成下列相关内容:
请完成下列相关内容:| 实验步骤 | 实验现象 | 实验结论 |
| ①取3.00g变质粉末于一支大试管中,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体. | 固体完全溶解, 带火星的木条复燃 | 该固体样品中含有Na2O2,其质量为1.56g. |
| ②继续向上述试管中加入足量的石灰水,充分反应. | 有白色沉淀 | 化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH. |
| ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g. | / | / |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com