
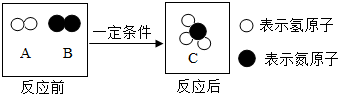
 氨气在化学工业中用途广泛,合成氨反应的微观过程如图所示:则该反应中,A与B的质量比为3:14;由该图示获得的信息还有在化学变化中分子可以再分,原子不能再分(写一条即可).
氨气在化学工业中用途广泛,合成氨反应的微观过程如图所示:则该反应中,A与B的质量比为3:14;由该图示获得的信息还有在化学变化中分子可以再分,原子不能再分(写一条即可). 分析 根据合成氨反应的微观过程如图,分析反应物、生成物和反应条件书写化学方程式,由方程式求出A与B的质量比,根据微粒的变化分析分子原子变化等.
解答 解:由合成氨反应的微观过程图可知,反应物是氢气和氮气、生成物是氨气,化学方程式为:N2+3H2$\frac{\underline{\;一定条件\;}}{\;}$2NH3,则B与A的质量比为:(14×2):(3×2)=14:3;由微粒的变化可知,在化学变化中分子可以再分,原子不能再分.
故答为:3:14;在化学变化中分子可以再分,原子不能再分.
点评 此类试题属于微观粒子模型的图示题,解答时一定要弄清各微观粒子的构成情况,并能把微观粒子与宏观物质很好的联系起来,才能根据微观粒子来推测物质的种类.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:初中化学 来源: 题型:填空题
| 组别 | 要解决的问题 | 所用方法 |
| A | 鉴别二氧化碳气体和氦气 | 用燃着的小木条 |
| B | 鉴别腈纶和羊毛 | 灼烧闻气味 |
| C | 分离食盐和硝酸钾 | 溶解过滤 |
| D | 电线着火了 | 先切断电源,再进行灭火 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验.
某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
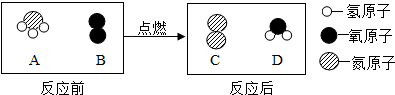
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
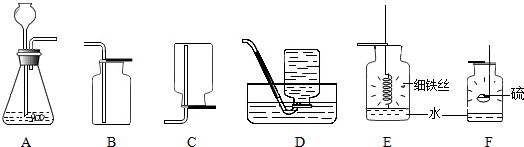
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| Ⅰ | 探究溶液的浓度对H2O2分解速率的影响 | 25℃ | 0.2gMnO2 | 10mL 4%H2O2 |
| Ⅱ | 25℃ | 0.2gMnO2 | 10mL 8%H2O2 |
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 | 实验时溶液 酸碱度 |
| Ⅰ | 探究溶液的酸碱性 对H2O2分解速率的影响 | 25℃ | 0.2gMnO2 | 0mL 8%H2O2 | pH=10.0 |
| Ⅱ | 25℃ | 0.2gMnO2 | 0mL 8%O2 | pH=4.0 |
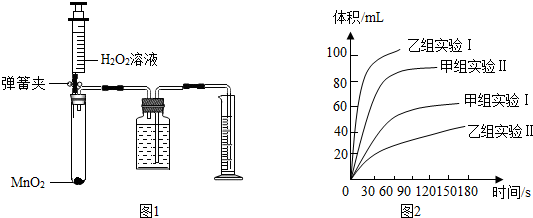
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | BaCl2、Na2CO3 | B. | KNO3、HCl | C. | Na2CO3、HCl | D. | Na2CO3、KNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 甲 | 乙 | 丙 | 丁 | 戊 | |
| 所取石灰石样品的质量/g | 22 | 22 | 22 | 22 | 22 |
| 加入盐酸的质量/g | 20 | 40 | 60 | 80 | 100 |
| 烧杯内剩余物的质量/g | 39.8 | 57.6 | 75.4 | 93.2 | 93.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com