
【题目】根据如图所示装置回答下列有关问题:
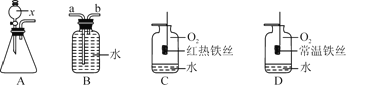
(1)仪器x的名称是____。
(2)若用装置B收集氧气,进气口应为__(填“a”或“b”)端。
(3)对比装置C和D,可以得出关于可燃物燃烧的条件是____。
(4)装置C中反应的化学方程式是_____________________
(5)在做硫燃烧时集气瓶中装入少量水的目的是__________________
科目:初中化学 来源: 题型:
【题目】某实验小组利用如下图所示装置测量空气中氧气体积分数并取得成功。
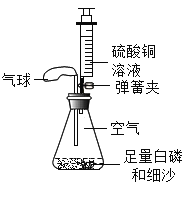
(查阅资料)白磷的着火点 40℃;硫酸铜溶液能与白磷反应,从而化解白磷的毒性。
(提出问题)氧气体积约占空气总体积的多少?
(实验准备)锥形瓶内空气体积为 230mL,注射器中硫酸铜溶液的体 积为 50mL,该装置气密性良好。
(实验探究)装入药品,按图所示连接好仪器,夹紧弹簧夹。先将锥形 瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出。
(现象分析)
(1)将锥形瓶底部放入热水中,白磷被引燃;足量的白磷在锥形瓶中未能全部燃烧,说明瓶内剩余气体_____(填“支持”或“不支持”)燃烧。
(2)在整个实验过程中,可观察到气球的变化是_____。
(3)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象:①注射器中的水 自动喷射出来,②当注射器中的水还剩约 4 mL 时停止下流。导致这些现象发生的原因是_____;______。
(得出结论)______。
(反思与评价)此装置与课本上的实验装置相比,有不少优点,请你写出一条:______。
(4)本实验装置______(填“要”或“不要”)进行气密性检查,如果需要,说出你的操 作方法:__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年春节,一首励志小诗《苔》因央视《经典咏流传》而火了起来。全诗如下:白日不到处,青春恰自来。苔花如米小,也学牡丹开。
苔藓是低级植物,多生于阴湿地方,可以为土壤涵养水源(请标出水中氢元素的化合价_____),苔藓的种类多少可以检测空气中铅、铜、锅等重金属污染物的含量( 其中铅的元素符号为_____),大多数的苔藓植物适于偏酸性的土壤(酸中的阳离子符号为_____),苔藓植物还能不断地分泌酸性物质,溶解岩石表面,慢慢形成土壤岩石中常含碳酸钙,碳酸钙中的阴离子是_____)。因此,人们常说苔藓是城市的生态保鲜剂和大自然的拓荒者。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据氧化铁(Fe2O3)的化学式计算:
(1)氧化铁的相对分子质量______。
(2)氧化铁中铁元素和氧元素的质量比______。
(3)氧化铁中铁元素的质量分数=______。
(4)320 g 氧化铁中含铁元素的质量为多少______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用下列仪器进行实验(所有装置的气密性都已检查完毕)
(1)把过氧化氢溶液缓缓加入盛有二氧化锰的容器中制取并收集氧气,完成该实验你所选用的仪器有______(填字母)。写出发生反应的表达式______。
这种方法与“把二氧化锰加入盛有过氧化氢溶液的试管中制氧气”相比有______的优点。
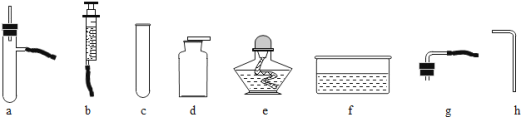
(2)科学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素。在四支试管中分别加入0.2克二氧化锰(MnO2)粉末,然后加入等量的不同溶质质量分数的过氧化氢溶液,观察气泡产生的速度,记录如下:
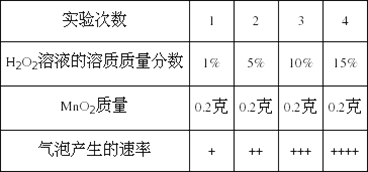
该实验研究的问题是,过氧化氢分解的速度与______的关系。
(3)某同学探究“红砖粉末是否也可以作过氧化氢分解反应的催化剂?”实验步骤和现象如下:
(4)①他分别向两支试管中加入等质量等溶质质量分数的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末(已称量出质量),然后将两支试管中的气体导出通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快
(5)②将反应较快的试管内固体过滤出来,洗涤、烘干、______.
(6)③用称量后的固体重复步骤①的实验,现象与步骤①的完全相同.
(7)试回答:步骤①中他除了选用试管外,还应用到的仪器有______(填字母);补全步骤步②的操作步骤;③的实验目的______.
(8)为了检验产生的气体是否为氧气,请你写出检验方法______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,回答问题:

(1)实验仪器的名称:① ________ ② _________
(2)实验室用高锰酸钾制氧气,反应的文字表达式为________________________,应选用的发生装置为____________(填字母序号,下同),实验时应在试管口放________,其作用是_________________________________;
(3)小明用G来排空气收集氧气,则气体从___________端进入(c或d),检验氧气收集满的操作是 __________________,保持氧气化学性质的微粒是__________,为测定高锰酸钾分解生成氧气的体积,应选用下图装置________(填编号)
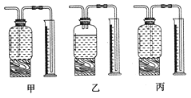
(4)小红同学在实验室制取氧气,采用了B装置,她选用的实验药品是二氧化锰和_______________,反应的文字表达式为______________________,在该反应中MnO2可以重复使用,理由是__________。
(5)氨气(NH3)的密度比空气的小,极易溶于水,实验室制取氨气的反应原理是:
氢氧化钙(固) + 氯化铵(固) ![]() 氯化钙(固)+氨气+水。
氯化钙(固)+氨气+水。
那么制取并收集氨气应选用上面的_________(填字母序号)(从A至F中选)
(6)实验室在常温下用块状电石与水反应制取不易溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是_______(填字母)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明、小强和小峰在学习了“质量守恒定律”后来到化学实验室亲自进行了实验探究,如图是他们分别设计的实验,请你与他们一起进行探究,并回答问题.

实验1:称量镁条,点燃,待反应结束后,再称量.
实验2:将盛有稀盐酸的小试管放入盛有锌粒的烧杯中称量,然后使稀盐酸与锌粒接触,充分反应后再称量.
实验3:将盛有氢氧化钠溶液的小试管放入盛有硫酸铜溶液的锥形瓶中称量,然后使氢氧化钠溶液与硫酸铜溶液混合,充分反应后再称量.
数据见下表:(锌与盐酸反应:Zn+2HCl=ZnCl2+H2↑;氢氧化钠溶液与硫酸铜溶液反应:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4)
编号 | 实验1 | 实验2 | 实验3 |
反应前称量质量 | 9.6g | 212.6g | 118.4g |
反应后称量质量 | 16.0g | 212.4g | 118.4g |
(1)写出实验1反应的化学方程式_____.
(2)上述三个反应_____(填“符合”或“不符合”)质量守恒定律,实验_____正确反映了反应物与生成物的质量关系.
(3)由上述实验我们得到启示,探究_____的反应验证质量守恒定律,实验必须在密闭的装置中进行.
(4)由质量守恒定律可知,化学反应前后,一定不变的是_____(填序号).
①物质种类②元素种类③原子种类④分子种类⑤分子数目⑥原子数目.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各组物质,能相互反应且反应前后溶液总质量增加的是( )
A. 氯化钡溶液和稀硫酸 B. 硝酸钾溶液和硫酸镁溶液
C. 碳酸钠固体和稀盐酸 D. 铁和硫酸铜溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定质量的氯酸钾和二氧化锰固体混合物受热过程中,某变量y随加热时间的变化趋势,如右图所示,纵坐标(y)表示的是( )
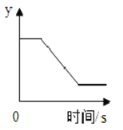
A. 生成氧气的质量
B. 固体中二氧化锰的质量
C. 试管内剩余固体的质量
D. 反应的速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com