
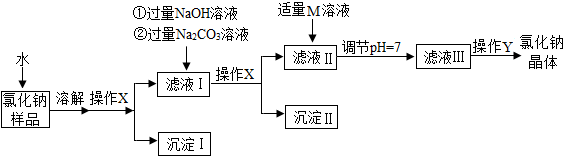
分析 根据镁离子用氢氧根离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子进行分析;利用溶质的质量=溶液质量×溶液中溶质的质量分数;根据溶液中溶质质量=溶液质量×溶液的质量分数,利用加水稀释前后溶液中溶质质量不变解答.
解答 解:因为镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀;钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,故除掉少量的CaCl2和MgCl2以及不溶性杂质,根据流程图,可知:
(1)操作X,分离可溶物和不溶物,此名称是过滤,过滤操作中用到的玻璃仪器有:烧杯、漏斗、玻璃棒;
(2)加入氢氧化钠和氯化镁会生成氢氧化镁沉淀,可除去的阳离子是Mg2+,反应的化学方程式为:2NaOH+MgCl2═Mg(OH)2↓+2NaCl;
(3)加入碳酸钠和氯化钙会生成碳酸钙沉淀,目的是除去滤液中的CaCl2,反应的化学方程式是:CaCl2+Na2CO3=2NaCl+CaCO3↓;
(4)滤液Ⅱ中含有氯化钠、氢氧化钠、碳酸钠,则为了除掉氢氧化钠、碳酸钠,需要加入的Y溶液为稀盐酸,故其中溶质的化学式是HCl;
(5)操作Y是蒸发,玻璃棒的作用是搅拌,防止局部过热造成液滴飞溅.
(6)100kg16%的氯化钠溶液中含溶质氯化钠的质量=100kg×16%=16kg;
取50g该溶液稀释成质量分数为8%的氯化钠溶液,设需加水质量为x,
50g×16%=(50g+x)×8%
解得x=50g,
配制时,需用到的玻璃仪器有烧杯、滴管、玻璃棒、量筒
应填写:16;50;量筒.
故答案为:
(1)漏斗;
(2)Mg2+;2NaOH+MgCl2═Mg(OH)2↓+2NaCl;
(3)除去滤液中的CaCl2 (或Ca2+);Na2CO3+CaCl2═CaCO3↓+2NaCl;
(4)HCl;
(5)搅拌,防止局部过热造成液滴飞溅;
(6)16;50;量筒.
点评 本题主要考查选择试剂、化学方程式的写法及蒸发操作,完成此题,可以依据物质的性质进行.


 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
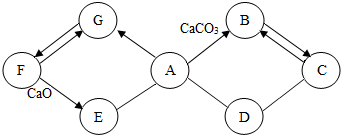 如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是最轻的气体,B和C含有相同的元素.
如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是最轻的气体,B和C含有相同的元素.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 溶液间进行的反应 | 甲+丙 | 甲+乙 | 乙+丁 | 丙+丁 |
| 实验现象 | 有气体产生 | 有沉淀产生 | 有沉淀产生 |
| A. | 一定有气体 | B. | 一定有沉淀 | ||
| C. | 可能有反应但无现象 | D. | 可能没有反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
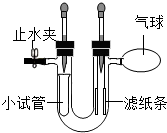 兴趣小组根据老师提供的实验装置进行如下实验,U型管左侧管内固定一小试管,右侧管内挂的是紫色石蕊试液浸泡过的滤纸条,其中一条是湿润的,一条是干燥的.
兴趣小组根据老师提供的实验装置进行如下实验,U型管左侧管内固定一小试管,右侧管内挂的是紫色石蕊试液浸泡过的滤纸条,其中一条是湿润的,一条是干燥的.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com