
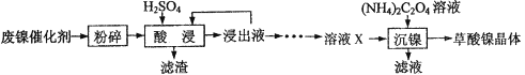
【题目】草酸镍晶体(NiC2O4·2H2O)可用于制镍催化剂。某小组用废镍催化剂(成分为Fe2O3、Ni、Fe、SiO2等)制备草酸镍晶体的部分实验流程如下:
已知:①Ni能和稀H2SO4反应。
②相关金属离子生成氢氧化物沉淀的pH如下表:
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Ni2+ | 6.7 | 9.5 |
③H2O2能将Fe2+氧化为Fe3+
(1)废镍催化剂“粉碎”的目的是______。
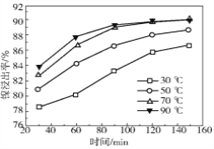
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图,“酸浸”的适宜温度与时间分别为 _______(填字母)。
A.30℃、30min B.90℃、150min C.70℃、120min D.90℃、120min
(3)“酸浸”中发生的复分解反应方程式为________。
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是_____(填字母)。
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液
加NaOH溶液调节pH_____(填范围),充分反应后得到滤渣的操作是______,该操作中所用到的玻璃仪器有玻璃棒、烧杯和_________。
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、_____ 、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体。
②用75%乙醇洗涤的目的是洗去杂质、___________;
③烘干温度不超过110℃的原因是______。
【答案】 增大与硫酸的接触面积,加快反应速率,充分反应 C Fe2O3 + 3H2SO4 ===Fe2(SO4)3 + 3H2O A 3.2≤pH<6.7(或3.2~6.7) 过滤 漏斗 降温结晶 减少草酸镍晶体的损失 防止草酸镍失去结晶水
【解析】(1)把废镍催化剂粉碎,增大了反应的接触面积,加快反应速率,提高镍的浸出率;
(2)根据镍浸出率随时间变化图可知,70℃时,镍浸出率很大,从时间看,120min时镍浸出率已经很高,再延长时间对镍浸出率没有实质性提高,选择70℃和120min为宜;
(3)废镍催化剂成分为Fe2O3、Ni、Fe、SiO2等,其中Ni、Fe与硫酸发生置换反应,SiO2与硫酸不反应,Fe2O3与硫酸反应生成硫酸铁和水,属于复分解反应方程式为Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O;
(4)“浸出液”得到“溶液x”过程中,要出去铁离子和亚铁离子,所以先加H2O2溶液,将亚铁离子转化为铁离子,再加NaOH溶液除去,要出去铁离子,并且保留镍离子,调节溶液3.2≤pH≤6.7,将固体和液体分开需要过滤操作,所用到的玻璃仪器有玻璃棒、烧杯和漏斗;
(5)①“沉镍”时蒸发浓缩、降温结晶、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体。
②“沉镍”工序生成了(NH4)2SO4,用乙醇洗涤,能洗去(NH4)2SO4的水水溶液、便于烘干,减少草酸镍晶体的损失;
③烘干温度不超过110℃,如果温度过高,草酸镍晶体会失去结晶水。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:初中化学 来源: 题型:
【题目】保险粉(化学式Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定;在NaCl存在下,Na2S2O4在水中溶解度显著下降。Na2S2O4制备流程如下:(已知:常温下Zn(OH)2的溶解度为1.42×105g)
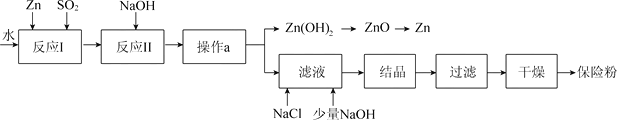
(1)反应I的原理为:Zn+2SO2===ZnS2O4,该反应的基本类型为___________。
(2)反应II为复分解反应,该反应的化学方程式为_________________________________。
(3)操作a的名称为__________。
(4)滤液中含有Na2S2O4,为使Na2S2O4结晶析出加入NaCl的原因是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】世界环境日为每年的6月5日,它反映了世界各国人民对环境问题的认识和态度,表达了人类对美好环境的向往和追求。下面做法不正确的是()
A. 减少使用塑料袋,减少白色污染 B. 推广使用太阳能、风能,缓解温室效应
C. 讲卫生,尽量多使用一次性餐具 D. 短时间不使用电脑,将其转为休眠模式
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取一定质量的石灰石(所含杂质不溶于水,不与酸反应,高温也不分解),高温煅烧一段时间后,将所得固体与200 g溶质质量分数为14.6%的稀盐酸充分反应,过滤得到10 g滤渣和一定质量的中性溶液,则原石灰石中碳酸钙的质量分数是
A. 80.0% B. 83.8% C. 74.4% D. 92.6%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生活密切相关。
Ⅰ.小明妈妈准备露营的食物。
(1)下列食物中富含糖类的是______(填序号)。
A. 青菜 B. 鱼肉 C. 牛奶 D. 大米
(2)牛奶中还含有维持人体正常生理功能所必需的磷、硒、钙、钠、镁、铁、锌、铜、锰、钾等元素,其中能够防止人体骨质疏松的元素是 ____(填元素符号)。
Ⅱ.小明一家与朋友们决定使用“共享汽车”出行。
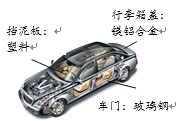
(1)①“共享汽车”中属于金属材料的是____(填材料名称,下同),属于合成材料的是____,属于复合材料的是____。
②将镁铝合金与铝片相互刻画,在铝片表面留下明显划痕,说明镁铝合金的硬度____铝的硬度(填“大于”或“小于”)。
(2)使用“共享汽车”出行出行的好处有______(填序号)
A.降低出行成本 B.减少汽车尾气排放 C.节约能源 D.降低交通压力
(3)“共享汽车”使用天然气作为燃料。“天然气水合物”即为“可燃冰”,它是在海底的高压、低温条件下形成的,外观像冰。1体积“可燃冰”可贮载100~200体积的天然气。下面关于“可燃冰”的叙述不正确的是______(填序号)
A.“可燃冰”有可能成为人类未来的重要能源 B.“可燃冰”是一种比较洁净的能源
C.“可燃冰”提供了水可能变成油的例证 D.“可燃冰”的主要可燃成分是甲烷
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将一定量的锌粉和铁粉加入到硝酸铜溶液中,充分反应后,过滤,向滤出的固体中加入稀盐酸,有气泡产生,则滤出的固体中一定含有_______(化学式表示),滤液中的溶质一定含有____________(化学式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为A、B、C三种固体物质的溶解度曲线,请回答下列问题。
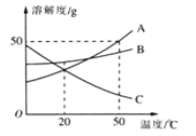
(1)20℃时,三种物质的溶解度大小关系为______。
(2)50℃时,150g A的饱和溶液中,含A____g。
(3)将C的饱和溶液变为不饱和溶液可采用的一种方法是_____。
(4)50℃时,将A、B、C三种物质的饱和溶液分别降温到20℃,溶质的质量分数变化最大的是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语表示:
(1)2个镁离子_______________;(2)氢氧化亚铁______________;
(3)保持二氧化硫的化学性质的最小粒子_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学利用如图装置探究铁与氧化铁化合的生成物成分。
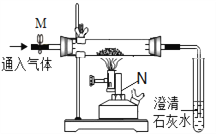
【认识仪器】由仪器N可知该反应的条件是_____________。
【查阅资料】铁的氧化物中只有Fe3O4能被磁铁吸引。
某些铁的氧化物加热时能与氧气反应。
【提出猜想】猜想①是FeO;
猜想②是Fe3O4;
猜想③是FeO和Fe3O4混合物。
【实验步骤】
①连接组装仪器,检查装置的气密性,方法是:关闭弹簧夹M,_________________________________________________________。
②称取16.0g氧化铁粉末与质量为m的铁粉,均匀混合后,放入玻璃管。
③通入CO2,当观察到明显现象时,夹上弹簧夹M,开始加热玻璃管。
④当固体全部呈黑色后,停止加热,______________________________________。将玻璃管中黑色粉末倒在滤纸上,取样,滴加稀盐酸,无气泡产生,用磁铁吸引,粉末被部分吸引。
【实验结论】猜想_________成立。所加铁粉质量m的范围是_________________。
【问题讨论】实验中澄清石灰水的主要作用是______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com