
【题目】某化学兴趣小组为探究化学反应中的能量变化,进行如下实验:
探究一:盐酸与氢氧化钠的反应
(1)甲同学设计实验:向一定量氢氧化钠固体中加入20mL4%盐酸,用温度计反应后溶液温度升高,得出中和反应放热。乙同学认为该实验方案不合理,其理由是_____。
(2)丙同学设计了如下三组实验,请你帮助他完成实验方案:
实验编号 | 实验方案 |
实验1 | 向20mL4%盐酸中加入20mL水,测定稀释前后溶液的温度。 |
实验2 | 向20mL5%氢氧化钠溶液中_____,测定稀释前后溶液的温度。 |
实验3 | _____ |
(3)丙同学观察到的实验现象是:实验3溶液升高的温度远大于实验1与实验2溶液升高的温度之和,由此你能得出的实验结论是_____。
探究二:盐酸与碳酸氢钠溶液的反应
下图是丁同学在20、基本隔热条件下利用温度传感器,绘制分别向20mL水和20mL饱和碳酸氢钠溶液中各加入20mL13.7%盐酸的温度与时间的变化曲线图。实验测得饱和碳酸氢钠溶液稀释时温度变化不大,可忽略不计。据此回答下列问题:

曲线①:水+盐酸的温度变化曲线;曲线②:饱和碳酸氢钠溶液+盐酸的温度变化曲线
(4)26秒后,曲线①逐渐下降的主要原因是_____。
(5)曲线②反应的化学方程式是_____。
(6)比较曲线①和曲线②,你认为13.7%盐酸与饱和碳酸氢钠溶液的反应是_____(填“放热”或“吸热”)反应,其理由是_____。
【答案】氢氧化钠固体溶于水,温度也升高 倒入20mL水 把20mL4%盐酸和20mL5%氢氧化钠溶液混合,测定混合后溶液的温度 ①氢氧化钠与盐酸能发生化学反应;②氢氧化钠与盐酸是放热反应,温度升高 盐酸的浓度很稀,不再放热 NaHCO3+HCl=NaCl+H2O+CO2↑ 放热 温度升高
【解析】
(1)乙同学认为该实验方案不合理,其理由是:氢氧化钠固体溶于水,温度也升高;故填:氢氧化钠固体溶于水,温度也升高;
(2)实验2:向20mL5%氢氧化钠溶液中倒入20mL水,测定稀释前后溶液的温度;实验3:把20mL4%盐酸和20mL5%氢氧化钠溶液混合,测定混合后溶液的温度;故填:倒入20mL水;把20mL4%盐酸和20mL5%氢氧化钠溶液混合,测定混合后溶液的温度;
(3)丙同学观察到的实验现象是:实验3溶液升高的温度远大于实验1与实验2溶液升高的温度之和,由此能得出的实验结论是:①氢氧化钠与盐酸能发生化学反应;②氢氧化钠与盐酸反应时,温度升高;故填:①氢氧化钠与盐酸能发生化学反应;②氢氧化钠与盐酸是放热反应,温度升高;
(4)26.0秒后,曲线①逐渐下降的原因是:盐酸的浓度很稀,不再放热;故填:盐酸的浓度很稀,不再放热;
(5)由题意可知曲线②是饱和碳酸氢钠溶液和盐酸的反应,反应生成氯化钠和水和二氧化碳,反应的化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑,故填NaHCO3+HCl=NaCl+H2O+CO2↑;
(6)比较曲线①和曲线②,我认为13.7%盐酸与饱和碳酸氢钠溶液的反应是放热反应,其理由是:温度升高;故填:放热;温度升高。


科目:初中化学 来源: 题型:
【题目】某化学兴趣小组为了分析生铁中铁的含量,进行了实验研究,即取60g经粉碎后的生铁,把800稀硫酸分4次加入到该样品中,测得数据记录如下表:
第1次 | 第2次 | 第3次 | 第4次 | |
加入稀硫酸质量(g) | 200 | 200 | 200 | 200 |
剩余固体质量(g) | 37.6 | 15.2 | 4 | 4 |
(说明:生铁中杂质不溶于水,也不与硫酸反应.)
(1)第2次测得剩余固体质量为15.2g,其成分为_____.
A 铁 B 铁和碳 C 碳
(2)生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)_____
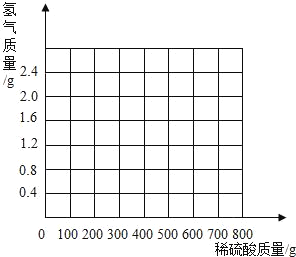
(3)计算所用稀硫酸的溶质质量分数为多少?_____(写出计算过程,结果保留到小数点后一位)并画出反应生成的氢气质量与加入稀硫酸质量的关系图._____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图:
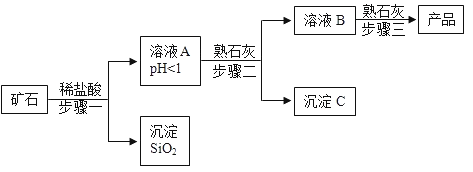
(1)请写出步骤一中发生反应的化学方程式: (任写一个)
(2)溶液A中所含的阳离子有 (填离子符号)
(3)已知:部分金属阳离子以氢氧化物形成沉淀时溶液的pH见表
沉淀物 | Fe(OH)2 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.9 | 4.2 | 9.1 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
步骤二中加入熟石灰,调节溶液的pH范围为
(4)3个步骤中均用到的操作是
(5)步骤三中生成产品的化学方程式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生活息息相关,请回答下列问题:
(1)“风吹柳花满店香”说明粒子具有_____的性质;
(2)冬季烧煤取暖时需做好尾气排放,因为碳在氧气不充足时燃烧会生成_____(填名称);
(3)检验人体呼出的气体中是否含有CO2气体用_____(填名称),发生的化学反应方程式为_____;
(4)生活中可以用双氧水处理伤口,杀灭厌氧细菌,其反应原理是血液中的酶可以加快过氧化氢的分解,请你写出该反应的化学方程式_____;
(5)医学上在治疗一些皮肤病时常用一种叫“PP粉”的暗紫色固体溶于水来清洗皮肤,这种药品也可以用于实验室制氧气,写出其反应方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室常见的装置。
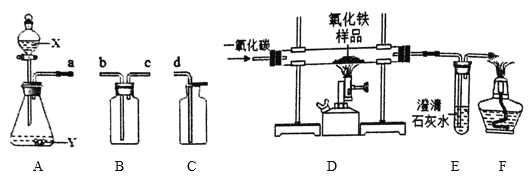
(1)写出A装置中任一仪器的用途:_____。
(2)若用A装置制取氧气,则A中发生反应的化学方程式为_____;若用装满水的B装置收集氧气,a端应与_____(选填“b”或“c”)端相连。
(3)若用ABC装置制取并收集一瓶干燥CO2,则试剂X的名称是_____,B装置中盛放适量的浓硫酸,导管的连接顺序为a→_____→_____→d。
(4)利用DEF装置测定某不纯氧化铁样品的纯度(杂质不参与反应),并验证气体生成物的性质。
①装置F的作用是_____。
②若氧化铁样品质量为20g,反应后D装置的质量减少4.8g,则该样品中氧化铁的纯度为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是医院常用的药瓶和注射器,请你据图回答:

(1)含有金属材料的是 (写一种即可,下同),属于有机合成材料是 .
(2)注射器洗净后可以用于家庭小实验,可以代替 仪器使用.
(3)钢针一般用不锈钢制造,主要是由于其不容易生锈,请你写出生活中防止铁制品生锈的方法(一条即可) .
(4)铝的金属活性比铁强,请写出铝放入硫酸亚铁溶液中反应的化学方程式 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上利用黄铁矿(主要成分是FeS2)生产硫酸。同时还能得到一种副产品氧化铁用于炼铁,其反应原理如下:
①4FeS2+11O2![]() 2Fe2O3+8SO2 ②2SO2+O2
2Fe2O3+8SO2 ②2SO2+O2 2SO3
2SO3
③SO3+H2O=H2SO4 ④ Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
下列说法不正确的是
A. 反应①②④均是在高温条件下进行的
B. 只有①②发生的是氧化反应
C. 反应②③属于化合反应
D. 反应①④不属于四种基本反应类型中的任何一种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a,b两种物质的溶解度曲线如图所示。下列说法正确的是( )
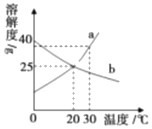
A. 20℃时,a,b溶液的溶质质量分数一定相等
B. 30℃时,a的饱和溶液溶质质量一定等于140g
C. 20℃时,a、b两种物质的溶解度相等
D. 将30℃时a,b的饱和溶液都降温到20℃,所得溶液溶质质量分数相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com