
【题目】某实验小组模拟高炉炼铁的化学反应原理设计了用一氧化碳还原氧化铁的实验装置,如图所示:
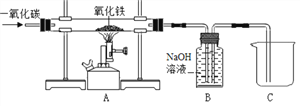
(提出问题)(1)实验所用的氧化铁完全反应后,玻璃管中剩余的黑色固体成分。
(2)反应后由B装置排到烧杯C中的溶液所含溶质的成分。
(查阅资料)
常见铁和铁的氧化物 | Fe | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 能 | 否 | 否 | 能 |
(探究1)玻璃管中剩余的黑色固体成分。
(初步验证)玻璃管中剩余固体为黑色,能全部被磁铁吸引。
实验小组的同学一致认为,黑色固体不可能是FeO和Fe2O3,理由是______。
(作出猜想)黑色固体可能:a.全部是Fe;b.全部是Fe3O4;c._______。
(设计实验)为确定黑色固体的成分,同学们设计了下列实验方案,请你一起参与探究活动。
实验操作 | 实验现象 | 实验结论 |
取少量黑色固体于试管中,加入_______ | ______ | 黑色固体全部是Fe3O4 |
(探究2)反应后由B装置排到烧杯C中的溶液所含溶质的成分。写出B装置中NaOH发生反应的化学方程式:_______
(作出猜想)猜想一:溶质是Na2CO3;猜想二:溶质是_______;
(设计实验)
实验操作 | 实验现象 | 实验结论 |
(1)取少量溶液于试管中,加入__________; | 产生白色沉淀 | 该反应的化学方程式为__________ |
(2)将(1)反应后的混合物过滤,取滤液加入________ | ___________ | 猜想一成立 |
(反思与交流)(1)B装置除了吸收CO2气体外,还有的作用是______;
(2)为了避免加热玻璃管时可能发生爆炸,在加热前应________。
【答案】 FeO、Fe2O3不能被磁铁吸引 Fe和Fe3O4的混合物 稀盐酸/稀硫酸 没有气泡产生 CO2+2NaOH=Na2CO3+H2O NaOH和Na2CO3 过量的CaCl2溶液 CaCl2+Na2CO3=CaCO3↓+2NaCl 无色酚酞试液 溶液不变红 收集多余的CO,防止污染大气 先通CO,排尽装置内的空气
【解析】本题考查了一氧化碳还原氧化铁后剩余固体成份的探究,金属、碱、盐的性质。掌握铁和铁的氧化物的性质以及尾气的处理等知识点是解答的基础。
探究1:初步验证:根据表格中信息可知FeO和Fe2O3不能被磁铁吸引,实验中黑色粉末能被磁铁全部吸引,说明不含这两种物质;
作出猜想:根据剩余固体可能是铁出可能是四氧化三铁,还可能是二者的混合物,所以猜想c是Fe和Fe3O4的混合物;
设计实验:若黑色固体全部是Fe3O4,黑色固体中没有铁,加入稀盐酸(或稀硫酸)没有气泡产生;
探究2:一氧化碳与氧化铁在高温条件下生成铁与二氧化碳。氢氧化钠溶液与二氧化碳反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O;
作出猜想:氢氧化钠溶液与二氧化碳反应生成碳酸钠和水。如完全反应溶液中的溶质只有Na2CO3,氢氧化钠溶液如没有完全反应,则溶液中的溶质有NaOH和Na2CO3两种,所以猜想二的溶质是NaOH和Na2CO3;
设计实验:碳酸钠能和氯化钙反应生成白色沉淀,反应后溶液显中性;如加入氯化钙后溶液仍显碱性,说明原溶液中除了碳酸钠溶质外还含有氢氧化钠,检验溶液显碱性常用无色酚酞溶液,能使无色酚酞溶液变红,说明溶液显碱性;因此:
实验操作 | 实验现象 | 实验结论 |
(1)取少量溶液于试管中,加入过量的CaCl2溶液; | 产生白色沉淀 | 该反应的化学方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl |
(2)将(1)反应后的混合物过滤,取滤液加入无色酚酞试液 | 溶液不变红 | 猜想一成立 |
反思与交流:(1)根据尾气中除了二氧化碳外还有一氧化碳,要进行处理,所以装置B除了吸收二氧化碳外还有收集多余的CO,防止污染大气;
(2)一氧化碳与空气混合有发生爆炸的危险,实验前要先通CO,排尽装置内的空气再进行加热。


 智能训练练测考系列答案
智能训练练测考系列答案科目:初中化学 来源: 题型:
【题目】下列图像分别与选项中的操作相对应,合理的是
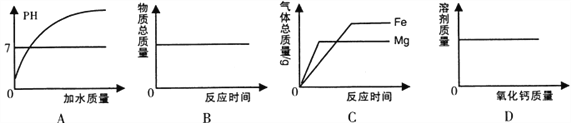
A. 向一定质量的稀盐酸中加水
B. 一定条件下,一定质量的碳和氧气在密闭容器中反应
C. 等质量的镁和铁分别与足量的稀硫酸反应
D. 一定温度下,向一定质量的饱和石灰水中加入氧化钙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)为了测定石灰石中碳酸钙的质量分数,某兴趣小组的同学称取石灰石样品12.5g,高温煅烧至质量不再改变,称得剩余固体质量为8.1g(假设杂质不参加反应;发生反应的化学方程式为CaCO3![]() CaO+CO2↑ ),试计算:
CaO+CO2↑ ),试计算:
(1)生成二氧化碳质量是__________g;
(2)石灰石样品中碳酸钙的质量分数是多少?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D四种化合物分别通过分解反应生成两种物质,如下所示(反应条件略去):① A → B + M ② B → M + N ③ C → M + P ④ D → M + Q在生成物中N被认为是最清洁的燃料,P是常温下为液态的金属,Q的水溶液跟硝酸银溶液反应生成一种不溶于稀硝酸的白色沉淀,试推断(用化学式表示):
(1)A是_____________B是 _____________ C是 _____________ D是 __________
(2)写出②对应的化学方程式______________________________
写出Q的水溶液跟硝酸银溶液反应的化学方程式______________反应类型______________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取一滤纸条,等间距滴10滴紫色石蕊试液,然后装入玻璃管中(如图),两端管口同时放入分别蘸有浓氨水和浓盐酸的棉球,几秒后观察到图示现象。下列结论不正确的是
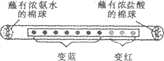
A. 氨水的pH大于7 B. 酸、碱溶液能使酸碱指示剂显示不同颜色
C. 氨分子和氯化氢分子在不断运动 D. 气体相对分子质量越小,运动速率越慢
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年入冬以来,我国北方大部分地区遭遇几十年未见的特大旱灾,缓解灾情,有些地区使用了干冰进行人工增雨,但二氧化碳也是温室效应的元凶之一因此,有科学家设想:将排放到空气中的二氧化碳压缩使其液化,然后将其压入到冰的深海中,但也有科学家担心海水中富含二氧化碳后酸度会增加,可能会杀死一些海生物,甚至会溶解掉部分海床,从而造成灾难性的后果。
(1)为减少二氧化碳这种温室气体的排放,我们可以采取的措施有:_____。(写一种即可)
(2)二氧化碳使海水酸度增加的原理用化学方程式表示为:_____;
(3)能用来鉴别CO和CO2的方法是_____(不定项选择)。
A.通入紫色石蕊试液 B.通入澄清石灰水 C.闻气味
(4)为减少大气中二氧化碳含量,将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷(CH4)这个反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某氢氧化钠固体样品,可能含有固体氢氧化钾和不溶于酸的杂质A,取5.6g该样品与100g一定质量分数的稀盐酸反应,两者恰好完全反应,生成mg水。下列说法正确的是
A. 若样品不含任何杂质,则m < 1.8
B. 若m =1.8,则样品中一定含有杂质A,可能含有固体氢氧化钾
C. 若m =1.8,则样品中至少含有杂质A或固体氢氧化钾中的一种
D. 若样品中既含有A,也含有固体氢氧化钾,则一定m > 1.8
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组欲从高锰酸钾制氧气剩余物中回收副产物,设计了如图所示实验方案:
【资料卡片】
①KMnO4能和纤维素反应。,在中性溶液中比较稳定,加热碱性条件中的KMnO4溶液会有部分KMnO4和H2O反应,生成MnO2;
②锰酸钾溶于水为墨绿色,不稳定,在水溶液中能全部转化为KMnO4、MnO2和KOH,反应的化学方程式如下:3K2MnO4+2H2O==2KMnO4和+MnO2↓+4KOH
【实验方案】

(1)将剩余物加入水中,观察到的现象是:①部分固体溶解;②有少量不溶物出现;③____________。
(2)回收物甲是____________________(填化学式)。
(3)静置后过滤时,发现滤液浑浊,在操作均正确的情况下(过滤前滤纸完好无损),原因是_______。
(4)滤液B中一定含有的溶质是KMnO4和_______________,需要加入少量硫酸进行中和,中和反应的化学方程式是____________________________________。
(5)冷却结晶后,低温烘干高锰酸钾晶体是为了防止_____________________。
(6)加热31.6gKMnO4使之完全分解,按以上实验方案可得回收物甲的质量可能是________。
A.8.7g B.11.5g C.12.8g D.28.4g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某不锈钢锅问题已经发生了几个月,炊具材料中锰含量不得超过2%。锰对人体的神经系统危害是相当大的,过量会导致锰狂症,进一步可以出现类似于帕金森综合症。如图是元素周期表中的锰的有关信息,其中认识错误的是( )
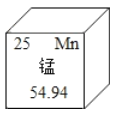
A. 锰原子的质子数为25 B. 锰元素属于金属元素
C. 锰原子的原子核外有25个电子 D. 锰的原子质量为54.94
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com