
【题目】人体缺碘会引起甲状腺肿大,幼儿缺碘影响生长发育,造成思维迟钝。食盐中通常加入一定量的碘酸钾(KIO3),补充人体需要的碘元素。结合图中信息判断,下列叙述中正确的是 ( )
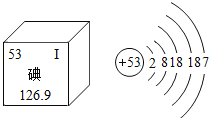
A. 碘是人体必需的微量元素,摄入越多越好B. 碘离子(I-)的核外电子数为54
C. 碘的相对原子质量是126.9 gD. 碘元素属于金属元素
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:初中化学 来源: 题型:
【题目】已知硝酸盐易溶于水。对于反应:![]() ,下列分析中正确的是( )
,下列分析中正确的是( )
A.该反应类型可能是中和反应B.X和Y的相对分子质量之差为18
C.X可能是单质,也可能是化合物D.Y可能是![]() 或
或![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列各图中有关信息,回答下列问题:
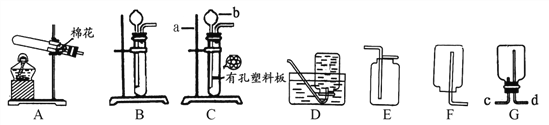
(1)仪器a、b的名称:a________,b________。
(2)若用装置A制取氧气,其反应的化学方程式_______________。若要收集到较纯净的氧气,其收集装置应选____;待收集完毕后应先_______,再________________。 某同学用收集好的氧气做铁丝燃烧实验时发现集气瓶炸裂,原因可能是_________。
(3)实验制取CO2,为了控制反应的发生与停止,选择最佳的发生装置是___________;若用G装置收集CO2气体,气体应从________端(填“c”或“d”)进入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)豆腐是生活中常见的食品,主要成分如图所示。

(1)图中所列成分,从营养角度看,共分为_______类。
(2)除豆腐外,很多食物也能提供丰富的蛋白质。下列能提供丰富蛋白质的食品是 (填字母序号)。

(3)豆腐可以补充人体每天所需的钙元素,缺钙会导致的疾病是 (填字母序号)。
A.贫血 B.龋齿 C.骨质疏松
(4)家庭制作豆腐主要有以下的过程:①打豆浆;②将豆浆与豆渣分离;③点卤;④将豆腐花与水分离;⑤压制成块。②和④中的两次分离采取的操作是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用闪锌矿(主要含ZnS,还含PbS等杂质)制备锌的流程如下(部分产物略去):
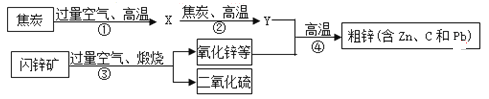
(1)X的化学式是_______,图中用过量空气的目的是_________。
(2)①~④中属于化合反应的是______。
(3)Zn______(填“能”或“不能)与PbCl2溶液反应。
(4)写出反应③中生成ZnO的化学方程式_________。
(5)结合下表数据设计:从粗锌中分离出纯锌的方案是_________。
物质 | Zn | Pb | C |
沸点℃ | 907 | 1749 | 4827 |
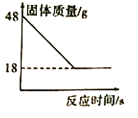
(6)反应②中固体质量随反应时间的变化图示如下图,计算产生Y的质量__________。(写出必要的计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】随着环境问题的日益严重,垃圾的处理问题正日益被人们所重视。某垃圾处理厂对金属垃圾(主要成分是铁、铜、氧化铁、二氧化硅)处理及综合利用的部分工艺如图所示。请回答下列问题:
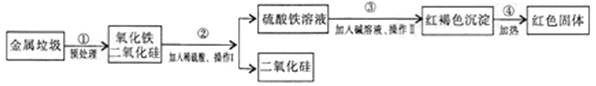
(1)I、II均为______操作,此操作中玻璃棒的作用是搅拌、______;
(2)步骤③所发生的反应属于基本反应类型中的___________;
(3)请写出步骤②、④所发生反应的化学方程式:
② ___________;④____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸(HNO3)是实验室常见的一种酸,实验小组对硝酸的某些性质进行研究。
I.挥发性
(实验1)取一瓶质量分数68%的浓硝酸,打开瓶盖,遇潮湿的空气,瓶口可以看到__________。
II.不稳定性
(查阅资料1)硝酸是无色液体,见光或受热分解生成红棕色的NO2气体。
(1)硝酸分解的化学方程式为:4HNO3![]() 4NO2↑+O2↑+___。
4NO2↑+O2↑+___。
(实验2)取3份浓度和体积均相同的浓硝酸分别放入3支试管中,塞好塞子,放置在室外阳光充足的地方(气温为26 ℃)。记录溶液上方的气体颜色随时间的变化情况。
实验编号 | ① | ② | ③ |
实验条件 |
|
|
|
实验现象 | 6分钟出现浅红棕色 15分钟红棕色比较明显 30分钟红棕色非常明显 | 60分钟无明显变化 | 3分钟出现浅红棕色 6分钟红棕色比较明显 10分钟红棕色非常明显 |
(2)实验①、②对比是研究对浓硝酸稳定性的影响__________________________________。
(3)实验①、③对比可得出的结论是__________________________________________。
III.酸性
(查阅资料2)硝酸能够与金属氧化物反应生成盐和水。
(实验3)向氧化铜粉末中加入硝酸,能够观察到的现象是_________________________。
IV.氧化性
(查阅资料3)浓硝酸在加热条件下能与木炭发生反应。C+4HNO3(浓)![]() 4NO2↑+ CO2↑+2H2O
4NO2↑+ CO2↑+2H2O
(实验4)如图所示,将红热的木炭伸到浓硝酸上方,观察到有红棕色气体产生。请解释生成该红棕色气体的原因可能有:
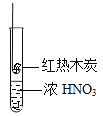
①___________________________________________________。
②___________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】1949 年 10 月 1 日中华人民共和国成立,在开国大典上首次实现了电动升国旗。 为保证国旗不被卷入,要求旗杆上的“阻断球”要足够结实,不易被撞裂。在“阻断球” 的制作过程中不仅使用了铁,还熔入了一定比例的铬(Cr)等金属,这是利用了合金_____的性质。在常见金属活动性顺序中没有铬,同学们决定对铬与常见金属镁和铜的活动性强弱进行探究。
(查阅资料)铬(Cr)是一种银白色金属,其化合物硫酸亚铬(CrSO4)的水溶液呈蓝色。硫酸亚铬中铬元素的化合价为_____。
(提出猜想)三种金属的活动性强弱为:
猜想一:Cr>Mg>Cu; 猜想二:_____;猜想三:Mg>Cu>Cr
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
①分别向盛有 Cr 和 Cu 两种金属片的试管中加入同体积同浓度的稀硫酸 | 只有盛_____的试管中有气泡产生,并得到蓝色溶液 | 猜想三错误 |
②向盛有硫酸镁溶液的试管中加入金属Cr | 无明显现象 | 猜想_____正确 |
(交流与讨论)
(1)实验前所用的金属片都需用砂纸打磨,目的是_____。
(2)实验①中发生反应的化学方程式为_____。
(3)结合探究结论,有同学提出上述三个实验可进行优化,只需选择三种药品,即可判断金属的活动性强弱。合理的选择是_____(选填序号)。
①硫酸镁溶液;②硫酸亚铬溶液;③硫酸铜溶液;④镁片;⑤铬片;⑥铜片
(拓展延伸)若将实验步骤①和②中反应后的混合物倒入同一烧杯中,搅拌、过滤, 得到固体 x 和溶液 y,则:
(1)溶液 y 中溶质的成分_____(选填序号)。
A 一定有 MgSO4 B 一定有CrSO4
C 可能有 H2SO4 D 可能有CuSO4
(2)过滤过程中,用到的玻璃仪器有烧杯、玻璃棒和 _____,其中玻璃棒的作用是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有“第四类新材料”之称的玉米塑料是由乳酸(C3H6O3)合成的,下列有关乳酸的说法中正确的是( )
A. 乳酸中碳、氢、氧三种元素的质量比为3:6:3
B. 乳酸与甲醛(CH2O)中碳元素质量分数相同
C. 1个乳酸分子中含有3个H2O分子
D. 乳酸的相对分子质量为90 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com