
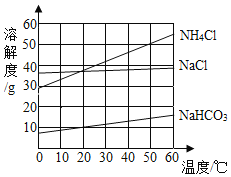
【题目】NH4Cl、NaCl、NaHCO3三种物质的溶解度曲线如下图所示,下列说法正确的是( )
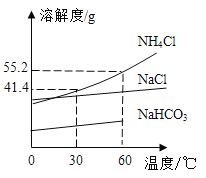
A.NH4Cl 的溶解度比NaCl 大
B.30℃时,将 25gNH4Cl 固体溶解在 50g 水中,可得到 75g溶液
C.NaHCO3 溶解度曲线消失是因为温度高于 60℃时NaHCO3受热分解
D.60℃时,NH4Cl 饱和溶液中溶质的质量分数为 55.2%
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:初中化学 来源: 题型:
【题目】某化学兴趣小组为了测定贝壳中碳酸钙的质量分数,做如下实验:取贝壳样品12g装入烧杯中,向其中加入一定质量分数的稀盐酸(杂质不溶于水也不参加反应),所加盐酸的质量与烧杯中剩余固体质量关系如下图。试计算:
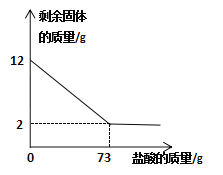
(1)贝壳中碳酸钙的质量为________g
(2)稀盐酸中溶质的质量分数______。(写出计算过程)
(3)恰好完全反应时,所得溶液中溶质的质量分数______。(计算精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2014年10月24日,我国探月工程三期再入返回飞行试验器在西昌卫星发射中心用长征三号丙运载火箭成功发射升空,首次成功实现再入返回飞行试验。回答下列问题:
(1)偏二甲肼是目前国际最普遍使用的火箭燃料,氧化剂为四氧化二氮,当火箭燃料完全反应时生成三种新物质,均是空气中的无害成分,写出该反应的化学方程式为_____。通过此反应谈谈你对燃烧的概念有什么新的认识?_______。
(2)火箭燃烧时将____能转化成热能,再转换成火箭的机械能,于是火箭升空。火箭从研制到发射过程,其中一定不属于物理变化的是________(填序号)
A 铝铜合金铸造火箭发动机 B 火箭推进剂采用液氦冷却
C 第三级燃料液氢由氢气液化而成 D 点燃火箭燃料燃烧
(3)火箭特种燃料易燃、易爆、剧毒、易挥发、强腐蚀,是一种危险级别最高的化工品,燃料加注将在火箭发射前24小时进行。因此在运输、储存和加注时应采取的安全保护措施是___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学方程式书写正确的是
A.C+ O2= CO2B.H2CO3 = H2O + CO2↑
C.S + O2 ![]() SO2↑D.2NaOH + CuSO4= Na2SO4 + Cu(OH)2
SO2↑D.2NaOH + CuSO4= Na2SO4 + Cu(OH)2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】多角度认识物质,能帮助我们更全面了解物质世界。以氧气和二氧化碳为例,回答下列问
(1)认识物质的性质。
如图所示,将高低两个燃着的蜡烛放入烧杯中,向烧杯中缓缓倾倒二氧化碳,观察到的实验现象是______;该实验说明CO2具有的性质是______。
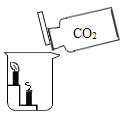
(2)辩证地认识物质。
功过相对论。以二氧化碳的“功”、“过”事实分析。“功”:为工业生产和植物的光合作用提供丰富的原料;“过”:使全球气候变暖导致海平面上升等。植物光合作用的化学方程式为:6CO2+6H2O![]() 6O2+X,则X的化学式是_____________;为了降低大气中二氧化碳含量过多所导致的危害,需要将二氧化碳吸收并加以利用,利用二氧化碳的成功范例是:在高温、高压下,以二氧化碳和氨气(NH3)为原料合成尿素[CO(NH2)2],同时有水生成,该反应的化学方程式是_________。
6O2+X,则X的化学式是_____________;为了降低大气中二氧化碳含量过多所导致的危害,需要将二氧化碳吸收并加以利用,利用二氧化碳的成功范例是:在高温、高压下,以二氧化碳和氨气(NH3)为原料合成尿素[CO(NH2)2],同时有水生成,该反应的化学方程式是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定石灰石中碳酸钙的质量分数,小明取石灰石样品,加到足量的稀盐酸中,进行实验(假定样品中其他成分不与稀盐酸反应)。
石灰石样品的质量 | 烧杯和稀盐酸的总质量 | 反应后烧杯及烧杯中各物质的总质量 |
12.5g | 87.5g | 95.6g |
请计算:
(1)生成二氧化碳的质量______________。
(2)求样品中碳酸钙的质量分数________________(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019 年 12 月 17 日,我国首艘国产航母山东舰正式入列,它和辽宁舰一起组成了我国首支双航母编队,共同守卫我国绵长的海岸线及丰富的海洋资源。

(1)可燃冰被科学家誉为“未来能源”、“21 世纪能源”。我国在南海海域试采可燃冰已获得成功,成为全球第一个在海域可燃冰试开采中获得连续稳定产气的国家。可燃冰是一种海底新型矿产资源,它是由天然气和水在低温高压条件下形成的冰状固体,其中甲烷占 80%~99.9%,(可表示为 mCH4·nH2O),能直接点燃,所以称为“可燃冰”。
①甲烷充分燃烧的化学方程式为_____________________________。
②为什么说可燃冰是清洁能源?______________________________。
(2)金属镁广泛应用于国防工业和生产生活。下图所示为从卤水(或海水)中提取镁的工艺流程:
![]()
①在上述工艺流程中,步骤①里所发生的反应属于_________反应。(选填“化合”、“分解”、“复分解”、“中和”之一)
②从海水中提取MgCl2 时,经历了“MgCl2 → Mg(OH)2↓ → MgCl2”的转化过程, 请分析这样做的目的是什么?__________。
(3)我国著名化工专家侯德榜在氨碱法基础上创立了更先进的侯氏制碱法,为世界纯碱工业技术发展做出了杰出贡献。在海水“制碱”过程中,涉及 NH4Cl、NaHCO3 等物质, 请结合如图所示的溶解度曲线,回答下列问题:
①侯氏制碱法中的“碱”是指(填化学式)___________________。
②30°C 时,将 11g NaHCO3 固体加入到 100g 水中, 充分搅拌,最终能得到__________g 溶液。
③氨碱法原理之一是:NaCl + NH3 + H2O + CO2 = NH4Cl + NaHCO3,在两种生成物中, 最先结晶析出的是_________________,请你根据溶解度曲线和产物质量关系,解释其原因:________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E、F是初中常见的六种不同物质(物质是溶液的只考虑溶质),其中A是红棕色固体,B由两种元素组成,侯德榜改进了F的生产方法。它们之间的部分关系如图所示(部分反应物、生成物及反应条件已略去,部分反应在溶液中进行),图中“—”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以通过一步反应转化为另一种物质。请回答下列问题:
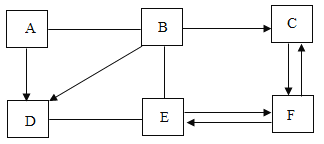
(1)写出下列物质的化学式:
A_____;B_____;
(2)写出C转化为F的化学方程式_____;
(3)写出向D溶液中加入足量的E溶液后反应的实验现象_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定质量的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法正确的是

A.0~a段发生了一个反应
B.c点沉淀的成分只有一种
C.d点对应溶液的溶质有两种
D.取e点对应的溶液,滴加硝酸银溶液,产生白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com