
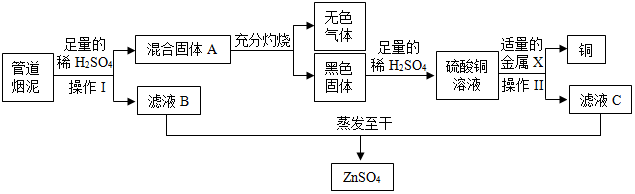
���� ��1�������������õĵ����ԡ������Ժ���չ�ԣ�
��2�����������£�һ����̼����������Ӧ�������Ͷ�����̼��
��3�������ܹ��ѹ����Һ����룬����ʱʹ���˲���������������������
ʵ������У�п��ϡ���ᷴӦ��������п��������������ͭ��Ӧ��������п��ͭ���������û���Ӧ��
��� �⣺��1�������Ƴ����ڰ�װ����������������������չ�ԣ�
���壺��չ�ԣ�
��2����һ����̼��ԭ�������Ļ�ѧ����ʽΪ��Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
���Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��3���ٲ����������ǹ��ˣ�������ʹ���˲���������������������
���������
��ʵ������з����û���Ӧ�ķ�Ӧ�ǣ�п��ϡ���ᷴӦ��������п��������������ͭ��Ӧ��������п��ͭ����Ӧ�Ļ�ѧ����ʽΪ��
Zn+H2SO4�TZnSO4+H2����Zn+CuSO4�TZnSO4+Cu��
���Zn+H2SO4�TZnSO4+H2����Zn+CuSO4�TZnSO4+Cu��
���� Ҫ�����ý����˳�������ʵ�飬��ǰ�ߵĽ�������ϡ���ᡢ���ᷴӦ�������ߵĽ���������ϡ���ᡢ���ᷴӦ��ǰ�ߵĽ�����Ѻ�ߵĽ�����������Һ���û�������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͼ�ǽ�������������Ӧ�����Ȼ��Ƶ���ʾ��ͼ������ͼʾ�ش��������⣮
��ͼ�ǽ�������������Ӧ�����Ȼ��Ƶ���ʾ��ͼ������ͼʾ�ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��֪A��B��C��D�dz��л�ѧ�г��������ʣ�����֮��IJ���ת����ϵ��ͼ��ʾ��ͼ�з�Ӧ���������ַ�Ӧ���������ʡ�ԣ���A��һ������ЧӦ����Ҫ���壬B�ǵ��ʣ�D�ڳ����²��ȶ��ֽ⣮
��֪A��B��C��D�dz��л�ѧ�г��������ʣ�����֮��IJ���ת����ϵ��ͼ��ʾ��ͼ�з�Ӧ���������ַ�Ӧ���������ʡ�ԣ���A��һ������ЧӦ����Ҫ���壬B�ǵ��ʣ�D�ڳ����²��ȶ��ֽ⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
 ��100g����������Ȼ��ƵĻ����Һ�У�����21.2%��̼������Һ��������Һ��pH�仯�����̼������Һ��������ϵ��ͼ���Է������㣺
��100g����������Ȼ��ƵĻ����Һ�У�����21.2%��̼������Һ��������Һ��pH�仯�����̼������Һ��������ϵ��ͼ���Է������㣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | CO2��SO2���ܺ�NaOH��Һ��Ӧ��COҲ�ܺ�NaOH��Һ��Ӧ | |
| B�� | CO��C���ܺ�CuO��Ӧ����Cu���л�ԭ�ԣ�H2Ҳ����CuO��Ӧ����Cu��Ҳ�л�ԭ�� | |
| C�� | ���ý��������ᷴӦ�������壬�����ᷴӦ������������ʲ�һ���ǻ���� | |
| D�� | �������ƺ��������ƶ����ڼ�����н���Ԫ�أ����Լ���н���Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
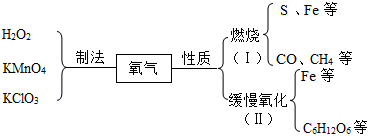
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com