
����Ŀ����ͼ��ʵ�����Ʊ�����������һϵ�����ʵ���װ��(�г��豸����)��

��1��װ��A�������ķ���װ�ã���д����Ӧ��Ӧ�Ļ�ѧ����ʽ��__________��
��2��װ��B�б���ʳ��ˮ��������___________��ͬʱװ��BҲ�ǰ�ȫƿ�����ʵ�����ʱC���Ƿ�����������д����������ʱB�е�����_______________��
��3��װ��C��ʵ��Ŀ������֤�����Ƿ����Ư���ԣ�Ϊ��C��I��II��III�����η������ʵ����Ӧ��_________����ĸ���)��
��� | I | II | III |
a | �������ɫ���� | ��ʯ�� | ʪ�����ɫ���� |
b | �������ɫ���� | ��ˮ����ͭ | ʪ�����ɫ���� |
c | ʪ�����ɫ���� | Ũ���� | �������ɫ���� |
d | ʪ�����ɫ���� | ��ˮ�Ȼ��� | �������ɫ���� |
��4�����װ��D��E��Ŀ���DZȽ��ȡ��塢�ⵥ�ʵ������ԡ���Ӧһ��ʱ���������װ��D��������Һ����װ��E�У����۲쵽��������__________________________��������__________(������������������)˵���嵥�ʵ�������ǿ�ڵ⣬ԭ����____________��
��5��װ��F��������__________________�����ձ��е���Һ����ѡ�������е�_____(����ĸ���)��
a������NaOH��Һ b������Ca(OH)2��Һ
c������Na2SO3��Һ d������Na2CO3��Һ
���𰸡�Ca(ClO) 2��4HCl(Ũ)=CaCl2��2Cl2����2H2O ��ȥCl2�е�HCl B�г���©����Һ���������γ�ˮ�� d E����Һ��Ϊ���㣬�ϲ�(����)Ϊ�Ϻ�ɫ ���� ������Cl2Ҳ�ɽ�I������ΪI2 �������ȣ���ֹ��Ⱦ���� b
��������
��1��Ư���е�Ca(ClO)2��Ũ���ᷴӦ����Cl2����ѧ����ʽΪ��Ca(ClO) 2��4HCl(Ũ)=CaCl2��2Cl2����2H2O��
��2����Ũ������ȡ��Cl2�к���HCl������װ��B�б���ʳ��ˮ�������dz�ȥCl2�е�HCl�����C�з���������B��ѹǿ������B�г���©����Һ���������γ�ˮ����
��3��Ϊ����֤�����Ƿ����Ư���ԣ�I�м���ʪ�����ɫ������IIΪU�ܣ��ɼ�������������õ������Cl2��III�м���������ɫ����������֤��Cl2�Ƿ����Ư���ԣ���d����ȷ��
��4��װ��D���Լ�Ϊ��ˮ�����뵽E�У�Br2��I��Ӧ����I2������ʵ������Ϊ��E����Һ��Ϊ���㣬�ϲ�(����)Ϊ�Ϻ�ɫ��Cl2ͨ��D��NaBr��Ӧ����Br2�����ܻ���Cl2ʣ�࣬����D����Һ���뵽E�У�Ҳ�п�����Cl2��I����ΪI2����˲���˵���嵥�ʵ�������ǿ�ڵ⣻
��5��Cl2�ж�����Ҫ����β������������װ��F���������������ȣ���ֹ��Ⱦ������A��Cl2����NaOH��Һ��Ӧ�������գ���ȷ��b����ΪCa(OH)2����ˮ������Ca(OH)2��ҺŨ��С�����ܳ������Cl2������C��Cl2���н�ǿ�����ԣ�������Na2SO3�������գ���ȷ��D��Cl2����Na2CO3��Һ��Ӧ������NaCl��NaClO��NaHCO3�������գ���ȷ����Ϊb��


 ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�
ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������12������Ϊ��ѧ��ѧ�г���������:
��Cu����NaCl����NaHSO4����SO3����H2SO4��C2H5OH����CaCO3����BaSO4����Cu(OH)2��Fe(OH)3��![]() NaOH��
NaOH��![]() NH3��H2O
NH3��H2O
��ش��������⣨����ţ���
��1�����ڵ���ʵ���_____��
��2�����ڷǵ���ʵ���_____��
��3����ˮ��Һ���ܵ���ĵ������_____��
��4������������ʵ���_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��̬��A�ڱ�״���µ��ܶ�Ϊ1.25 g��L��1��C�ܹ�����������Ӧ�� E��B��D���ܷ���������Ӧ���й����ʵ�ת����ϵ���£�

��ش�
(1) F�Ľṹ��ʽ______��
(2) A��B�ķ�Ӧ����______��
(3) C��D�Ļ�ѧ����ʽ______��
(4) ����˵������ȷ����______��
A����������Ͷ��B�У������Ƴ���ײ����������ķų�����
B��2 mol F���Է�Ӧ����1 mol��״����������ʽΪC4H6O5
C��G����NaHCO3��Һ�л��������
D��1 mol H�����뺬2 mol NaOH��ˮ��Һ��ȫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ϵ�صĹ���ԭ������ͼ��ʾ��ͨ������ȼ�ϵ������ʽ(���������ҺΪ����ʱ)�ͼ�ʽ[���������ҺΪNaOH(aq)��KOH(aq)ʱ]���֡��Իش��������⣺

(1)��ʽ��صĵ缫��Ӧ��������___________________________________��������________________________________________________________������ܷ�Ӧ��________________________________________________���������ҺpH�ı仯________(��������С�����䡱)��
(2)��ʽ��صĵ缫��Ӧ��������_______________________________________��������______________________________________________________������ܷ�Ӧ��____________________________________________________���������ҺpH�ı仯________(��������С�����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������������ˢ����ѧ���������ά�����ⷢ�������Ա���ۣ���Ҫ�ɷ�ΪBaCO3������SiO2��Fe2+��Mg2+�����ʣ��Ʊ����������������£�
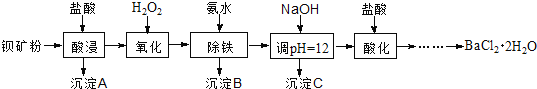
��֪��������Fe3+��Mg2+��ȫ������pH�ֱ��ǣ�3.4��12.4��
��1������A������Ϊ___________��
��2����Һ1��H2O2��Ŀ����___________��
��3����NaOH��Һ����pH��12.5���õ�����C����Ҫ�ɷ���___________��д��ѧʽ��
��4����Һ3���������ữ���پ�����Ũ��____________ϴ�ӣ���ո����һϵ�в�����õ�BaCl2��2H2O���塣
��5�������£���BaCl2��2H2O���Ƴ�0.2 mol/Lˮ��Һ��������Һ��Ӧ���ɵõ���������������д���÷�Ӧ�����ӷ���ʽ___________����֪Ksp(BaF2)��1.84��10-7������������ȫ����ʱ����������Ũ�ȡ�10-5 mol/L����������Ҫ�ķ�����Ũ����___________mol/L����֪![]() ��1.36��������������λ��Ч���֣���
��1.36��������������λ��Ч���֣���
��6��5.0 t��80��BaCO3�ı���ۣ����������������BaCl2��2H2O����___________t ��������2λС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���з�Ӧ�����ӷ���ʽ�ǣ� ��
A. ��ˮ��ͨ��������Cl2+H2O2H++Cl��+ClO��
B. ����������Ũ���ᷴӦ��MnO2+4HCl��Ũ��![]() Mn2++2Cl2��+2H2O
Mn2++2Cl2��+2H2O
C. ̼��������Һ�ӹ�������ʯ��ˮ��2HCO3��+Ca2++2OH���TCaCO3��+2H2O+CO32��
D. ������������ͭ��Һ��Ӧ��2Na+2H2O+Cu2+�T2Na++Cu��OH��2��+H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2O2(l)����MnO2�����º���MnO2�����·ֽ�������仯��ͼ��ʾ������˵����ȷ��

A. ��MnO2�����µķ�Ӧ������a����
B. a���߱�Ϊb���ߣ���Ӧ�Ļ���Ӱٷ�������
C. a���߱�Ϊb���ߣ�ƽ��ʱH2O2��ת��������
D. b���ߵ��Ȼ�ѧ����ʽΪ��H2O2(l) =H2O(l) +1/2O2(g) ��H= - ( E1 - E2)KJmol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ���������ʵ��װ�ã�����Ũ���������ǵķ�Ӧʵ�顣

��1��ʵ�鿪ʼʱ��������ƿ�м���15g���ǣ������뼸��ˮʹ������ȫʪ��Ȼ��ӷ�Һ©���м���15mLŨ���ᣬˮ��������_________��
��2��ʵ������ƿ�ں�ɫ�����������͵�ԭ����________���û�ѧ����ʽ��ʾ����
��3��Ϊ�˼���ʵ���в�����CO2���������ӿ�a֮���ʵ�����������_________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���ӵ����Ų��ĽǶȽ���Fe2+���ױ�����ΪFe3+��ԭ���ǣ�___________
��2����ҵ�õ���Ȼ�þ�Ƶ�þ������������þ��ԭ��____________________
��3����̬��ԭ�ӵ���Χ�����Ų�ʽΪ5d106s1�����жϽ���Ԫ�����ڱ���λ�ڵ�________���ڵ�________�壮
��4����֪Ag��Cuλ��ͬһ�壬��Ag��Ԫ�����ڱ���λ��________��(��s��p��d��f�� ds )��
��5��CaC2����ľ����ṹ��NaCl���������(��ͼ��ʾ)����CaC2�����к���������![]() �Ĵ��ڣ�ʹ������һ������������CaC2������1��Ca2����Χ���������
�Ĵ��ڣ�ʹ������һ������������CaC2������1��Ca2����Χ���������![]() ��ĿΪ________��
��ĿΪ________��

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com