
【题目】(1)请把下列几组物质进行归类。
A.金刚石与足球烯
B.D与T

①互为同位素的是________(填字母,下同);
②互为同素异形体的是________;
③互为同分异构体的是________;
④属于同一种物质的是________。
(2)写出下列工业生产过程所涉及的主要反应的化学方程式。
①用铝热法炼铁:___________________________________。
②用电解法炼铝:______________________________________。
③生产聚乙烯塑料:______________________________________。
【答案】BADC2Al+Fe2O3![]() Al2O3+2Fe2Al2O3(熔融)
Al2O3+2Fe2Al2O3(熔融)![]() 4Al+3O2↑nCH2===CH2
4Al+3O2↑nCH2===CH2![]()
![]() CH2—CH2
CH2—CH2![]()
【解析】
(1)根据同位素、同分异构体、同素异形体的概念作答:①具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素;②同素异形体是同种元素形成的不同单质;③具有相同分子式而结构不同的化合物互为同分异构体;④分子式、结构均相同,是同一物质。(2)根据反应物和生成物写出方程式,注意反应条件。
(1)①具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素;D与T是氢元素的不同氢原子,互为同位素,故选B;②同素异形体是同种元素形成的不同单质;金刚石与“足球烯”(C60);由碳元素形成的不同的单质,互为同素异形体,故选A;③具有相同分子式而结构不同的化合物互为同分异构体;丁烷和异丁烷分子式相同,结构不同,互为同分异构体,故选D;④分子式、结构均相同,是同一物质,故选C;(2)①用铝热法炼铁:2Al+Fe2O3![]() Al2O3+2Fe。②用电解法炼铝:2Al2O3(熔融)
Al2O3+2Fe。②用电解法炼铝:2Al2O3(熔融)![]() 4Al+3O2↑。
4Al+3O2↑。
③生产聚乙烯塑料:nCH2===CH2![]()
![]() CH2—CH2
CH2—CH2![]() 。
。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】I.双氧水(主要成分H2O2)是常见的氧化剂、还原剂。
(1)如下图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式____________。

(2)H2O2可看作二元弱酸,写出它在水中第一步电离的方程式______________________________。
II.A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。

(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:__________________________________________________________________________________。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则X可能为______________________(填代号)。
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.Na[Al(OH)4]
(3)若A为淡黄色粉末,则A的电子式为____________________。若X为一种最常见的造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为__________(填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为________________________________,E是__________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废气H2S经资源化利用后可回收能量并得到单.质硫。反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ·mol-1。H2S燃料电池的工作原理如图所示。下列有关说法不正确的是( )

A. 电极a为电池的负极
B. 电极b上的电极反应式为:O2+4H++4e-=2H2O
C. 若有17gH2S参与反应,则会有1molH+经质子膜进入正极区
D. 若电路中通过2mol电子,则电池内部释放632kJ热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼酸(H2BO3)可以通过电解NaB(OH)4溶液的方法制备,工作原理如图所示。下列有关表述错误的是( )
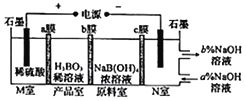
A. M室的电极反应式为2H2O-4e-=O2↑+4H+
B. N室中,进口和出口的溶液浓度大小关系为a%<b%
C. b膜为阴离子交换膜,产品室发生反应为H++[B(OH)4]-=H3BO3+H2O
D. 理论上每生成1molH3BO3,阴极室可生成5.6L气体(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
A. 0.1 mol CH4分子所含质子数为1.6 NA
B. 在0℃,101kPa时,22.4 L H2中含有NA个氢原子
C. 16 g氧气和16 g臭氧所含的原子数均为NA
D. NA个CO分子和11.2L CH4的质量比为7:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在周期表中的相对位置如图所示,这四种元素原子的最外层电子数之和为20。下列说法正确的是
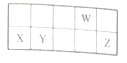
A. X的简单离子与Z的简单离子具有相同的电子层结构
B. 最简单氢化物的稳定性:W>Y
C. 原子半径:Y>X
D. 化合物YW2和YZ4中均含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G[ ]是一种医药中间体,它的一种合成路线如下:
]是一种医药中间体,它的一种合成路线如下:

已知:
请回答下列问题:
(1)A的名称是_____________。
(2)B→C的反应条件为_____________。
A→B和D→E的反应类型分别是_____________、_____________。
(3)D在浓硫酸加热的条件下会生成一种含六元环的化合物,该化合物的结构简式为_____________。(4)H是一种高聚酯,D→H的化学方程式为_____________。
(5)下列关于化合物G的说法错误的是_____________。
A.G的分子式为C12H14O5
B.1molG与NaOH溶液加热最多消耗2molNaOH
C.一定条件下G发生消去反应生成的有机物存在顺反异构体
D.在一定条件下G能与HBr发生取代反应
(6)M是D的同分异构体,与D具有相同的官能团。则M可能的结构有____种。
(7)已知酚羟基不易与羧酸发生酯化反应,写出由苯酚,甲苯为原料制备苯甲酸苯酚酯(![]() )的合成路线(其它试剂任选)。 __________________
)的合成路线(其它试剂任选)。 __________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭绝热容器中发生反应:SO2(g)+NO2(g) ![]() SO3(g)+NO(g) △H<0下列有关说法不正确的是 ( )
SO3(g)+NO(g) △H<0下列有关说法不正确的是 ( )
A. 增大SO2的浓度,平衡正向移动
B. 使用催化剂,正反应速率和逆反应速率同时增大
C. 反应达到平衡时,扩大容器体积,平衡逆向移动
D. 反应达到平衡时,降低温度,平衡正向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com