
【题目】由冰铜(mCu2O·nFeS)冶炼得到粗铜,再以粗铜为原料制纯铜的流程如下:
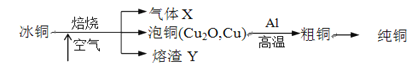
请回答下列问题:
(1)气体X是________。
(2)写出泡铜冶炼粗铜反应的化学方程式_______。
(3)某研究性学习小组用熔渣Y与CO反应来制取Fe(已略去加热装置)。
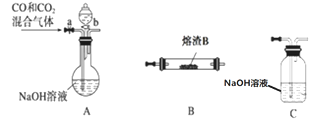
①请按气流由左到右的方向连接下列各装置,顺序为A→________→尾气处理装置;
②装置C的作用是________________。

(4)熔渣Y中铁元素的价态有+2价和+3价,为了测定熔渣中二价铁的含量。学习小组取23.2g熔渣用足量硫酸使其完全溶解,向反应后的溶液中加入酸性KMnO4溶液,一共消耗200mL0.1mol/L的KMnO4溶液。
①写出溶液中加入酸性高锰酸钾溶液后发生的离子方程式:________。
②熔渣中二价铁的质量分数为___%(保留三位有效数字)。
【答案】SO2 3Cu2O+2Al![]() 6Cu+ Al2O3 D→B→C 除去尾气中的CO2 5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O 24.1
6Cu+ Al2O3 D→B→C 除去尾气中的CO2 5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O 24.1
【解析】
冰铜焙烧得到二氧化硫、泡铜和铁的氧化物,泡铜通过铝热反应得到粗铜,粗铜经提纯可制得纯铜。
(1)FeS在空气中灼烧可生成二氧化硫;
(2)泡铜与铝发生铝热反应得粗铜;
(3)①用铁的氧化物与CO反应来制取Fe,应先将制得CO进行干燥再通与铁反应,反应后生成的二氧化碳用氢氧化钠溶液吸收,未反应的CO在空气中点燃,以免对空气产生污染;
②根据①的分析可析可知,便于CO点燃,用氢氧化钠除去尾气中的CO2;
(4)加入酸性高锰酸钾发生5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O,结合高锰酸钾的物质的量可计算二价铁的质量分数。
:(1)冰铜含有S元素,在高温下可生成SO2,故答案为:SO2;
(2)泡铜与铝发生铝热反应得粗铜,反应的化学方程式为3Cu2O+2Al![]() 6Cu+Al2O3,
6Cu+Al2O3,
故答案为:3Cu2O+2Al![]() 6Cu+Al2O3;
6Cu+Al2O3;
(3)①用铁的氧化物与CO反应来制取Fe,应先将制得CO进行干燥再通与铁反应,反应后生成的二氧化碳用氢氧化钠溶液吸收,未反应的CO在空气中点燃,以免对空气产生污染,所以按气流由左到右的方向连接下列各装置,顺序为A→D→B→C,
故答案为:D→B→C;
②根据①的分析可析可知,便于CO能点燃,用氢氧化钠除去尾气中的CO2,所以装置C的作用是除去尾气中的CO2,
故答案为:除去尾气中的CO2;
(4)①亚铁离子具有还原性,与高锰酸钾发生氧化还原反应,离子方程式为5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O,
故答案为:5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O;
②n(KMnO4)=0.2L×0.1mol/L=0.02mol,由离子方程式可知n(Fe2+)=0.1mol,则23.2g熔渣中二价铁的质量分数为![]() ×100%=24.1%,故答案为:24.1。
×100%=24.1%,故答案为:24.1。


科目:高中化学 来源: 题型:
【题目】下列有关乙烯和乙烷的说法中错误的是![]()
![]()
A. 乙烯是平面分子,乙烷分子中所有原子不可能在同一平面内
B. 溴的四氯化碳溶液和酸性![]() 溶液都可以鉴别乙烯和乙烷
溶液都可以鉴别乙烯和乙烷
C. 溴的四氯化碳溶液和酸性![]() 溶液都可以除去乙烷中混有的乙烯
溶液都可以除去乙烷中混有的乙烯
D. 乙烯的化学性质比乙烷的化学性质活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】透明聚酯玻璃钢可用于制造宇航员面罩和导弹达罩。制备橐酯的一种配方中含有中基丙烯酸甲酯(MMA,结构简式如图。下列有关MMA的说法正确的是

A. MMA易溶于水和有机溶剂
B. MMA的含氧官能团是羧基
C. MMA的一种同分异构体为CH3CH2 COOCH2CH3
D. MMA能发生加成反应、水解反应、氧化反应、加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃料法测定某种氨基酸(CxHyOzNp)的分子式组成,取Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现用下图所示装置置进行实验(铁架台、铁夹、酒精灯等未画出)。请回答有关问题:
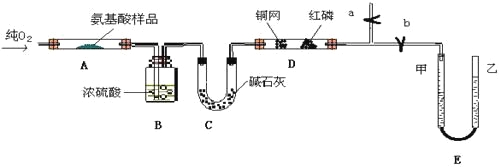
(1)实验开始时,首先打开止水夹a,关闭止水夹b,通入一段时间的氧气,这样做的目的是______________________,之后关闭止水夹a。
(2)由装置B、C可分别确定待测氨基酸中含有的________和_______质量。
(3)E装置的作用是测量__________的体积,并由此确定待测氨基酸中含有的____________________的质量,为了较准确地测量该气体的体积。在读反应前后甲管中液面的读数求其差值的过程中,应注意____________(填代号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平
(4)实验中测定的哪一数据可能不准确__________________________
其理由是_____________________________
(5)严格地说,按上述方案只能确定氨基酸的____________________。
若要确定此氨基酸的分子式,还要测定该氨基酸的______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)甲烷和氯气在光照条件下发生卤代反应,其反应机理如下:
反应①:![]() △H=242.7kJ·mol-1
△H=242.7kJ·mol-1
反应②:![]() △H=7.5kJ·mol-1
△H=7.5kJ·mol-1
反应③:![]() △H=-112.9kJ·mol-1
△H=-112.9kJ·mol-1
反应②、③反复循环,反应物浓度逐渐降低,自由基逐渐消失,反应停止。
(1)在该反应条件下断裂1mol CH3Cl中C—Cl键,需要吸收的能量为______。
(2)反应②与反应③的反应过程,如下图所示:
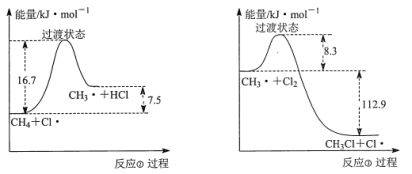
则该条件下,反应②的速率______反应③的速率(填“>”、“<”或“=”)。
(3)根据以上的反应机理,我们可以推测甲烷和氯气在光照条件下反应,除生成CH3Cl、CH2Cl2、CHCl3、CCl4外,还会有乙烷等有机物,原因是______。
(二)煤燃烧排放的SO2和NO2可形成严重的大气污染,某兴趣小组提出利用反应![]() 来处理。
来处理。
(4)在一定温度下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,达到平衡时NO2和SO2的体积之比为1:5,则该温度下平衡常数K为______。
(5)若向绝热恒容密闭容器中通入SO2和NO2,v正随时间变化如下图。下列结论正确的是______。
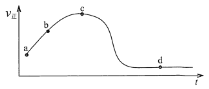
A. a点颜色比b点深
B. c点正反应速率等于逆反应速率
C. 若升高温度,d点SO2的转化率将增大
D. 反应的过程中,容器内气体压强保持不变
E. 若外界条件不发生改变,d点NO2和NO的体积比将保持不变
(6)若用一定浓度的NaClO2溶液(已调节其初始pH为5)充分吸收煤燃烧排放的烟气后,测得溶液中各物质的浓度如下表所示:

其中 NaClO2溶液吸收SO2的主要离子反应方程式为______。
(7)为消除NOx,科学家开发了一种能传导O2-的固态高温陶瓷电池,一极通氨气,另一极通NOx,生成无污染的常见气体和液体。写出该电池的正极反应式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品有:①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。将上述物质分别溶于水,其水溶液具有碱性的是______(填序号,下同),主要成分中属于盐类的是________,相互间能发生反应的是______。
(2)生活中遇到下列问题,不涉及到化学变化的是________。
①用四氯化碳可擦去圆珠笔油 ②自来水厂用液氯消毒 ③可用食醋洗掉水垢
(3)当前,环境治理已成为重要的民生工程。
①我国城市发布的“空气质量日报”中,下列物质不列入首要污染物的是_____(填字母代号)。
A.二氧化硫 B.二氧化碳 C.二氧化氮 D.可吸入颗粒物
②煤炭直接燃烧会引起多种环境问题。燃煤产生的SO2是导致______(填名称)污染现象形成的原因;处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S,发生反应的化学方程式为_____________________。
(4)向浑浊的水中加入明矾KAl(SO4)212H2O后,水可得到净化。写出明矾在水中的电离方程式___,往明矾溶液中逐滴加入Ba(OH)2溶液直至Al3+恰好沉淀完全,发生反应的离子方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组按下列两条线合成咖啡因:
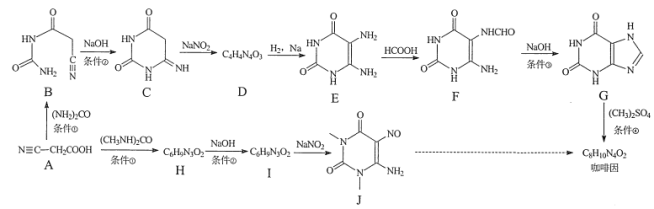
已知:R1-NH-R2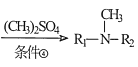 ,请回答:
,请回答:
(1)下列说法正确的是____。
A. 化合物A能与碳酸氢钠反应产生气体
B. 化合物C在酸性条件下水解,加热后有CO2产生
C. 化合物E到F的反应为酯化反应
D. 化合物J的分子式是C6H10N4O3
(2)化合物D的结构简式是______。
(3)写出H→I的化学方程式______。
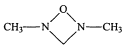
(4)化合物(CH3NH2)2CO的同分异构体的1H—NMR谱显示分子中只有2种化学环境不同的氢原子,符合要求的结构简式如图,除这三种外,还有______。
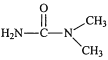 、
、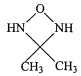 、
、
(5)根据题目所提供的信息,请设计J→咖啡因的合成路线(用流程图表示,无机试剂任选)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组在实验室用如图所示装置制取氨并验证氨的某些性质,请回答。
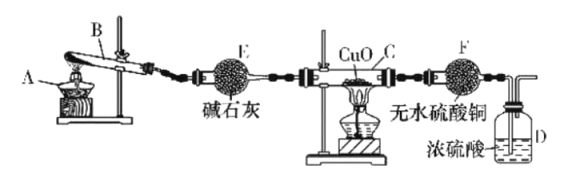
(1)写出此实验中制氨的化学方程式:___。
(2)实验进行一段时间,观察到硬质玻璃管内黑色氧化铜粉末变为红色,盛无水硫酸铜的干燥管内出现蓝色,同时有氮气生成。根据这些现象,写出在硬质玻璃管内发生反应的化学方程式:__,这个反应说明氨具有___(填字母代号)。
A.碱性 B.还原性 C.氧化性 D.不稳定性
(3)装置E的作用是__,装置F的作用是___。E中的碱石灰__(填“能”或“不能”)换成CaCl2。
(4)D中浓硫酸的主要作用是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为减轻大气污染,必须要加强对工业废气和汽车尾气的治理,根据所学知识回答下列问题:
(1)化石燃料包括煤、石油和________。
(2)酸雨是指pH____(填“>”“<”或“=”)5.6的降水,煤的燃烧是导致酸雨形成的主要原因,而正常雨水的pH约为5.6,原因是__________________ (用化学方程式表示)。
(3)煤的气化是高效、清洁利用煤的重要途径,可将煤炼成焦炭,再将焦炭在高温下与水蒸气反应生成一氧化碳和氢气的化学方程式为_________,该反应的基本类型是_________。
(4)在汽车尾气排放口加装“三效催化净化器”,在不消耗其他物质的情况下,可将尾气中的一氧化碳、一氧化氮转化为参与大气循环的气体和无毒的气体,该反应的化学方程式为__________________。
(5)在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施,以下对乙醇作汽车燃料的描述错误的是__________(填字母)。
![]()
A.原料来源丰富 B.是可再生能源 C.燃烧完全没有污染
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com