
【题目】链状有机物A是一种食用型香精,在一定条件下有如下变化:
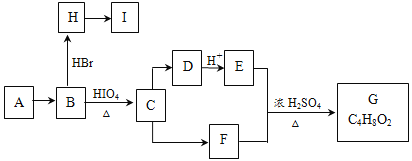
已知:(1)
(2)A和G互为同分异构体,A不能使Br2的CCl4溶液褪色。B和F中所含官能团的类型相同。
完成下列填空:
(1)F的分子式为________________;C→D的反应类型是__________________________。
(2)A的结构简式为________________________________。
(3)若C中混有少量的E,请写出相应的除杂试剂和分离方法:________________。
(4)I中所有碳原子均在一条直线上,H转化为I的化学方程式为:______________________。
(5)X是A的一种同分异构体,1mol X在HIO4加热条件下完全反应,可以生成1mol无支链有机物,则X的结构简式为_________________。
(6)设计有1-丁烯为原料,合成H的合成路线。(合成路线常用的表示方式为:甲![]() 乙……
乙……![]() 目标产物)______________________________________
目标产物)______________________________________
【答案】C2H6O 氧化反应  NaOH溶液(其他合理答案也可以,如Na2CO3溶液),蒸馏
NaOH溶液(其他合理答案也可以,如Na2CO3溶液),蒸馏 ![]() +2NaOH
+2NaOH![]() CH3-C≡C-CH3+2NaBr+2H2O
CH3-C≡C-CH3+2NaBr+2H2O 
![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
根据信息反应(1),B生成C,说明B分子对称,又A生成B,则A与B碳原子数相同,A和G互为同分异构体,A不能使Br2的CCl4溶液褪色,所以A含有4个碳原子,不含碳碳双键,所以B也含4个碳原子,则B为![]() ,A为
,A为 ,B与HBr发生取代反应生成H,则H为
,B与HBr发生取代反应生成H,则H为![]() ,H生成I,I中所有碳原子均在一条直线上,则I为CH3-C≡C-CH3,又B发生信息反应(1)生成C,则C为CH3CHO,C与银氨溶液反应在水浴加热的条件下生成D,D在酸化生成E,则E为CH3COOH,由E与F在浓硫酸加热条件下发生酯化反应生成G,则F为醇,C发生还原反应生成F为CH3CH2OH,G为CH3COOCH2CH3,据此分析解答。
,H生成I,I中所有碳原子均在一条直线上,则I为CH3-C≡C-CH3,又B发生信息反应(1)生成C,则C为CH3CHO,C与银氨溶液反应在水浴加热的条件下生成D,D在酸化生成E,则E为CH3COOH,由E与F在浓硫酸加热条件下发生酯化反应生成G,则F为醇,C发生还原反应生成F为CH3CH2OH,G为CH3COOCH2CH3,据此分析解答。
(1)由上述分析可知,F为CH3CH2OH,分子式为:C2H6O;C→D的反应为CH3CHO与银氨溶液反应在水浴加热的条件下生成D,属于氧化反应;
(2)由上述分析可知,A的结构简式为 ;
;
(3)若CH3CHO中混有少量CH3COOH,可将CH3COOH转化为盐,然后利用盐类与乙醛的沸点差异进行分离,可选用NaOH溶液反应,然后利用蒸馏蒸馏出乙醛;
(4)H为![]() ,I为CH3-C≡C-CH3,
,I为CH3-C≡C-CH3,![]() 在NaOH的醇溶液中进行加热发生消去反应生成CH3-C≡C-CH3,反应方程式为:
在NaOH的醇溶液中进行加热发生消去反应生成CH3-C≡C-CH3,反应方程式为:![]() +2NaOH
+2NaOH![]() CH3-C≡C-CH3+2NaBr+2H2O;
CH3-C≡C-CH3+2NaBr+2H2O;
(5)X是A的一种同分异构体,则分子式为C4H8O2,1molX在HIO4加热条件下完全反应,可以生成1mol无支链的有机物,则X为环状结构,则X的结构简式为 ;
;
(6)![]() 中Br可由碳碳双键与Br2发生加成反应生成,因此需通过1-丁烯先合成2-丁烯,可利用1-丁烯与HBr发生加成反应生成2-溴丁烷,2-溴丁烷发生消去反应生成2-丁烯,合成路线为:
中Br可由碳碳双键与Br2发生加成反应生成,因此需通过1-丁烯先合成2-丁烯,可利用1-丁烯与HBr发生加成反应生成2-溴丁烷,2-溴丁烷发生消去反应生成2-丁烯,合成路线为:![]()
![]()
![]()
![]()
![]()
![]()
![]() 。
。


科目:高中化学 来源: 题型:
【题目】pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为1×10-3mol·L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。如图为H2CO3在加入强酸或强碱溶液后,平衡时溶液中三种成分的pC-pH图。下列说法不正确的是
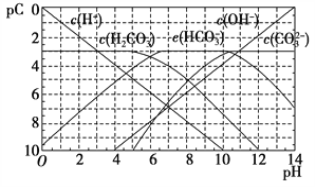
A. H2CO3、HCO3-、CO32-不能在同一溶液中大量共存
B. H2CO3电离平衡常数Ka1≈10-6
C. pH=7时,溶液中存在关系c(HCO![]() )>c(H2CO3)>c(CO
)>c(H2CO3)>c(CO![]() )
)
D. pH=9时,溶液中存在关系c(H+)+c(H2CO3)=c(OH-)+c(CO![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠离子电池具有成本低、能量转换效率高、寿命长等优点。一种钠离子电池用碳基材料(NamCn)作负极,利用钠离子在正负极之间嵌脱过程实现充放电,该钠离子电池的工作原理为:![]()
![]()
![]() 。下列说法不正确的是( )
。下列说法不正确的是( )
A. 充电时,阴极质量减小且Na+数目增加
B. 充电时,阳极的电极反应式为NaCoO2-me-=Na1-mCoO2+mNa+
C. 放电时,Na+向正极移动
D. 放电时,负极的电极反应式为NamCn-me-=mNa++Cn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是我国化工专家侯德榜发明的联合制碱法简要流程:

关于此流程说法正确的是
A. 副产品Y是NH4HCO3B. 向母液中通入的气体X是CO2
C. 循环II是为了提高食盐的利用率D. 析出NaHCO3后的母液中只含NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的核外电子排布式为____________________,有___________个未成对电子。
(2)磷的一种同素异形体一一白磷(P4)的立体构型为_______________,其键角为___________,推测其在CS2中的溶解度___________(填“大于”或“小于”)在水中的溶解度。
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因_________________________________。

(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如上左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为___________,其中心原子杂化轨道类型为___________,B为___________。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,上图为其立方晶胞,其中的每个原子均测是8电子稳定结构,试判断其熔点___________(填“高于”或“低于”)金刚石熔点。已知其B—P键长均为xcm,则其密度为___________g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的图示及分析均正确的是
选项 | 实验目的 | 实验图示 | 实验分析 |
A | 催化裂解正戊烷并收集产物 |
| 正戊烷裂解为分子较小的烷烃和烯烃 |
B | 酸碱中和滴定 |
| 摇动锥形瓶,使溶液向一个方向做圆周运动,勿使瓶口接触滴定管,溶液也不得溅出 |
C | 制取并收集乙炔 |
| 用饱和食盐水代替纯水,可达到降低反应速率的目的 |
D | 实验室制硝基苯 |
| 反应完全后,可用仪器a、b蒸馏得到产品 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型电池材料结构如图,M、W、X、Y、Z是同周期主族元素,除M外均满足8电子稳定结构,X的最外层电子数是W次外层电子数的3倍,下列说法正确的是

A.M的单质可以保存在煤油中
B.原子半径Z>X>Y
C.气态氢化物稳定性X>Y
D.W的最高价氧化物对应的水化物为三元弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是合成抗心律失常药物决奈达隆的一种中间体,可通过以下方法合成:
请回答下列问题:
(1)R的名称是_______________;N中含有的官能团数目是______。
(2)M→N反应过程中K2CO3的作用是____________________________________。
(3)H→G的反应类型是______________。
(4)H的分子式________________。
(5)写出Q→H的化学方程式:___________________________________。
(6)T与R组成元素种类相同,符合下列条件T的同分异构体有_____种。
①与R具有相同官能团;②分子中含有苯环;③T的相对分子质量比R多14
其中在核磁共振氢谱上有5组峰且峰的面积比为1:1:2:2:2的结构简式有___________。
(7)以1,5-戊二醇(![]() ) 和苯为原料(其他无机试剂自选)合成
) 和苯为原料(其他无机试剂自选)合成![]() ,设计合成路线:_________________________________________。
,设计合成路线:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子组成为C3H5O2Cl的含氯有机物A,与NaOH水溶液反应后再酸化,得到分子组成为C3H6O3的有机物B;在适当条件下,两分子B可以发生酯化反应生成一分子C。则C的结构简式不可能是( )
A.CH3CH(OH)COOCH(CH3)COOHB.![]()
C. D.
D.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com