

 ;D若为纯净物,D的核磁共振氢谱存在2种吸收峰,面积比为1:1;
;D若为纯净物,D的核磁共振氢谱存在2种吸收峰,面积比为1:1; ,反应类型:消去反应;
,反应类型:消去反应;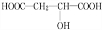 +HCOOH$?_{△}^{浓硫酸}$
+HCOOH$?_{△}^{浓硫酸}$ +H2O,反应类型:取代反应;
+H2O,反应类型:取代反应; ;
;分析 根据题意,MX=81×2=162,O:$\frac{162×49.4%}{16}$=5,H:10,C:$\frac{162-10-5×16}{12}$=6,所以X的分子式为C6H10O5,结合信息②和反应④⑤知A中含有羟基和羧基,且A中含有手性碳原子,故A结构为HOOCCH2CH(OH)COOH,A发生消去反应生成D为HOOCCH═CHCOOH,E为D的加聚产物,E结构简式为 ,结合X的分子式及X生成A的条件可知,X为
,结合X的分子式及X生成A的条件可知,X为 ,B为环状化合物,含一个六元环的有机物B结构简式为
,B为环状化合物,含一个六元环的有机物B结构简式为 ,A与甲酸发生酯化反应生成C为
,A与甲酸发生酯化反应生成C为 ,据此答题.
,据此答题.
解答 解:根据题意,MX=81×2=162,O:$\frac{162×49.4%}{16}$=5,H:10,C:$\frac{162-10-5×16}{12}$=6,所以X的分子式为C6H10O5,结合信息②和反应④⑤知A中含有羟基和羧基,且A中含有手性碳原子,故A结构为HOOCCH2CH(OH)COOH,A发生消去反应生成D为HOOCCH═CHCOOH,E为D的加聚产物,E结构简式为 ,结合X的分子式及X生成A的条件可知,X为
,结合X的分子式及X生成A的条件可知,X为 ,B为环状化合物,含一个六元环的有机物B结构简式为
,B为环状化合物,含一个六元环的有机物B结构简式为 ,A与甲酸发生酯化反应生成C为
,A与甲酸发生酯化反应生成C为 ,
,
(1)根据上面的分析可知,X的分子式为 C6H10O5,A结构为HOOCCH2CH(OH)COOH,A的分子中含有官能团的名称是羧基和羟基,E的结构简式为  ;D为HOOCCH═CHCOOH,D的核磁共振氢谱存在2种吸收峰,面积比为1:1,
;D为HOOCCH═CHCOOH,D的核磁共振氢谱存在2种吸收峰,面积比为1:1,
故答案为:C6H10O5;羧基和羟基; ;2;1:1;
;2;1:1;
(2)反应②的化学方程式为  ,反应类型:消去反应;反应④的化学方程式为
,反应类型:消去反应;反应④的化学方程式为 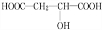 +HCOOH$?_{△}^{浓硫酸}$
+HCOOH$?_{△}^{浓硫酸}$ +H2O,反应类型:取代反应,
+H2O,反应类型:取代反应,
故答案为: ;消去反应;
;消去反应;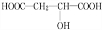 +HCOOH$?_{△}^{浓硫酸}$
+HCOOH$?_{△}^{浓硫酸}$ +H2O; 取代反应;
+H2O; 取代反应;
(3)根据上面的分析可知,B的一种含一个六元环的同分异构体的结构简式为 ,
,
故答案为: ;
;
(4)因为A的分子式为C4H6O5可看成C2H6O(CO2)2,因此等物质的量的A与C2H6O完全燃烧生成H2O的物质的量相等,耗氧量也相等,所以:C2H6O+3O2→2CO2+3H2O,因此耗O2量就等于生成H2O的物质的量为$\frac{18g}{18g/mol}$=1mol,
故答案为:1mol.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及知识综合应用能力,正确判断X结构简式是解本题关键,注意掌握官能团及其性质关系,题目难度中等.


科目:高中化学 来源: 题型:选择题
| 选项 | 规律 | 推论 |
| A | 含Ag+离子的溶液中滴加氯化钡溶液会产生白色沉淀 | 滴加氯化钡溶液产生白色沉淀的溶液中不一定含有Ag+离子 |
| B | 常温下铜与浓硝酸可以制取NO2 | 常温下铁与浓硝酸也可以制取NO2 |
| C | Fe(OH)3固体中滴加稀盐酸生成氯化铁和水 | Fe(OH)3固体中滴加氢碘酸生成碘化铁和水 |
| D | 铜片不溶于稀硫酸 | 铜片也不溶于稀硝酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在Na2SO4、Na2O以及Na2O2中,阳离子与阴离子的个数比均为2:1 | |
| B. | 实验桌上金属钠着火不能用常规灭火器灭火,可以选择用湿布盖灭 | |
| C. | 长距离运输鱼苗,最好在水中加入一定量的Na2O2,以起到供氧和杀菌的作用 | |
| D. | 金属钠和钾都保存在煤油中,所以金属锂(密度为0.534 g/cm3)也应该保存在煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将少量的金属钠分别投入CuSO4溶液中,有气体放出,且溶液质量减轻 | |
| B. | 露置在空气中的金属钠表面迅速变暗,是因为钠与空气中的氧气反应生成了氧化钠 | |
| C. | 发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔 | |
| D. | 在含有Na+、Cl-、CO${\;}_{3}^{2-}$、SO${\;}_{3}^{2-}$的溶液中加入足量Na2O2后,各离子仍能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | H-H | C-O | C═O | H-O | C-H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
| A. | 403 kJ•mol-1,-66 kJ•mol-1 | B. | 423 kJ•mol-1,+28 kJ•mol-1 | ||
| C. | 314 kJ•mol-1,-18 kJ•mol-1 | D. | 413 kJ•mol-1,-58 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①②③ | C. | ①②④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔既是物质的量的单位又是物质的质量单位 | |
| B. | 物质的量既表示物质的数量又表示物质的质量 | |
| C. | 阿伏加德罗常数是12kg碳12中含有的碳原子数目 | |
| D. | 1molH2O中含有10mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O的相对分子质量是18克 | |
| B. | H2O的摩尔质量是18克 | |
| C. | 标准状况下H2O的摩尔体积是22.4L.mol-1 | |
| D. | 1mol H2O的质量是18克 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com