
| ��ѧ�� | H-H | C-O | C�TO | H-O | C-H |
| E/��kJ��mol-1�� | 436 | 343 | 1076 | 465 | 413 |
| A�� | 403 kJ•mol-1��-66 kJ•mol-1 | B�� | 423 kJ•mol-1��+28 kJ•mol-1 | ||
| C�� | 314 kJ•mol-1��-18 kJ•mol-1 | D�� | 413 kJ•mol-1��-58 kJ•mol-1 |
���� ���ݸ�˹���ɿ�֪���Ȼ�ѧ����ʽ��+�ۿɵ��Ȼ�ѧ����ʽ�ڣ��Ӷ��ó���H2�����ݱ������ݿ�֪C-H���ļ���Ϊ413kJ/mol���ݴ˽��н��
��� �⣺���ݱ������ݿ�֪��C-H�ļ���Ϊ413kJ/mol��
��CO��g��+2H2��g��?CH3OH��g����H1=-99kJ?mol-1
��CO2��g��+H2��g��?CO��g��+H2O��g����H3=+41kJ?mol-1��
���ݸ�˹���ɢ�+�ۿɵã���CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H2=-99kJ?mol-1+41kJ?mol-1=-58 kJ•mol-1��
��ѡD��
���� ���⿼���˸�˹�������Ȼ�ѧ����ʽ�е�Ӧ�ã���Ŀ�Ѷ��еȣ���ȷ��˹���ɵĺ���Ϊ���ؼ���ע�������Ȼ�ѧ����ʽ����дԭ������������ѧ�������Ӧ��������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��ˮ��ֹ������ʴ | |
| B�� |  CuSO4��ͭ�ľ��� | |
| C�� |  ZnCl2��Һ��Ƭ��п | |
| D�� |  ����ʳ��ˮ��֤NaCl��Һ������̪�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���¶ȡ�ѹǿһ���������£������غ������ع�ͬ����һ����ѧ��Ӧ�ķ��� | |
| B�� | �¶ȡ�ѹǿһ��ʱ�����ȵ������ӵķ�Ӧһ�����Է����� | |
| C�� | ��Ӧ�ʱ��Ǿ�����Ӧ�Ƿ��Է����е�Ψһ���� | |
| D�� | ������ܽ�������ر��й� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=1 | B�� | pH��1 | C�� | pH��1 | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��D��Ϊ�����D�ĺ˴Ź������״���2�����շ壬�����Ϊ1��1��
��D��Ϊ�����D�ĺ˴Ź������״���2�����շ壬�����Ϊ1��1�� ����Ӧ���ͣ���ȥ��Ӧ��
����Ӧ���ͣ���ȥ��Ӧ��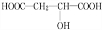 +HCOOH$?_{��}^{Ũ����}$
+HCOOH$?_{��}^{Ũ����}$ +H2O����Ӧ���ͣ�ȡ����Ӧ��
+H2O����Ӧ���ͣ�ȡ����Ӧ�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�32�������к���2NA��ԭ�� | |
| B�� | ��״���£�1L��ϩ��ȫȼ�պ���������̬����ķ�����Ϊ6NA/22.4 | |
| C�� | 78g Na2O2�����к��е���������ĿΪ2NA�� | |
| D�� | 1molNa2O2������CO2��Ӧת�Ƶĵ�������Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ����ʱ���Ƚ���Һ©�����²�Һ����¿ڷų����ٽ��ϲ�Һ����¿ڷų� | |
| B�� | ��������ʱ��Ӧʹ������е�ˮ����ȫ���ɺ���ֹͣ���� | |
| C�� | �������ʱ��Ӧ��������ƿ�м��뼸���ʯ���Է�ֹ���� | |
| D�� | ��ȡ����ʱ������ѡ��CCl4��ƾ���Ϊ��ȡ������ˮ����ȡ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 240 mL 0.2 mol•L-1��NaOH��Һ���ƣ���Ҫʹ����ƽ���ձ���250 mL����ƿ������ | |
| B�� | ��ȥCu���е�CuO�����������еμ�����ϡ�����ٹ��� | |
| C�� | Ϊ��ǿ��ˮ��Ư���ԣ������м���̼��� | |
| D�� | Ϊʹ0.5mol/L��NaNO3��Һ���ʵ���Ũ�ȱ�Ϊ1mol/L���ɽ�ԭ��Һ����������50��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ͭƬ�������������ɣ���ͭƬΪ������Ϊ���������һ�� | |
| B�� | ��������ỻ��ƻ��֭�������в����е������� | |
| C�� | װ���д��ڡ���ѧ�ܡ����ܡ����ܡ���ת�� | |
| D�� | �����пƬ������Ƭ����·�еĵ���������ͭƬ������������Ƭ����Ƭ����������Ӧ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com