
| 0.48 |
| 24 |
| c(CH 3COO -)?c(H +) |
| c(CH 3COOH) |
| 0.48 |
| 24 |
| c(CH 3COO -)?c(H +) |
| c(CH 3COOH) |


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④⑤ | B、①③⑥ |
| C、②④⑤⑥ | D、①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 光 |
| A、烧碱溶液 |
| B、溴水 |
| C、AgNO3溶液 |
| D、淀粉KI试剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1400℃ |
| 约3000℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
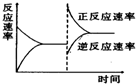 如图是关于反应A2(g)+3B2(g)=2C(g)(正反应为放热反应)的平衡移动图形,影响平衡移动的原因是( )
如图是关于反应A2(g)+3B2(g)=2C(g)(正反应为放热反应)的平衡移动图形,影响平衡移动的原因是( )| A、升高温度,同时加压 |
| B、降低温度,同时减压 |
| C、增大反应物浓度,同时使用催化剂 |
| D、增大反应物浓度,同时减小生成物浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管 |
| B、取10 mL该硫酸于烧杯中,再加入10mL的水,可配得49%的硫酸 |
| C、配制200mL4.6mol/L的稀硫酸需取该硫酸50 mL |
| D、该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com