
 .
. 分析 (1)无害的+5价砷类化合物在维生素C的作用下,能够转化为有毒的+3价的含砷化合物,As元素的化合价降低,则维生素C中某元素的化合价升高;
(2)As元素的化合价降低,得到电子,结合化合价变化计算转移电子;
(3)氧化还原反应中得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,还原剂对应的产物是氧化产物,根据元素化合价变化标出电子转移的方向和数目.
解答 解:(1)无害的+5价砷类化合物在维生素C的作用下,能够转化为有毒的+3价的含砷化合物,As元素的化合价降低,则维生素C中某元素的化合价升高,则维生素C具有还原性,故答案为:还原性;
(2)上述过程中+5价砷类物质得到电子,作为氧化剂,+5价砷元素发生反应还原;2mol+5价砷完全转化为+3价砷,共转移2mol×(5-3)×NA=4NA个电子,
故答案为:氧化剂;还原;4NA;
(3)该反应中,硝酸得电子作氧化剂,铁失电子作还原剂,铁对应的产物硝酸亚铁是氧化产物,该反应中铁失去电子数=3(2-0)=6,硝酸得电子数=2(5-2)=6,所以用双线桥法在化学方程式中表示出电子转移的方向和数目为: ,
,
故答案为: .
.
点评 本题考查氧化还原反应,为高考常见题型,题目难度中等,试题侧重于学生的分析能力和计算能力的考查,明确氧化还原反应的实质与特征为解答关键,注意从化合价的角度及电子守恒角度解答该题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaSO4难溶于水,在水中离子浓度很小,所以BaSO4是弱电解质 | |
| B. | 在水溶液中能导电的化合物就是电解质 | |
| C. | H2SO4在电流作用下在水中电离出H+和SO42- | |
| D. | 液态HCl,固态NaCl均不导电,但HCl、NaCl是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
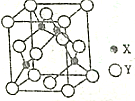 已知常见元素X的原子序数比常见元素Y的小,X的氢化物能与其最高价氧化物的水化物发生化合反应生成一种离子化合物M,Y元素的周期序数等于最外层电子数.回答下列问题:
已知常见元素X的原子序数比常见元素Y的小,X的氢化物能与其最高价氧化物的水化物发生化合反应生成一种离子化合物M,Y元素的周期序数等于最外层电子数.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | b=0.2a | B. | b=0.3a | C. | b=0.25a | D. | a=2b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
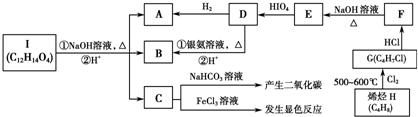
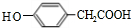 ,E
,E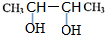 ;
; ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com