
 2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.| 温度(℃) | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
| 时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
分析 (1)①化学平衡常数K=$\frac{c(C{H}_{3}OC{H}_{3}).{c}^{3}({H}_{2}O)}{{c}^{2}(C{O}_{2}).{c}^{6}({H}_{2})}$;
②可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的物质的量、物质的量浓度、百分含量不变,由此引起的一系列物理量不变;
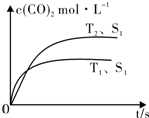
(2)①根据先拐先平数值大知,T1>T2,升高温度,二氧化碳浓度降低,说明正反应是放热反应;
②催化剂只改变反应速率不改变平衡移动,所以平衡时二氧化碳浓度不变,但反应到达平衡的时间缩短;
(3)①该反应的浓度商=$\frac{0.8}{0.4×0.{4}^{2}}$=12.5>K,平衡逆向移动;
②根据表中数据知,20min时该反应达到平衡状态,恒温恒容条件下,反应前后气体物质的量之比等于其压强之比,反应后压强是反应前的0.70倍,则反应后气体物质的量=0.70×(1+2)mol=2.1mol,根据方程式知,参加反应的n(CO)为反应前后气体减少物质的量的一半,所以参加反应的n(CO)=(1+2-2.1)mol×$\frac{1}{2}$=0.45mol,据此计算其转化率;
(4)根据盖斯定律计算其反应热,从而确定三个焓变关系;
(5)燃料碱性电池中,正极上氧气得电子和水反应生成氢氧根离子.
解答 解:(1)①化学平衡常数K=$\frac{c(C{H}_{3}OC{H}_{3}).{c}^{3}({H}_{2}O)}{{c}^{2}(C{O}_{2}).{c}^{6}({H}_{2})}$,故答案为:$\frac{c(C{H}_{3}OC{H}_{3}).{c}^{3}({H}_{2}O)}{{c}^{2}(C{O}_{2}).{c}^{6}({H}_{2})}$;
②A.容器中气体质量不变、容器体积不变,所以容器中密度始终不变,则不能根据密度判断平衡状态,故错误;
B.单位时间内消耗2molCO2,同时消耗1mol二甲醚也同时生成1mol二甲醚,二甲醚正逆反应速率相等,该反应达到平衡状态,故正确;
C.无论反应是否达到平衡状态都存在v(CO2):v(H2)=1:3,所以不能据此判断平衡状态,故错误;
D.反应前后气体物质的量之和减小,所以反应前后气体压强改变,当容器内压强保持不变时,该反应达到平衡状态,故正确;
故选BD;
(2)①根据先拐先平数值大知,T1>T2,升高温度,二氧化碳浓度降低,说明正反应是放热反应,则焓变小于0,故答案为:<;
②催化剂只改变反应速率不改变平衡移动,所以平衡时二氧化碳浓度不变,但反应到达平衡的时间缩短,其图象为 ,
,
故答案为: ;
;
(3)①该反应的浓度商=$\frac{0.8}{0.4×0.{4}^{2}}$=12.5>K,平衡逆向移动,则正反应速率小于逆反应速率,故答案为:<;
②根据表中数据知,20min时该反应达到平衡状态,恒温恒容条件下,反应前后气体物质的量之比等于其压强之比,反应后压强是反应前的0.70倍,则反应后气体物质的量=0.70×(1+2)mol=2.1mol,根据方程式知,参加反应的n(CO)为反应前后气体减少物质的量的一半,所以参加反应的n(CO)=(1+2-2.1)mol×$\frac{1}{2}$=0.45mol,所以CO转化率=$\frac{0.45mol}{1mol}×100%$=45%,
故答案为:45%;
(4)由反应4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H1 ①
4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H2 ②
4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H3③
则反应$\frac{3②+2③}{5}$可得到反应①,则△H1=$\frac{3△{H}_{2}+2△{H}_{3}}{5}$,故答案为:△H1=$\frac{3△{H}_{2}+2△{H}_{3}}{5}$;
(5)燃料碱性电池中,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-,故答案为:O2+2H2O+4e-=4OH-.
点评 本题考查较综合,涉及原电池原理、盖斯定律、化学平衡常数有关计算等知识点,为高频考点,只有反应前后改变的物理量才能作为平衡状态判断依据,难点是电极反应式的书写及平衡移动方向判断,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | CaCO3+H2O+CO2═Ca(HCO3)2 | B. | AgNO3+NaCl═AgCl↓+NaNO3 | ||
| C. | Na2CO3+Ca(OH)2═CaCO3↓+2NaOH | D. | KCl+NaOH═NaCl+KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
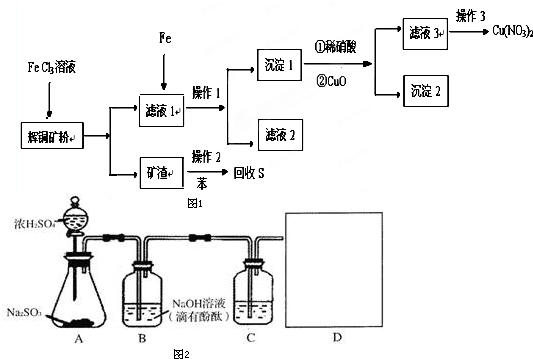
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
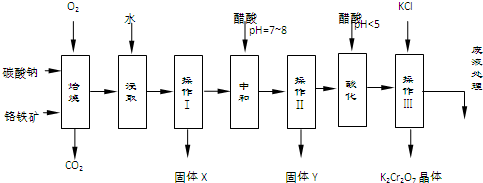
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
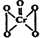 ),该反应可用来检验Cr2O72-的存在.写出反应的离子方程4H2O2+Cr2O72-+2H+═2CrO5+5H2O.该反应不属于(填“属于”或“不属于”)氧化还原反应.
),该反应可用来检验Cr2O72-的存在.写出反应的离子方程4H2O2+Cr2O72-+2H+═2CrO5+5H2O.该反应不属于(填“属于”或“不属于”)氧化还原反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH和CH3COOH OH-+H+=H2O | |
| B. | 过量的CO2与NaOH溶液 CO2+2OH-=CO32-+H2O | |
| C. | Ba(OH)2+H2SO4=BaSO4+2H2O Ba2++SO42+=Ba SO4 | |
| D. | NaHS+HCl=NaCl+H2S HS++H+=H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
①分离饱和食盐水与沙子的混合物 | ②分离水和汽油的混合物 | ③分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物,CCl4和甲苯互溶 | ④提取出碘水中的碘单质 |
| D | B | C | A |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com