
| m |
| M |
| n |
| V |
| N |
| NA |
| 92g |
| 46g/mol |
| 2mol |
| 0.5L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
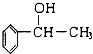 )互为同系物.
)互为同系物.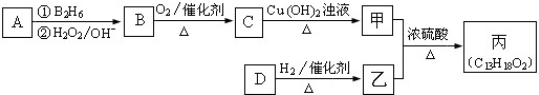
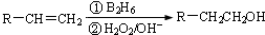
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化碳的水溶液能导电,所以二氧化碳是电解质 |
| B、1mol?L-1的硫酸钠溶液和1mol?L-1的氢氧化钠溶液,分别做导电性实验,两种溶液的导电性不同 |
| C、氢氧化铁胶体能导电,故氢氧化铁胶体是电解质 |
| D、在相同温度下,饱和溶液一定比不饱和溶液的导电性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 成分 | 质量(g) | 摩尔质量(g?mol-1) |
| 蔗糖(C12H22O11) | 25.00 | 342 |
| 硫酸钾 | 0.25 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.25 | 158 |
| 硝酸银 | 0.02 | 170 |
查看答案和解析>>
科目:高中化学 来源: 题型:
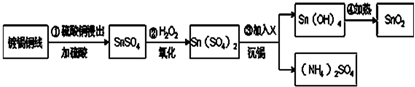
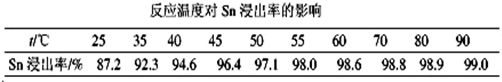
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Na+2H2O═2NaOH+H2↑ | ||||
B、C+H2O(g)
| ||||
| C、CaO+H2O═Ca(OH)2 | ||||
| D、Cl2+H2O═HCl+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
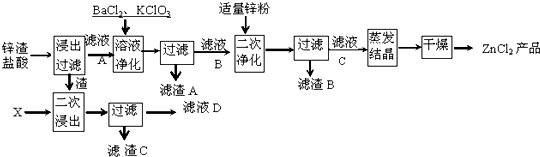
查看答案和解析>>
科目:高中化学 来源: 题型:
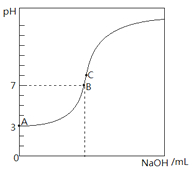 常温下,下图是用0.1000mol/L NaOH溶液滴定20.00mL0.1000mol/L HA溶液所得到滴定曲线.下列相关的说法错误的是( )
常温下,下图是用0.1000mol/L NaOH溶液滴定20.00mL0.1000mol/L HA溶液所得到滴定曲线.下列相关的说法错误的是( )| A、由图可知HA是一种弱酸,且Ka=1.0×10-5 |
| B、滴定到B点时,c(Na+)=c(A-) |
| C、当NaOH溶液的体积为10.00mL时,有c(A-)+c(OH-)=c(H+)+c(HA) |
| D、C点溶液中的离子浓度关系为:c(Na+)>c(A-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
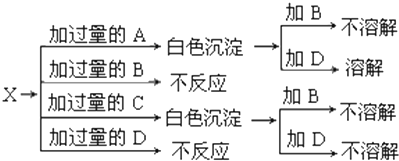 如图中A、B、C、D分别是KNO3、KOH、HNO3和Ba(NO3)2四种溶液中的一种,现利用另一种溶液X,用如图所示的方法可将它们依次确定.
如图中A、B、C、D分别是KNO3、KOH、HNO3和Ba(NO3)2四种溶液中的一种,现利用另一种溶液X,用如图所示的方法可将它们依次确定.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com