
【题目】25℃,CH3COOH的电离常数Ka=1.75×10-5。
(1)计算0.1 mol·L-1的CH3COOH溶液中c(H+)=__________________;
(2)0.1 mol·L-1的CH3COOH和0.1 mol·L-1的CH3COONa的混合溶液中,c(H+)=_____________;
(3)25°C,将0.1 mol·L-1的CH3COOH溶液加水稀释,请填写下列表达式中的数据情况(填“变大”、“变小”或“不变”)。
①![]() =____________;
=____________;
②![]() =____________;
=____________;
③![]() =____________;
=____________;
④![]() =____________。
=____________。
【答案】1.32×10-3 mol·L-1 1.75×10-5 mol·L-1 变小 不变 变大 不变
【解析】
0.1 mol/L醋酸溶液中,存在电离平衡CH3COOH![]() H++CH3COO-
H++CH3COO-
(1)CH3COOH是弱酸,存在电离平衡,可用三段式计算,设溶液中H+浓度为![]() ,
,
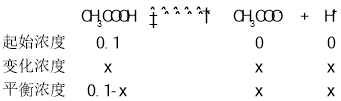
根据Ka=![]() 带入数据,x=1.32×10-3 mol·L-1,则0.1 mol·L-1的CH3COOH溶液中c(H+)=1.32×10-3 mol·L-1。
带入数据,x=1.32×10-3 mol·L-1,则0.1 mol·L-1的CH3COOH溶液中c(H+)=1.32×10-3 mol·L-1。
(2)0.1 mol·L-1的CH3COOH和0.1 mol·L-1的CH3COONa的混合溶液中, 设溶液中H+浓度为![]() ,列三段式如下
,列三段式如下
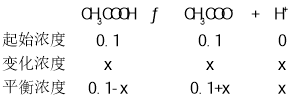
Ka=![]() ,x=1.75×10-5 mol·L-1 则c(H+)=1.75×10-5 mol·L-1
,x=1.75×10-5 mol·L-1 则c(H+)=1.75×10-5 mol·L-1
(3)将①做如下改变,![]() =
=![]() ,Ka在稀释过程中不变,
,Ka在稀释过程中不变,![]() 减小,则①表达式数据变小;
减小,则①表达式数据变小;
②![]() =Ka,Ka只与温度有关,所以②表达式数据不变;
=Ka,Ka只与温度有关,所以②表达式数据不变;
③![]() =
=![]() ,Ka在稀释过程中不变,
,Ka在稀释过程中不变,![]() 减小,则③表达式数据变大;
减小,则③表达式数据变大;
④![]() ,Ka及KW在稀释过程中不变,则④表达式数据不变。
,Ka及KW在稀释过程中不变,则④表达式数据不变。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】室温下,用0.10 mol·L-1KOH溶液滴定10.00 mL 0.10 mol·L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答下列问题:
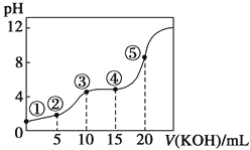
(1)点①所示溶液中,Kw=__________。
(2)点②所示溶液中的电荷守恒式为______________________________________。
(3)点③所示溶液中存在________种平衡。
(4)点④所示溶液中的物料守恒式为0.10 mol·L-1=___________________________。
(5)点⑤所示溶液中各离子浓度的大小顺序为________________________________。
(6)上述5点所示溶液中,水的电离程度最大的是_______,最小的是________(用序号回答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物F是一种重要的有机合成中间体,其合成路线如下图所示:
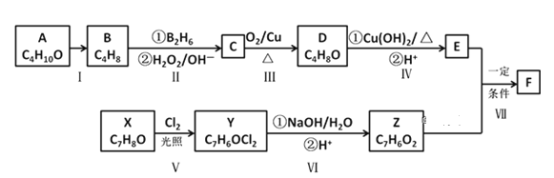
已知:①A的核磁共振氢谱图中显示两组峰
②F的结构简式为:
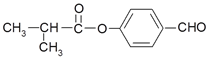
③通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
④R-CH=CH2![]() R-CH2CH2OH
R-CH2CH2OH
请回答下列问题:
(1)A的名称为______________(系统命名法);Z中所含官能团的名称是___________。
(2)反应Ⅰ的反应条件是__________。
(3)E的结构简式为_______________________。
(4)写出反应Ⅴ的化学方程式____________________________________________。
(5)写出反应IV中的化学方程式____________________________________________。
(6)W是Z的同系物,相对分子质量比Z大14,则W的同分异构体中满足下列条件:
①能发生银镜反应,②苯环上有两个取代基,③不能水解,遇FeCl3溶液不显色的结构共有_________种(不包括立体异构),核磁共振氢谱有四组峰的结构为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下来事实不能说明NH3·H2O为弱电解质的是
A. 0.1 mol·L-1NH3·H2O的pH小于13
B. 0.1 mol·L-1 NH4Cl溶液的pH小于7
C. 相同条件下,浓度均为0.1 mol·L-1 NaOH溶液和氨水,氨水的导电能力弱
D. 0.1 mol·L-1NH3·H2O能使无色酚酞试液变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以二氧化锰为原料制取高锰酸钾晶体的实验流程如下:

下列说法正确的是
A. “灼烧”可在石英坩埚中进行
B. 母液中的溶质是K2CO3、KHCO3、KCl
C. “结晶”环节采用加热蒸发结晶的方法
D. “转化”反应中,生成的KMnO4和MnO2的物质的量之比为2︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯是高效、低毒的消毒剂。已知:ClO2是极易溶于水的气体,实验室制备及性质探究装置如图所示。回答下列问题:
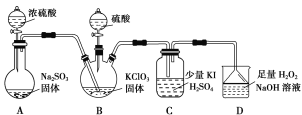
(1)装置B用于制备ClO2,同时还生成一种酸式盐,该反应的化学方程式为___________。装置C中滴有几滴淀粉溶液,反应时有蓝色岀现。淀粉的作用是______。
(2)装置C的导管靠近而不接触液面,其目的是________。
(3)用ClO2消毒自来水,其效果是同质量氯气的______倍(保留一位小数)。
(4)装置D用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是2∶1,则还原产物的化学式是___________。
(5)若将装置C中的溶液改为Na2S溶液,通入ClO2后溶液无明显现象。由此可以产生两种假设:
假设a:ClO2与Na2S不反应。
假设b:ClO2与Na2S反应。
①你认为哪种假设正确,阐述原因:___________。
②请设计实验证明你的假设(仅用离子方程式表示):__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于盐类水解的应用中,说法正确的是( )
A. 加热蒸干Na2CO3溶液,最后可以得到NaOH和Na2CO3的混合固体
B. 除去MgCl2中的Fe3+,可以加入NaOH固体
C. 明矾净水的反应:Al3++3H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
D. 加热蒸干KCl溶液,最后得到KOH固体(不考虑与CO2的反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将①H+、②Cl-、③Al3+、④K+、⑤S2-、⑥OH-、⑦NO3-、⑧NH4+分别加入H2O中,基本上不影响水的电离平衡的离子是( )
A.①③⑤⑦⑧B.②④⑥⑧C.①⑥D.②④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中含有的Cr2O72-和CrO42-会对水体产生很大的危害,因此这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下:
CrO42—![]() Cr2O72-
Cr2O72-![]() Cr3+
Cr3+![]() Cr(OH)3↓
Cr(OH)3↓
①中反应为2 CrO42-(黄色)+2H+Cr2O72-(橙色)+H2O。
下列说法正确的是
A.①中,酸化后废水黄色变浅
B.②中,反应的氧化剂与还原剂的物质的量之比为3︰1
C.③中,所得沉淀Cr(OH)3中含有Fe(OH)3
D.①中,所加酸可以是盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com