
【题目】二氧化氯是高效、低毒的消毒剂。已知:ClO2是极易溶于水的气体,实验室制备及性质探究装置如图所示。回答下列问题:
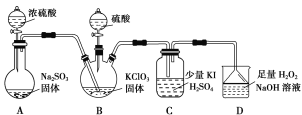
(1)装置B用于制备ClO2,同时还生成一种酸式盐,该反应的化学方程式为___________。装置C中滴有几滴淀粉溶液,反应时有蓝色岀现。淀粉的作用是______。
(2)装置C的导管靠近而不接触液面,其目的是________。
(3)用ClO2消毒自来水,其效果是同质量氯气的______倍(保留一位小数)。
(4)装置D用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是2∶1,则还原产物的化学式是___________。
(5)若将装置C中的溶液改为Na2S溶液,通入ClO2后溶液无明显现象。由此可以产生两种假设:
假设a:ClO2与Na2S不反应。
假设b:ClO2与Na2S反应。
①你认为哪种假设正确,阐述原因:___________。
②请设计实验证明你的假设(仅用离子方程式表示):__________。
【答案】SO2+H2SO4+2KClO3=2KHSO4+2ClO2 通过检验I2的存在,证明ClO2有强氧化性 使ClO2尽可能多的与溶液反应,并防止倒吸 2.6 NaClO2 假设b正确, S2-的还原性强于I-,所以ClO2也能氧化S2-或ClO2是强氧化剂,S2-具有强还原性 SO42-+Ba2+=BaSO4↓
【解析】
浓硫酸和亚硫酸钠反应生成二氧化硫,A制备二氧化硫,B用于制备ClO2,同时还生成一种酸式盐,则B中发生反应SO2+H2SO4+2KClO3═2KHSO4+2ClO2,ClO2是一种黄绿色易溶于水的气体,具有强氧化性,所以C中发生氧化还原反应生成碘,注意防倒吸,装置C中滴有几滴淀粉溶液,碘遇淀粉变蓝色;装置D用于吸收尾气,反应生成NaClO2,双氧水作还原剂生成氧气,从而防止尾气污染环境,据此解答。
(1)装置B用于制备ClO2,同时还生成一种酸式盐,根据元素守恒知,酸式盐为硫酸氢钠,该反应的化学方程式为SO2+H2SO4+2KClO3═2KHSO4+2ClO2;装置C中滴有几滴淀粉溶液,淀粉遇碘变蓝色,根据淀粉是否变色来判断是否有碘生成,从而证明二氧化氯具有氧化性;
(2)ClO2是极易溶于水的气体,所以检验其强氧化性时导管靠近而不接触液面,以防倒吸;
(3)1molCl2即71g消毒时转移2mol电子,71gClO2消毒时转移电子为![]() ×(4+1)=5.2mol,其效果是同质量氯气的
×(4+1)=5.2mol,其效果是同质量氯气的![]() =2.6倍;
=2.6倍;
(4)装置D用于吸收尾气,H2O2作还原剂生成O2,H2O2O22e,生成1molO2转移电子2mol,则2molClO2得到2mol电子生成2molNaClO2;
(5)①由于ClO2具有强氧化性,Na2S具有强还原性,二者不可能不反应,所以假设a错误,假设b正确;
②ClO2氧化Na2S后溶液无明显现象,说明ClO2将S2氧化生成更高价的酸根SO42,所以可通过检验SO42的存在以证明ClO2与Na2S发生氧化还原反应,所用试剂为稀盐酸和BaCl2溶液,离子反应为:SO42+Ba2+═BaSO4↓。


科目:高中化学 来源: 题型:
【题目】可逆反应mA(s)+nB(g)![]() cC(g)+fD(g)反应过程中,当其它条件不变时,C的体积分数(C%)与温度(T)和压强(P)的关系如图所示(T2>T1),下列叙述正确的是( )
cC(g)+fD(g)反应过程中,当其它条件不变时,C的体积分数(C%)与温度(T)和压强(P)的关系如图所示(T2>T1),下列叙述正确的是( )

A.达到平衡后,若使用催化剂,C的体积分数增大
B.达到平衡后,若使温度升高,化学平衡向逆反应方向移动
C.化学方程式中n>c+f
D.达到化学平衡后,增加A的量有利于化学平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热反应原理可以应用在生产上,如用于焊接钢轨等,实验室铝热反应的实验装置如图所示。
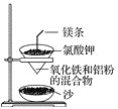
(1)镁条的作用是___。
(2)写出该反应的化学方程式:___;在冶金工业上也常用这一反应原理来冶炼__(填字母)。
A.不活泼金属 B.较活泼金属
C.稀有金属 D.高熔点金属
(3)为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验:
①若取ag样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为bL。反应的离子方程式是___;样品中铝的质量为___g。
②另取ag样品将其点燃,恰好完全反应,反应产物冷却后,加入足量盐酸,测得生成的气体体积为cL,该气体与(1)中所得气体的体积比c∶b=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值。下列说法正确的是( )
A.常温常压下,11.2 L SO2含有的氧原子数小于NA
B.0. 1 mol Na2O2和Na2O的混合物中含有的离子总数等于0.4NA
C.10 g质量分数为34%的H2O2溶液含有的氢原子数为0.2NA
D.100 mL 0.1 mol/L醋酸中含有的醋酸分子数是0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,CH3COOH的电离常数Ka=1.75×10-5。
(1)计算0.1 mol·L-1的CH3COOH溶液中c(H+)=__________________;
(2)0.1 mol·L-1的CH3COOH和0.1 mol·L-1的CH3COONa的混合溶液中,c(H+)=_____________;
(3)25°C,将0.1 mol·L-1的CH3COOH溶液加水稀释,请填写下列表达式中的数据情况(填“变大”、“变小”或“不变”)。
①![]() =____________;
=____________;
②![]() =____________;
=____________;
③![]() =____________;
=____________;
④![]() =____________。
=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在容积为2 L的密闭容器中发生反应2X(g)+Y(g)![]() 2W(g) ΔH<0,当充入2 mol X和1 mol Y,经20 s达到平衡时生成了0.4 mol W。下列说法正确的是( )
2W(g) ΔH<0,当充入2 mol X和1 mol Y,经20 s达到平衡时生成了0.4 mol W。下列说法正确的是( )
①升高温度,W的体积分数减小,ΔH增大 ②以Y的浓度变化表示的反应速率为0.01 mol·L-1·s-1 ③在其他条件不变的情况下,增加1 mol X,则X和Y的转化率均提高 ④增大压强,正反应速率增大,逆反应速率减小,则平衡向正反应方向移动 ⑤再向容器中通入2 mol X和1 mol Y,达到平衡时,X、Y的转化率均增大
A. ⑤ B. ①⑤ C. ②③④ D. ④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于盐类水解的说法错误的是( )
A.浓度均为0.1 mol·L-1的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2溶液中,c(NH4+)的大小顺序为①>②>③
B.pH相等的①NaHCO3、②Na2CO3、③NaOH溶液的物质的量浓度大小:①>②>③
C.在NH4Cl溶液中加入稀HNO3,能抑制NH4+水解
D.将硫酸亚铁溶液加热蒸干得不到原溶质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.20mol/L的NaOH溶液滴定10.00mL0.20mol/L的NaHSO3溶液,滴定过程中溶液的pH变化和滴加NaOH溶液的体积关系如图所示。下列说法错误的是( )
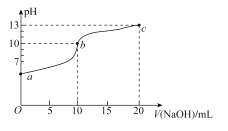
A.溶液中水的电离程度:b>a>c
B.pH=7时,消耗的V(NaOH)<10.00mL
C.在室温下K2(H2SO3)约为1.0×10-7
D.c点溶液中c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,可用废镍催化剂(主要含Ni、Al,少量Cr、FeS 等)来制备,其工艺流程如下:

回答下列问题:
(1)“浸泡除铝”时,发生反应的离子反应方程式为_________________________;
(2)“溶解”时放出的气体为_______________ (填化学式);
(3)已知该条件下金属离子开始沉淀和完全沉淀的pH如下表:
开始沉淀的pH | 完全沉淀的pH | |
Ni2+ | 6.2 | 8.6 |
Fe2+ | 7.6 | 9.1 |
Fe3+ | 2.3 | 3.3 |
Cr3+ | 4.5 | 5.6 |
“调pH 1”时,溶液pH范围为______________________;
(4)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式_____________;

(5)金属铬在溶液中有多种存在形式, CrO42—和Cr2O72—在溶液中可相互转化。室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c(Cr2O72—)随c(H+)的变化如图所示,用离子方程式表示Na2CrO4溶液中的转化反应________________,根据A点数据计算出该转化反应的平衡常数为______________,温度升高,溶液中CrO42—的平衡转化率减小,则该反应的△H____0(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com