
2015年4月,于敏获颁“影响世界华人终身成就奖”。“钚--239”是“于敏型”氢弹
的重要原料。下列说法正确的是
A.239Pu原子的原子核中含有239个质子
B.238Pu、239Pu和241Pu属于不同的核素
C.238Pu与238U在元素周期表中的位置相同
D.239Pu衰变成235U属于化学变化
科目:高中化学 来源:2015-2016学年湖南师大附属中学高一上三次阶段测化学卷(解析版) 题型:填空题
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①SO2中S元素处于中间价态,既有氧化性又有还原性;
②将SO2通入酸性KMnO4溶液中,溶液由紫红色褪至无色,SO2表现出 性质。
A.氧化性 B.还原性 C.既有氧化性又有还原性
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成。其中SiO2属于 (填“酸性”、“碱性”或“两性”,下同)氧化物,Al2O3属于 氧化物。
②现取一份蛇纹石试样进行实验:
Ⅰ.先将其溶于过量的盐酸中,过滤,滤渣的主要成分是 ;
Ⅱ.再向滤液中加入NaOH溶液至过量,过滤,滤渣中的主要成分是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川阆中中学校高二上第二次段考化学试卷(解析版) 题型:选择题
把一小块钠投入水中,不会出现的现象是
A.钠浮在水面上 B.钠熔化成银白色的小球,不停地游动
C.溶液由无色变为红色 D.发出“嘶嘶”响声
查看答案和解析>>
科目:高中化学 来源:2016届天津市高三上12月学业调研化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.相同物质的量的OH-和CH3+含有相同数目的电子
B.25℃时,pH=13的1.0 LBa(0H)2溶液中含有的OH-数目为0.2NA
C.标准状况下,2.24LCl2通入足量H2O或NaOH溶液中转移的电子数均为0.2NA
D.常温常压下,4.4gCO2和N2O混合物中所含有的原子数为0.3 NA
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期12月阶段测化学试卷(解析版) 题型:推断题
铁及其化合物有重要用途,如聚合硫酸铁[Fe2(0H)n(S04)3-n/2]m是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:
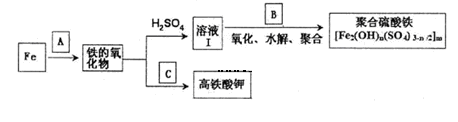
请回答下列问题:
(1)若A为H20(g),可以得到Fe304,写出其转化的化学方程式: 。
(2)若C为KNO3和KOH的混合物,写出其与Fe2O3加热共融制得高铁酸钾的化学方程式 并配平:

(3)为测定溶液Ⅰ中铁元素的总含量,实验操作:准确量取20.00mL溶液Ⅰ于带塞锥形瓶中,加入足量H202 ,调节pH<3,加热除去过量H202 ;加入过量KI充分反应后,再用 O.1OOOmol.L-1 Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。
已知:2Fe3++2I-=2Fe2++I2 I2+2S2O32-=2I-+S4O62-
①写出滴定选用的指示剂 ,滴定终点观察到的现象 。
②溶液Ⅰ中铁元素的总含量为 g.L-1。若滴定前溶液中H202没有除尽,所测定的铁元素的含量将会 (填“偏高” “偏低” “不变”)。
(4)将3.48gFe3O4完全溶解在100mL 1 mol·L-1H2SO4溶液中,然后加入K2Cr2O7溶液25mL,恰好使溶液中的Fe2+全部反应,Cr2O72-转化为Cr3+。则K2Cr2O7溶液的物质的量浓度为
查看答案和解析>>
科目:高中化学 来源:2015-2016年海南省高一上第三次月考化学试卷(解析版) 题型:选择题
10g镁铝合金与足量的氢氧化钠溶液反应后,生成气体3.36L(标准状况),则此合金中含镁的质量分数为
A.35.6% B.27% C.10% D.73%
查看答案和解析>>
科目:高中化学 来源:2015-2016年海南省高一上第三次月考化学试卷(解析版) 题型:选择题
以下氧化物既可以与酸反应,又可以与碱反应的是
A.FeO B.Fe2O3 C.Al2O3 D.Fe3O4
查看答案和解析>>
科目:高中化学 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:选择题
下列图像能正确地表达可逆反应3A(g) + B(g) 2C(g) (△H<0) 的是
2C(g) (△H<0) 的是
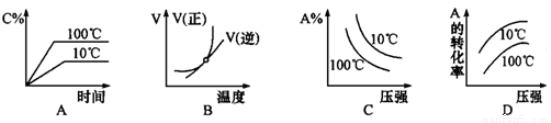
查看答案和解析>>
科目:高中化学 来源:2015-2016年山东省高一上12月月考化学试卷(解析版) 题型:填空题
某同学采用如图装置进行实验,证明了铜与稀硝酸反应生成了NO。实验时,先向注射器内加入一定量的稀硝酸,排净注射器内的空气,迅速将带有铜丝的橡皮帽盖上,一段时间后,注射器内有无色气体产生。
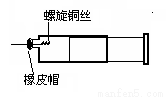
(1)请写出铜与稀硝酸反应的化学方程式__________________。
(2)若证明无色气体是NO的实验操作和现象是________________。
一氧化氮是大气污染物之一。目前,有一种治理方法是在400 ℃左右、有催化剂存在的情况下,用氨把一氧化氮还原为氮气和水。该反应的化学方程式为4NH3+6NO 5N2+6H2O,每有10mol N2生成,氧化产物与还原产物的比___________,反应中转移的电子的电子数为___________。
5N2+6H2O,每有10mol N2生成,氧化产物与还原产物的比___________,反应中转移的电子的电子数为___________。
(3)若将上述稀硝酸换成浓硝酸,其生成的气体通入水中,发生反应的化学方程式为____________。
(4)分别将等质量的铜片与等体积过量的浓、稀硝酸反应,所得溶液前者呈绿色,后者呈蓝色。某同学认为可能是Cu2+浓度的差异引起的,你认为是否正确? (填“正确”或“不正确”),理由是 。
(5)①写出实验室由NH4Cl和Ca(OH)2加热制取氨气的化学方程式:__________________;检验氨 气已收集满的方法是: 。
②进行喷泉实验,若在水中加入酚酞,得到红色喷泉。该实验体现了氨气的两个重要性质分别是_______________、______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com