
青蒿素是一种高效、速效抗疟药,是中医药献给世界的一份礼物。屠呦呦因在发现、研究青蒿素方面做出的杰出贡献而获得2015年诺贝尔医学奖。青蒿素分子结构如下图,下列说法中正确的是

A.青蒿素能与热的NaOH溶液反应
B.青蒿素的分子式为C15H21O5
C.青蒿素分子结构中只含有极性键
D.青蒿素能使酸性KMnO4溶液、溴的CCl4溶液分别褪色
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源:2016-2017学年江苏省高二学业水平测试化学试卷(解析版) 题型:选择题
高炉炼铁中存在反应:3CO+Fe2O3 3CO2+2Fe。下列说法正确的是
3CO2+2Fe。下列说法正确的是
A. CO是氧化剂 B. CO是还原剂
C. CO既是氧化剂又是还原剂 D. CO既不是氧化剂又不是还原剂
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省哈尔滨市高三二模理科综合化学试卷(解析版) 题型:填空题
金属镓是一种广泛用于电子工业和通讯领域的重要金属,化学性质与铝元素相似。
(1)工业上提纯镓的方法很多,其中以电解精炼法为多。具体原理如下:以待提纯的粗镓(内含Zn、Fe、Cu杂质)为阳极,以高纯镓为阴极,以NaOH水溶液为电解质溶液。在电流作用下使粗镓在阳极溶解进入电解质溶液,并通过某种离子迁移技术到达阴极并在阴极放电析出高纯镓。
①已知离子氧化性顺序为:Zn2+<Ga3+<Fe2+<Cu2+。电解精炼镓时阳极泥的成分是_________________。
②GaO2-在阴极放电的电极方程式是_______________________。
(2)工业上利用柜台Ga与NH3高温条件下合成固体半导体材料氮化镓(GaN)同时又有氢气生成。反应中每生成3mol H2时就会放出30.8kJ热量。
①该反应的热化学方程式为__________________。
②一定条件下,加入一定量的Ga与NH3进行上述反应,下列叙述符合事实且可作为判断反应已达到平衡状态的标志的是_________________。
A.恒温恒压下,混合气体的密度不变
B.断裂3molH-H键,同时断裂2molN-H键
C.恒温恒压下达平衡,加入2molH2使平衡移动,NH3的消耗速率等于原平衡时NH3的消耗速率
D.升高温度,氢气的生成速率先增大再减小,最后不变
(3)在密闭容器中,充入一定量的Ga与NH3发生反应,实验测得反应平衡体系中NH3的体积分数与压强的关系曲线如图1所示。


①比较图1中A点和C点化学平衡常数的大小关系:K1A1________________K1C1,(填“<”、“=”或“>”),理由是________________________________
②在T1和P6的条件下,往密闭容器中充入2molNH3和足量的Ga,该反应在第5min时达到平衡,此时容器的体积为3L。
a.若温度保持T1℃不变,压强恒定在P7的条件下重新达到平衡状态A(P7、50%)时,容器的体积变为起始体积的______________倍。
b.若T1和P6条件下反应至3min时刻,改变条件并与D点处达到平衡,H2的浓度随反应时间的变化趋势如图2所示(3~4min的浓度变化未表示出来),则改变的条件为_________(仅改变温度或压强中的一种)
(4)在工业上利用N2(g)+3H2(g)  2NH3(g)合成氮气。对于气相反应,用某组份(B)的平衡压强(PB)代替物质的量浓度(CB)也可以表示平衡常数(记作Kp),且PB=P×B的体积分数。则该反应的化学平衡常数表达式(Kp)是_____。恒温恒压下,在一容积可变的容器中,该反应达到平衡状态时,N2、H2、NH3各1mol,若此时再充入3molN2,则平衡_________移动(填“正向”、“逆向”或“不”)。
2NH3(g)合成氮气。对于气相反应,用某组份(B)的平衡压强(PB)代替物质的量浓度(CB)也可以表示平衡常数(记作Kp),且PB=P×B的体积分数。则该反应的化学平衡常数表达式(Kp)是_____。恒温恒压下,在一容积可变的容器中,该反应达到平衡状态时,N2、H2、NH3各1mol,若此时再充入3molN2,则平衡_________移动(填“正向”、“逆向”或“不”)。
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三适应性月考(六)理综化学试卷(解析版) 题型:选择题
短周期元素A、B. C. D最高价氧化物对应的水化物分别为X、Y、Z、W、A是短周期中原子半径最大的元素,常温下X、W均能与Y反应,A、C、D的原子序数及0.1mol/LX、Z、 W溶液的pH如图所示(已知1g2=0.3)。下列说法正确的是
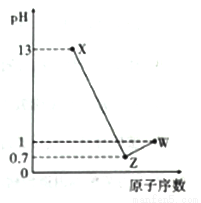
A. A的简单离子半径是这些元素中最小的
B. B与D两种元素可形成共价化合物
C. 气态氢化物的热稳定性:C>D
D. Z的盐溶液一定能促进水的电离
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三下学期周练(四)理科综合化学试卷(解析版) 题型:实验题
铁是人类较早使用的金属之一,铁及其化合物在现代社会各个领域仍有广泛的应用。
I.氧化物—Fe2O3:用工业FeCl3粗品(含Ca、Mn、Cu等杂质离子)制取高纯铁红,实验室常用萃取剂X(甲基异丁基甲酮)萃取法制取高纯铁红的主要实验步骤如下:

已知:HCl(浓) + FeCl3 HFeCl4 。试回答下列问题:
HFeCl4 。试回答下列问题:
(1)用萃取剂X萃取,该步骤中:
① Ca2+、Mn2+、Cu2+等杂质离子主要在__________(填“水”或“有机”)相。
② 若实验时共用萃取剂X 150mL,萃取率最高的方法是__________(填字母)。
a.一次性萃取,150mL b.分2次萃取,每次75mL c.分3次萃取,每次50mL
(2)用高纯水反萃取,萃取后水相中铁的存在形式是________________(写化学式);反萃取能发生的原因是___________________。
(3)所得草酸铁沉淀需用冰水洗涤,其目的一是洗去沉淀表面吸附的杂质离子,二是________________。
(4)测定产品中铁的含量需经酸溶、还原为Fe2+,然后在酸性条件下用标准K2Cr2O7溶液滴定,已知铬的还原产物为Cr3+,写出该滴定反应的离子方程式 ___________________。
II.含氧酸盐—铁酸铜(CuFe2O4)是很有前景的热化学分解水制氢的材料,CuFe2O4在制氢过程中可以循环使用。在热化学循环分解水制氢的过程中,铁酸铜(CuFe2O4)先要煅烧成氧缺位体(CuFe2O4-a),氧缺位值(a)越大,活性越高,制氢越容易。
(5)根据以上提示,写出氧缺位体与水常温下反应制氢的化学方程式____________。
(6)课外小组将铁酸铜样品在N2的气氛中充分煅烧,得氧缺位体的质量为原质量的96.6%,则氧缺位值(a)=__________。(结果保留小数点后2位)
查看答案和解析>>
科目:高中化学 来源:2017届贵州省贵阳市高三下学期第六次适应性考试理综化学试卷(解析版) 题型:简答题
2015年10月,我国著名药学家屠呦呦因发现治疗疟疾新型药物青蒿素和双氢靑蒿素而获得2015年诺贝尔生理学或医学奖,成为首位获得诺贝尔科学奖的华人女科学家,震惊世界,感动中国。青蒿素(C15H22O5)的结构如图甲所示。请回答下列问题:

(1)组成靑蒿素的三种元素电负性由大到小的顺序是_________;在基态O原子中,核外存在________对自旋方向相反的电子。
(2)下列关于青蒿素的说法正确的是_______(填序号)。
a.青蒿素中既存在极性键又存在非极性键
b.在青蒿素分子中,所有碳原子均处于同一平面
c.图中数字标识的五个碳原子均只以σ键与其他原子成键
(3)在确定青蒿素结构的过程中,可采用硼氢化钠(NaBH4)作为还原剂,其制备方法为4NaH+ B(OCH3)3 NaBH4+3CH3ONa。
NaBH4+3CH3ONa。
①NaH为______晶体,图乙是NaH晶胞结构,则NaH晶体的配位数是______;若晶胞棱长为a,则Na原子间最小核间距为_______。
②B(OCH3)3中B采用的杂化类型是__________。写出一种与B(OCH3)3具有相同空间构型的分子或离子:______________________。
③NaBH4结构如图丙所示,结构中存在的作用力有__________。NaBH4是有机化学中的一种常用还原剂,其在热水中水解生成偏硼酸钠和氢气,该反应的化学方程式为______________。
(4)硼(B)及其化合物在化学中有重要的地位。科学家发现硼化镁在39k时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图丁是该晶体微观空间中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同—平面上。根据图示确定硼化镁的化学式为_______________。
查看答案和解析>>
科目:高中化学 来源:2017届贵州省贵阳市高三下学期第六次适应性考试理综化学试卷(解析版) 题型:选择题
应用下列实验装置进行实验,能达到目的的是
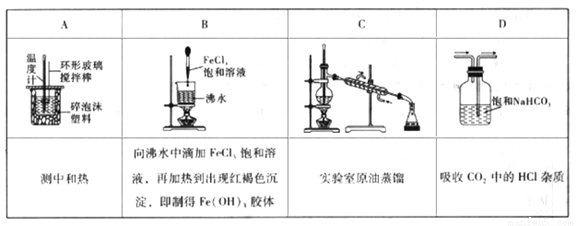
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二下学期第一次月考化学试卷(解析版) 题型:选择题
中国著名药学家屠呦呦因制成了青蒿素而获得2015年度诺贝尔生理 学或医学奖。青蒿素的结构如右图,关于该物质的分类正确的是

A.单质 B.有机物
C.无机物 D.有机高分子化合物
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二3月月考化学试卷(解析版) 题型:选择题
NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
A. 1mol —CH3(甲基)中含有的电子数为10NA
B. 标准状况下,22.4 L C3H8中含共价键的数目为8 NA
C. 标准状况下,22.4 L苯中含C—H数目为6 NA
D. 184g 甘油与足量的钠反应生成H2的数目为3 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com