
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.依据溴乙烷的性质,请你进行以下探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.依据溴乙烷的性质,请你进行以下探究.| 图序 | 装置图 | 所盛试剂 | 实验现象 |
| 1 |  | A是 | |
| 2 |  | C是 |
| H2O |
| △ |
| H2O |
| △ |


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
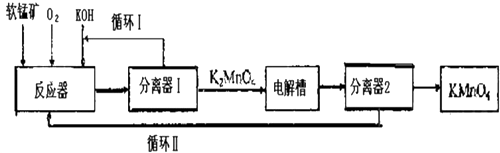
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
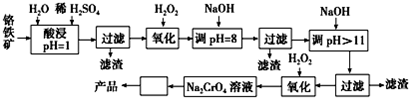
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.6 | 9.0 | -- | -- |
| 沉淀完全时的pH | 3.7 | 9.6 | 11.0 | 8 | 9(>9溶解) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳原子由基态变为激发态 |
| B、碳原子由激发态变为基态 |
| C、该过程将产生发射光谱 |
| D、碳原子要向外界环境释放能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com