
����Ŀ���ۺϷ�Ӧ���Ʊ����Ͳ��ϵ���Ҫ;��������Ȼ�ĵ���A�Ʊ��Ļ�����F��K�����Ӿ۷�Ӧ�ɵõ����߷��Ӳ��ϡ�

��֪����E�Ľṹ��ʽΪ ������������F��K���Ӿ����м���
������������F��K���Ӿ����м���
��![]()
��1��A��ϵͳ������������Ϊ_____________________��
��2����Ӧ�ٵķ�Ӧ����Ϊ________________����Ʋ���٢�Ŀ����______________��
��3���л���Ľṹ��ʽΪ_______________��
��4��д��F��K�����ʵ���1:1�����γɸ߷��ӻ�����Ļ�ѧ����ʽΪ______________________________��
��5���л�������J��ͬϵ��ұ�J��һ��̼ԭ�ӣ����ж���ͬ���칹�壬��������������������ͬ���칹����_________�֡�
a�����з��ǻ�
b���ܷ���ˮ�ⷴӦ���ܷ���������Ӧ
c�������ϵ�һ�ȴ���ֻ��һ��
d���˴Ź���������5���
��6�����������ϳ�·�ߣ����һ�����Ҷ����ͱ�Ϊԭ�ϣ����Լ���ѡ���Ʊ������� ��![]() ���ĺϳ�·��_________��
���ĺϳ�·��_________��
���𰸡� 2-��-1,3-����ϩ �ӳɷ�Ӧ ����̼̼˫���������� ![]()
 2
2 ![]()
![]()
��������A��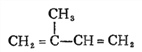 ���巢��1��4-�ӳ�����B��
���巢��1��4-�ӳ�����B��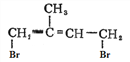 ��
�� ����������ˮ��Һ�м���ˮ�����C��
����������ˮ��Һ�м���ˮ�����C��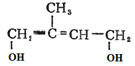 ��
�� �����Ȼ��ⷢ���ӳɷ�Ӧ����D��
�����Ȼ��ⷢ���ӳɷ�Ӧ����D��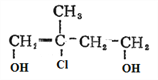 ��
��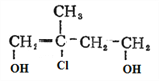 �����Ը��������������E��
�����Ը��������������E��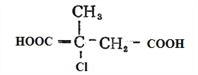 ��
�� ����������ˮ��Һ�м���ˮ������ữ�õ�G��
����������ˮ��Һ�м���ˮ������ữ�õ�G��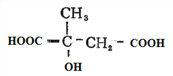 �����������Ƶ��Ҵ���Һ�м�����ȥ��Ӧ�����ữ�õ�F��
�����������Ƶ��Ҵ���Һ�м�����ȥ��Ӧ�����ữ�õ�F��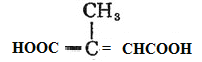 ��
��
��1����Ȼ�ĵ����������ϩ��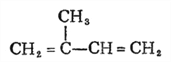 ��ϵͳ������������Ϊ��2-��-1,3-����ϩ����2����Ӧ��Ϊ�ӳɷ�Ӧ���ٵ��۷�Ӧǰ���Ϊ̼̼˫���������з���������Ӧ����϶�Ϊ����̼̼˫��������������3��H��
��ϵͳ������������Ϊ��2-��-1,3-����ϩ����2����Ӧ��Ϊ�ӳɷ�Ӧ���ٵ��۷�Ӧǰ���Ϊ̼̼˫���������з���������Ӧ����϶�Ϊ����̼̼˫��������������3��H��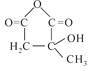 ��ת��ΪI����֪�����ƣ�
��ת��ΪI����֪�����ƣ�![]() ��H���������ɵ�I����6��̼�����Լ��ױ��뺬������ֻ��6��̼�����л���Ľṹ��ʽΪ��
��H���������ɵ�I����6��̼�����Լ��ױ��뺬������ֻ��6��̼�����л���Ľṹ��ʽΪ��![]() ��
��
��4��F��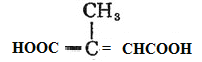 ��K�ܷ����Ӿ۷�Ӧ�Һ����м�����KΪ��
��K�ܷ����Ӿ۷�Ӧ�Һ����м�����KΪ��![]() �� F��K�����ʵ���1:1�����γɸ߷��ӻ�����Ļ�ѧ����ʽΪ��
�� F��K�����ʵ���1:1�����γɸ߷��ӻ�����Ļ�ѧ����ʽΪ��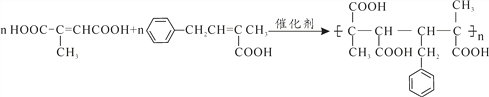 ��
��
��5���л�������J��ͬϵ��ұ�J��һ��̼ԭ�ӣ�
a�����з��ǻ����ǻ�ֱ�����ڱ����ϣ�b���ܷ���ˮ�ⷴӦ���ܷ���������Ӧ�����м������Ľṹ��c�������ϵ�һ�ȴ���ֻ��һ�֣�����ֻ�������ԳƵ�ȡ��λ��d���˴Ź���������5����������������ҵ�ͬ���칹������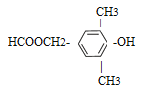 ��
��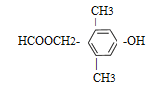 2�֣���6���Ҷ��������Ը��������Һ�б����������Ҷ��ᣬ�Ҷ�����һ��������ת��Ϊ
2�֣���6���Ҷ��������Ը��������Һ�б����������Ҷ��ᣬ�Ҷ�����һ��������ת��Ϊ![]() ��
��![]() �뱽�ڴ���������ת��Ϊ
�뱽�ڴ���������ת��Ϊ![]() ��
��![]() ��һ��������ת��Ϊ
��һ��������ת��Ϊ![]() ���ʺϳ�·��Ϊ
���ʺϳ�·��Ϊ![]()
![]() ��
��


 ����ʦ��Сһ����ʦ������ҵϵ�д�
����ʦ��Сһ����ʦ������ҵϵ�д� ���100�ֵ�Ԫ�Ż�������ϵ�д�
���100�ֵ�Ԫ�Ż�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС����ʵ������������ͼװ��(�г�װ����ȥ)�ⶨij������(FexSy)����ɣ���̽����Ӧ��Dװ��������Һ�к��������ɡ�

(һ)����(FexSy)�����
ʵ�鲽�裺
����� ��ͼ����װ�ã����װ�������ԣ�װ��ҩƷ��
����� ��Һ©����������������ˮ������ȼ�ƾ���ƣ�
����� ��Ӳ�ʲ������й����������ٸı�ʱ��ֹͣ���ȣ�����ͨ�롪��ʱ���O2
����� ʵ�������D��������Һ��ˮ���Ƴ�250 mL��Һ��
����
��ش�
������a������Ϊ______________________��
(2)������У�ֹͣ���Ⱥ������ͨ��һ��ʱ���O2����Ŀ��Ϊ__________________��
(3)����IV��������Һʱ����IJ������������������ձ��⣬����___________________��
(4)ȡ25. 00 mL����IV��������Һ������������˫��ˮ���ټ������������ữ��BaCl2��Һ�������ó������ˡ�ϴ�ӡ������������Ϊ4.66g����FexSy�Ļ�ѧʽΪ___________________��
(5)�������ۣ���ͬѧ��Ϊ�ɽ�װ��D��Ϊװ��������ʯ�ҵĸ���ܣ�ͨ���ⶨ��Ӧǰ�����ܵ�������������Ԫ�صĺ���������Ϊ�˷���________(��ǡ���)������ԭ��Ϊ_______________________��
(��)̽����Ӧ��Dװ��������Һ�к��������ɡ�
�����Ʋ⣺��Һ�г�����Na2SO4�⣬�����ܺ���Na2SO3��
ʵ��̽�����ζ����ⶨ��Һ��Na2SO3�ĺ�����
�ɹ�ѡ����Լ�����0.10 mol L-1 KmnO4������Һ ��30%H2O2
��0.10 mol L-1 KI������Һ
(6)��ѡ�Լ�Ϊ___________(�����)����ѡ�Լ�Ӧװ��_____________(���ʽ����ʽ��)�ζ����С�
�������õķ�Ӧԭ��Ϊ__________________(�����ӷ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ݻ���Ϊ10L���ܱ�������͢��з�����Ӧ��2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)����ʼ���ʵ������±���ʵ������������ͬ�¶��´ﵽƽ��ʱCO2�����ʵ���Ũ������ͼ��ʾ������˵���������
N2(g)+2CO2(g)����ʼ���ʵ������±���ʵ������������ͬ�¶��´ﵽƽ��ʱCO2�����ʵ���Ũ������ͼ��ʾ������˵���������

���� | ��ʼ���ʵ��� | ||
NO | CO | ||
�� | 1mol | 0.5mol | |
�� | 2mol | 1mol | |
A. ��ӦN2(g)+2CO2(g)![]() 2NO(g)+2CO(g)�Ħ�H��0����S��0
2NO(g)+2CO(g)�Ħ�H��0����S��0
B. P������ʱ�M����
C. M��N���������ڵ�ѹǿ�� P(M) ��2P(N)
D. N���ƽ�ⳣ��Ϊ44.4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
H��C��N��O��W��Fe��V���������뻯ѧ��ҵ�г���Ԫ�أ���ش��������⣺
��̼������CH3-�Ŀռ乹��Ϊ_______�����ݵȵ���ԭ����NO+�ĵ���ʽΪ________��
��N��Na+��Fe3+��Cu2+��������̬�ĺ�������Ų�ʽ��δ�ɶԵ�����������________��Cu2+��ˮ�г�����ɫ����Ϊ�γ���ˮ��ͭ���ӣ��仯ѧʽΪ______��

(3)���������˹��ϳɵĶ��۷��̵���ø(�ṹ��ͼ��)�����̵�ø�з�����λԭ����__________(��Ԫ�ط���)��
(4)������(�ṹ��ͼ��)�����ںϳɹ�ϸ�øNADPH�������������е�ԭ�ӵ��ӻ����������______��1 mol�÷����к��Ҽ�����ĿΪ________________��
(5)��ͼΪ̼���پ����һ���ֽṹ��̼ԭ��Ƕ������ٵľ���ļ�϶�������ƻ�ԭ�н����ľ����γ���϶+�����壬Ҳ��Ϊ��϶������ڴ˽ṹ�У�������ԭ����______����1����ԭ����Χ������ԭ�������̼ԭ����______��������ò��־�������ΪVcm3��̼���ٵ�Ħ������ΪM g/mol���ܶ�Ϊb g/cm3�����ӵ�����NA���������ݿ��Ա�ʾΪ___________________��
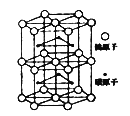
(6)12 gʯīϩ(�ṹ��ͼ��)�к��е��������ε����ʵ���Ϊ_____mol������Ԥ����Ƿ������γ�����ʯīϩ�Ľṹ����˵������____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�100mL 0.1mol/L K2SO4��Һ��������ȷ����
A. ����0.1molK2SO4 B. ˮ�����Ϊ0.1L
C. c(K+)=0.2 mol/L D. ȡ��10mL��Һ��c(K2SO4)=0.01mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(NaClO2)����Һ�ж�����ClO2��HClO2��ClO2-��Cl-�ȣ�����HClO2��ClO2���Ǿ���Ư�����á���֪pOH=��lgc(OH-)�����ⶨ25��ʱ����ֺ�����pOH�仯�����ͼ��ʾ(Cl-û�л���)�����¶��£����з�����ȷ����

A. HClO2�ĵ���ƽ�ⳣ������ֵKa=10-8
B. pOH=11ʱ��ClO2-����ת����ClO2��Cl-���ӵķ���ʽΪ��5ClO2-+2H2O=4ClO2+ Cl-+4OH-
C. pH=7ʱ����Һ�к�������Ũ�ȴ�СΪ��c(HClO2)��c(ClO2-)��c(ClO2)��c(Cl-)
D. ͬŨ�ȵ�HClO2��Һ��NaClO2��Һ�������ϣ�������Һ����c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Ԫ��Seλ�ڵ���������A�壬����˵������ȷ����
A. Se��ԭ������Ϊ34
B. ����Se�ڿ�����ȼ�տ�����SeO3
C. ���γ�Na2SeO3��Na2SeO4������
D. H2S��H2Se�ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������������������ɵ���Ⱦ��Ŀǰ�о�����Ҫ���⡣
��1��ȼú�������������·�����
�����������Ƚ���(��Ҫ�ɷ�CO��CH4��H2)��SO2�ڸ����»�ԭ�ɵ������漰�IJ��ַ�Ӧ���£�2CO(g)+SO2(g)=S(g)+2CO2(g) ��H1= + 8.0 kJ��mol-1
2CO(g)+O2(g)=2CO2(g) ��H2=��566.0kJ��mol-1
2H2(g)+O2(g)=2H2O(g) ��H3=��483.6 kJ��mol-1
��H2(g)��ԭSO2(g)����S(g)��H2O(g)���Ȼ�ѧ����ʽΪ______________________��
��һ����̼��ԭ�����ھ��Ⱥ��ݵ��ܱ������У���Ӧ2CO(g)+SO2(g)![]() S(s)+2CO2(g)�ﵽƽ��ʱ������˵����ȷ����____(�����)��
S(s)+2CO2(g)�ﵽƽ��ʱ������˵����ȷ����____(�����)��
a�������������ѹǿ���ֲ��� b�������S������Ӧ���ʼ�С
���ٳ���һ������CO2����Ӧ��ƽ�ⳣ������
���ð�ˮ��SO2ת��ΪNH4HSO3����������(NH4)2SO4��ʵ����NH4HSO3��Һ��![]() =15������Һ��pHΪ________�� (��֪��H2SO3��Ka1=1.5��10-2��Ka2=1.0��10-7)
=15������Һ��pHΪ________�� (��֪��H2SO3��Ka1=1.5��10-2��Ka2=1.0��10-7)
��2�����NO�����Ʊ�NH4NO3,�乤��ԭ������ͼ��ʾ�������ĵ缫��ӦʽΪ��____________��Ϊʹ������ȫ��ת��ΪNH4NO3���貹������A��A��___________ ��

��3��Na2S�dz��õij�������ij��ҵ��ˮ�к��е�Ũ�ȵ�Cu2+��Fe2+��Pb2+���μ�Na2S��Һ�����������ij�����________�������һ�����ӳ�����ȫʱ(������Ũ��Ϊ10-5 mol��L-1),��ʱS2-��Ũ��Ϊ_________________________
����֪: Ksp(FeS)=6.3��10-18 ��Ksp(CuS)=6��10-36 ��Ksp(PbS)=2.4��10-28��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. �е㣺�ڶ��ױ�>����ױ�>�Զ��ױ�
B. �����[��NH4Cl��Һ���ܷ������������Dz��ܺ����ᷢ����ѧ��Ӧ
C.  �л���A�ķ���ʽΪC16H16O3
�л���A�ķ���ʽΪC16H16O3
D.  ��������KMnO4��Һ����ɫ��ȥ����֤����ṹ�д���̼̼˫��
��������KMnO4��Һ����ɫ��ȥ����֤����ṹ�д���̼̼˫��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com