
分析 常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应、所有中和反应、绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应、个别的化合反应(如C和CO2)、少数分解、置换以及某些复分解反应(如铵盐和强碱).
解答 解:A.铝片与稀H2SO4反应制取H2属于放热反应;
B.氢气在氧气中燃烧属于放热反应;
C.碳酸钙高温分解成氧化钙和二氧化碳属于吸热反应;
D.氢氧化钠和盐酸中和属于放热反应;
E.Ba(OH)2•8H2O与NH4Cl反应属于吸热反应;
F.葡萄糖在人体内氧化分解是氧化反应,属于放热反应,故答案为:ABDF、CE.
点评 本题考查吸热反应,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.


科目:高中化学 来源: 题型:解答题
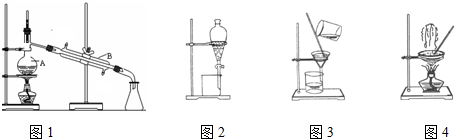
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/LHCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) | |
| B. | 1L0.1mol•L-1 CuSO4•(NH4)2SO4•6H2O的溶液中:c(${SO}_{4}^{2-}$)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) | |
| C. | 0.1mol/LNaHCO3溶液中:c(H+)+c(H2CO3)=c(${CO}_{3}^{2-}$)+c(OH-) | |
| D. | 将0.2mol/LHCN溶液和0.1mol/L的NaOH溶液等体积混合后,溶液显碱性:c(Na+)>c(HCN)>c(CN-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA | |
| B. | 通常状况下,NA个CO2分子占有的体积为22.4 L | |
| C. | 常温常压下,1.06g Na2CO3含有的Na+数为0.02 NA | |
| D. | 标准状况下,22.4L 乙醇含有的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. ;含有离子键和非极性共价键的化合物的电子式为
;含有离子键和非极性共价键的化合物的电子式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,28g C2H4含nA个碳碳双键 | |
| B. | 1mol丙烯酸中含有双键的数目为NA | |
| C. | 常温常压下,22.4L CCl4含有nA个CCl4分子 | |
| D. | 100ml0.1mol/L的醋酸溶液中含有的氢离子数为0.01NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 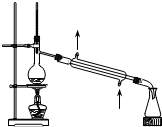 装置可用于分离苯和溴苯的混合物 | B. | 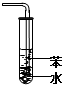 装置可用于吸收HCl或NH3气体 | ||
| C. | 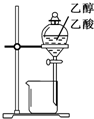 用图所示装置分离乙醇与乙酸 | D. | 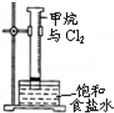 图中量筒中发生了加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com